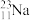现有下列物质:①O2 ②Na2O2 ③KOH ④HF ⑤H2O2 ⑥MgCl2 ⑦NH4Cl ⑧CO2,请回答下列问题(填序号):
(1)只由离子键构成的物质是___________ ;
(2)只由极性键构成的物质是___________ ;
(3)只由非极性键构成的物质是___________ ;
(4)只由非金属元素组成的离子化合物是___________ ;
(5)由极性键和非极性键构成的物质是___________ ;
(6)由离子键和极性键构成的物质是___________ ;
(7)由离子键和非极性键构成的物质是___________ 。
(1)只由离子键构成的物质是
(2)只由极性键构成的物质是
(3)只由非极性键构成的物质是
(4)只由非金属元素组成的离子化合物是
(5)由极性键和非极性键构成的物质是
(6)由离子键和极性键构成的物质是
(7)由离子键和非极性键构成的物质是
更新时间:2024-03-05 19:01:52
|
相似题推荐
填空题
|
较易
(0.85)
【推荐1】请写出下列物质的电子式:
(1)Cl2___________ (2)Na2O2 ___________ (3)NaOH ___________
(4)HCl___________ (5)H2O2___________ (6)
___________
(1)Cl2
(4)HCl

您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,请针对表中所列标号为①~⑩的元素回答下列问题。
(1)元素②的原子结构示意图是_______
(2)元素⑧在周期表中所处位置_______ ,从元素原子得失电子的角度看,元素⑤具有_______ (填“氧化性”或“还原性”)。
(3)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是_______ 。(填离子符号)
(4)第三周期元素除⑩外原子半径最大的是_______ (填元素符号),这些元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),具有两性的是_______ ,这两种物质反应的离子方程式为_______ 。
(5)⑤和⑨它们可以形成_______ (填“离子”或“共价”)化合物。
 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(1)元素②的原子结构示意图是
(2)元素⑧在周期表中所处位置
(3)元素④、⑤、⑥形成简单离子的半径由大到小的顺序是
(4)第三周期元素除⑩外原子半径最大的是
(5)⑤和⑨它们可以形成
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】(1)比较下列粒子的半径大小
①Na Mg O F__________
②Na+ Mg2+ O2- F-__________
③Fe Fe2+ Fe3+__________
④Na+ Mg2+ S2- Cl-__________
(2)下列物质中:只存在共价键的是__________ (填序号,下同),只存在离子键的是__________ ,既存在离子键又存在极性共价键的是__________ ,既存在离子键又存在非极性共价键的是__________ 。
①Ar ②CO2③Na2O2 ④KOH ⑤MgBr2⑥NH4Cl ⑦CaO ⑧H2SO4
(3)氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g) ===CO2(g)+4H2(g) 反应过程中能量变化如图所示,则该反应为__________ 反应(填“吸热”或“放热”)。若已知,破坏1mol化学键需要吸收的热量如代数式表示:
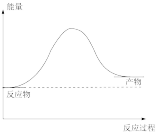
则根据该反应制取1mol H2要吸收或放出热量为___________ kJ(用含a、b、c、d字母表示)。
①Na Mg O F
②Na+ Mg2+ O2- F-
③Fe Fe2+ Fe3+
④Na+ Mg2+ S2- Cl-
(2)下列物质中:只存在共价键的是
①Ar ②CO2③Na2O2 ④KOH ⑤MgBr2⑥NH4Cl ⑦CaO ⑧H2SO4
(3)氢气可由天然气和水反应制备,其主要反应为:CH4(g)+ 2H2O(g) ===CO2(g)+4H2(g) 反应过程中能量变化如图所示,则该反应为
| 化学键 | C—H | O—H | C=O | H—H |
| 吸收热量(kJ/mol) | a | b | c | d |

则根据该反应制取1mol H2要吸收或放出热量为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】下表为元素周期表的一部分
(1)As原子的次外层电子数目为:___________
(2)NH3分子的电子式为:___________
(3)下列说法正确的是___________
A.H2S具有强还原性和热不稳定性
B.H3AsO4为弱酸
C.NH3的沸点低于PH3
D.H2O2含离子键和共价键
(4)由W、X、Y、Z四种短周期元素组成化合物如图。
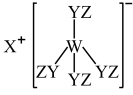
以下几种元素中可能是W元素的有___________
A.NB.AlC.BD.PE.C
(5)以下物质中含有非极性共价键的是___________
A.P4B.Na2O2C.C2H2D.CH2O
| B | N | ||
| Si | P | S | |
| As |
(2)NH3分子的电子式为:
(3)下列说法正确的是
A.H2S具有强还原性和热不稳定性
B.H3AsO4为弱酸
C.NH3的沸点低于PH3
D.H2O2含离子键和共价键
(4)由W、X、Y、Z四种短周期元素组成化合物如图。
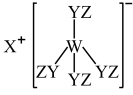
以下几种元素中可能是W元素的有
A.NB.AlC.BD.PE.C
(5)以下物质中含有非极性共价键的是
A.P4B.Na2O2C.C2H2D.CH2O
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】硅是重要的半导体材料。近日,我国宣布突破了碳基半导体材料制备的瓶颈,有望替代目前的硅材料,支持高端芯片的国产化。

(1)Si在元素周期表中的位置是___ 。
(2)制作芯片需要高纯度的硅,高纯硅中Si原子之间的相互作用是___ (填“离子键”或“共价键”)。
(3)非金属性Si弱于P,用原子结构解释原因:___ ,得电子能力Si小于P。
(4)下列关于C和Si及其化合物的推断中,正确的是___ (填序号)。
①C的最高正化合价与Si的最高正化合价相同
②SiO2具有还原性
③最高价氧化物对应水化物的酸性:H2CO3>H2SiO3

(1)Si在元素周期表中的位置是
(2)制作芯片需要高纯度的硅,高纯硅中Si原子之间的相互作用是
(3)非金属性Si弱于P,用原子结构解释原因:
(4)下列关于C和Si及其化合物的推断中,正确的是
①C的最高正化合价与Si的最高正化合价相同
②SiO2具有还原性
③最高价氧化物对应水化物的酸性:H2CO3>H2SiO3
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】回答下列问题:
(1)用电子式表示下列化合物的形成过程:
HClO :_______ ,MgCl2:_______ 。
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是_______ ;只含有非极性键的是_______ ;既含有极性键的是又含有非极性键的是_______ ;只含离子键的是_______ ;⑥含有什么键_______ ;属于离子化合物的是_______ ;属于共价化合物的是_______ 。
(1)用电子式表示下列化合物的形成过程:
HClO :
(2)有以下物质:①AlCl3 ②HClO ③H2O ④NH4Cl ⑤NaCl ⑥Na2O2 ⑦H2 ⑧H2O2 ⑨NaOH
只含有极性键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】在下列物质中:①CO2 ②KOH ③He ④BaSO4 ⑤NaCl。
(1)其中只含离子键的是(填序号,下同)_______ ,既含离子键又含共价键的是_______ ,不含化学键的是_______ 。
(2)下列物质在所述变化中:①烧碱熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。其中化学键未被破坏的是(填序号,下同)_______ ,仅发生共价键破坏的是_______ ,既发生离子键破坏,又发生共价键破坏的是_______ 。
(1)其中只含离子键的是(填序号,下同)
(2)下列物质在所述变化中:①烧碱熔化 ②HCl气体溶于水 ③NH4Cl受热分解 ④干冰升华。其中化学键未被破坏的是(填序号,下同)
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】根据所学知识,回答下列问题:
(1)写出下列物质的电子式。
Ca2+:____________
NaOH:____________
(2)写出下列物质的结构式。
N2:__________________
CH4:___________________
(3)用电子式表示HCl的形成过程:______
(4)现有下列物质①Na2SO4②CO2③HF ④Na2S ⑤C60 ⑥石墨烯,其中属于共价化合物的是___________ (填序号,下同);属于离子化合物的是 _______________ ;属于同素异形体的是________________
(1)写出下列物质的电子式。
Ca2+:
NaOH:
(2)写出下列物质的结构式。
N2:
CH4:
(3)用电子式表示HCl的形成过程:
(4)现有下列物质①Na2SO4②CO2③HF ④Na2S ⑤C60 ⑥石墨烯,其中属于共价化合物的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.回答下列问题:
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为____ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为____ (填化学式,下同),还原性由强到弱的顺序为____ ,键角由大到小的顺序为____ 。
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是____ 。
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是____ 。
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是____ 。
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O____ C2H5OH(填“>”“<”或“=”);用一个化学方程式说明OH-和C2H5O-结合H+能力的相对强弱:____ 。
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:____ 。
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是____ 。
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为____ 和____ 。
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____ ,原因是____ 。
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在____ 。
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
您最近一年使用:0次

 ②
② ③
③ ④
④