I.回答下列问题:
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为____ 。
(2)NH3、PH3、AsH3的沸点由高到低的顺序为____ (填化学式,下同),还原性由强到弱的顺序为____ ,键角由大到小的顺序为____ 。
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是____ 。
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是____ 。
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是____ 。
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O____ C2H5OH(填“>”“<”或“=”);用一个化学方程式说明OH-和C2H5O-结合H+能力的相对强弱:____ 。
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:____ 。
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是____ 。
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为____ 和____ 。
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为____ ,原因是____ 。
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在____ 。
(1)Sn为IVA族元素,单质Sn与干燥Cl2反应生成SnCl4。常温常压下SnCl4为无色液体,SnCl4空间构型为
(2)NH3、PH3、AsH3的沸点由高到低的顺序为
II.回答下列问题:
(3)气态氢化物热稳定性HF大于HCl的主要原因是
(4)CaCN2是离子化合物,各原子均满足8电子稳定结构,CaCN2的电子式是
(5)常温下,在水中的溶解度乙醇大于氯乙烷,原因是
III.回答下列问题:
(6)比较给出H+能力的相对强弱:H2O
(7)CaC2是离子化合物,各原子均满足8电子稳定结构.写出CaC2的电子式:
(8)在常压下,甲醇的沸点(65℃)比甲醛的沸点(-19℃)高,主要原因是
IV.研究发现,在CO2低压合成甲醇反应(CO2+3H2=CH3OH+H2O)中,Co氧化物负载的Mn氧化物纳米粒子催化剂具有高活性,显示出良好的应用前景。回答下列问题:
(9)CO2和CH3OH分子中C原子的杂化形式分别为
(10)在CO2低压合成甲醇反应所涉及的4种物质中,沸点从高到低的顺序为
(11)硝酸锰是制备上述反应催化剂的原料,Mn(NO3)2中的化学键除了σ键外,还存在
更新时间:2022-10-01 15:54:53
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】下表是元素周期表短周期的一部分,请参照元素①~⑨在表中的位置,回答下列问题。

(1)元素②在周期表中的位置是______________ 。
(2)元素⑤和⑨形成的化合物的电子式为__________________ 。
(3)元素④、⑤、⑥形成的简单离子的半径依次__________________ (填“增大”“减小”或“不变”)。
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是_____________ (填化学式)。
(5)元素⑥形成的单质可与⑤的最高价氧化物对应的水化物发生反应,其反应的离子方程式为___________
(6)在一定条件下,①与③可形成一种化合物X,其相对分子质量与O2相同,且X可在纯氧中燃烧,所得产物对环境均无污染,则X燃烧的化学方程式为________________

(1)元素②在周期表中的位置是
(2)元素⑤和⑨形成的化合物的电子式为
(3)元素④、⑤、⑥形成的简单离子的半径依次
(4)表中元素②、③、⑦最高价含氧酸的酸性由强到弱的顺序是
(5)元素⑥形成的单质可与⑤的最高价氧化物对应的水化物发生反应,其反应的离子方程式为
(6)在一定条件下,①与③可形成一种化合物X,其相对分子质量与O2相同,且X可在纯氧中燃烧,所得产物对环境均无污染,则X燃烧的化学方程式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】(1)第四周期中,未成对电子数最多的元素是________ ,(填名称)它位于第________ 族;核外电子排布式是__________________ 。它有________ 种运动状态不同的电子,其价电子排布图为:______________ 。
(2)已知NH5为离子化合物,写出其电子式:________ 。
(3)某同学根据掌握的知识分析Mg的核外电子排布为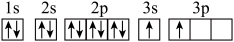 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了________ 。
(4)在基态14C原子中,核外存在________ 对自旋相反的电子。
(2)已知NH5为离子化合物,写出其电子式:
(3)某同学根据掌握的知识分析Mg的核外电子排布为
 。该同学所画的电子排布图违背了
。该同学所画的电子排布图违背了(4)在基态14C原子中,核外存在
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】下列物质:①N2 ②CO2 ③NH3 ④Na2O ⑤Na2O2 ⑥NaOH ⑦CaBr2 ⑧H2O2 ⑨NH4Cl ⑩HBr。
(1)含有极性键和非极性键的是___________ ;含有极性键的离子化合物是___________ 。(均填序号)
(2)写出下列物质的电子式H2O2___________ ;NaOH:___________ 。
(1)含有极性键和非极性键的是
(2)写出下列物质的电子式H2O2
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】下面是同学们熟悉的物质:
①O2 ②C60 ③熔融NaBr ④H2SO4 ⑤Na2CO3晶体 ⑥NH4Cl晶体 ⑦冰醋酸 ⑧CO2⑨Na2O2粉末 ⑩NaOH溶液⑪Ar
(1)这些物质中能导电,且属于电解质的是_____ (填序号,下同)。
(2)这些物质中不能导电,且属于强电解质的是_____ 。
(3)这些物质中,属于弱电解质的是______ 。
(4)这些物质中,属于非电解质的是______ 。
(5)这些物质中,属于离子化合物的是_______ 。
(6)这些物质中,直接由共价分子构成的是_____ 。
(7)这些物质中,属于纯净物,且只含有离子键的是____ 、既含有共价键又含有离子键的是___ 。
①O2 ②C60 ③熔融NaBr ④H2SO4 ⑤Na2CO3晶体 ⑥NH4Cl晶体 ⑦冰醋酸 ⑧CO2⑨Na2O2粉末 ⑩NaOH溶液⑪Ar
(1)这些物质中能导电,且属于电解质的是
(2)这些物质中不能导电,且属于强电解质的是
(3)这些物质中,属于弱电解质的是
(4)这些物质中,属于非电解质的是
(5)这些物质中,属于离子化合物的是
(6)这些物质中,直接由共价分子构成的是
(7)这些物质中,属于纯净物,且只含有离子键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐1】回答下列问题
(1)用VSEPR 理论判断:
(2)基态Fe原子有___________ 个未成对电子,Fe3+的价电子排布式为___________ 。Fe在周期表中位于___________ 列。
(3)Cl的核外电子排布式为___________ 。
(4)22Ti的原子结构示意图___________ 。
(5)Sn为ⅣA族元素,单质Sn与干燥 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为___________ 。
(1)用VSEPR 理论判断:
| 物质 | 孤对电子对数 | 轨道杂化方式 | 分子或离子的空间结构 |
PO | |||
| COCl2 |
(3)Cl的核外电子排布式为
(4)22Ti的原子结构示意图
(5)Sn为ⅣA族元素,单质Sn与干燥
 反应生成
反应生成 。常温常压下
。常温常压下 为无色液体,
为无色液体, 空间构型为
空间构型为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】按照要求填空:
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
(2)① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。
①既有 键,又有
键,又有 键的是
键的是_______ (用序号作答);既含有极性键又含有非极性键的极性分子的电子式为_______ ;既含有极性键又含有非极性键的非极性分子中碳原子的杂化方式为________ ;苯环中存在的大 键可表示为
键可表示为________ 。
②属于离子化合物的物质的电子式为______ ; 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为_____ ; 中
中 键和
键和 键之比为
键之比为______ 。
(1)判断下列分子的极性、分子的空间构型和中心原子的杂化方式。
| 序号 | 化学式 | 分子的极性 | 空间构型 | 中心原子的杂化方式 |
| ① |  | |||
| ② |  | |||
| ③ |  | - |
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦
⑦ ⑧
⑧ ⑨
⑨ 。
。①既有
 键,又有
键,又有 键的是
键的是 键可表示为
键可表示为②属于离子化合物的物质的电子式为
 与
与 结构相似,则
结构相似,则 的电子式为
的电子式为 中
中 键和
键和 键之比为
键之比为
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】已知N、P同属于元素周期表的第ⅤA族元素。 呈三角锥形,N原子位于锥顶,3个H原子位于锥底,
呈三角锥形,N原子位于锥顶,3个H原子位于锥底, 间的夹角是107°。
间的夹角是107°。
(1) 分子的空间结构为
分子的空间结构为 ,它是一种
,它是一种_______ (填“极性”成“非极性”)分子。
(2) 分子与
分子与 分子的结构
分子的结构_______ (填“相似”或“不相似”), 为
为_______ (填“极性”或“非极性”)键, 为
为_______ (填“极性”或“非极性”)分子。
(3) 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是_______ (填标号)。
a.该分子呈平面三角形b.该分子中的化学键为极性键c.该分子为极性分子
 呈三角锥形,N原子位于锥顶,3个H原子位于锥底,
呈三角锥形,N原子位于锥顶,3个H原子位于锥底, 间的夹角是107°。
间的夹角是107°。(1)
 分子的空间结构为
分子的空间结构为 ,它是一种
,它是一种(2)
 分子与
分子与 分子的结构
分子的结构 为
为 为
为(3)
 是一种淡黄色油状液体,下列对
是一种淡黄色油状液体,下列对 的有关描述不正确的是
的有关描述不正确的是a.该分子呈平面三角形b.该分子中的化学键为极性键c.该分子为极性分子
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】(1)甲烷和苯都不能使酸性高锰酸钾溶液褪色,甲苯却可以使其褪色,主要原因是_______ 。
(2)常温下硝酸为液体且易挥发,尿素为固体,两者沸点高低差异的可能原因是_______ 。
(2)常温下硝酸为液体且易挥发,尿素为固体,两者沸点高低差异的可能原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为___________ ; SiCl4是生产高纯硅的前驱体,其中Si采取的杂化轨道类型为___________ 。
(2)SiCl4可发生水解反应,机理如下:___________ (填标号)。
(3)CS2分子中存在___________ 个σ键和___________ 个π键。
(4)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是___________ 。
(5)FeCO3的阴离子的空间构型为___________ 。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为
(2)SiCl4可发生水解反应,机理如下:
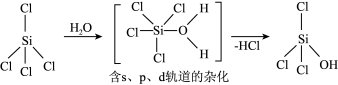
(3)CS2分子中存在
(4)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(5)FeCO3的阴离子的空间构型为
您最近一年使用:0次

 )在空气中放置一段时间漂白效果更好,这是因为和空气中的
)在空气中放置一段时间漂白效果更好,这是因为和空气中的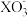 +6H+=3X2+3H2O,短周期元素X在周期表中的位置是
+6H+=3X2+3H2O,短周期元素X在周期表中的位置是 。
。 。
。

 。
。


