2021年2月22日,嫦娥五号采样返回器带回的月壤公开亮相。对月壤中化学元素的分析有助于认识月球表面环境。元素周期表揭示了化学元素间的内在联系,部分元素在周期表中的位置如下:
(1)元素c代表的元素是(写元素符号)_______ 。
(2)画出元素f的原子结构示意图_______ 。
(3)月壤中含有大量的g元素,g在周期表中的位置为_______ 。
(4)元素d、e、i所形成的简单离子半径由大到小的顺序为_______ (用离子符号表示)。
(5)元素e和i可以形成_______ (填“离子”或“共价”)化合物。
(6)g、h、i三种元素的气态氢化物最稳定的是_______ (用化学式表示)。
(7)根据元素周期律,请你试着写出e元素所对应的单质与a和d元素所形成的简单化合物反应的离子方程式:_______ 。
| a | |||||||||||||||||
| b | c | d | |||||||||||||||
| e | f | g | h | i | |||||||||||||
| j |
(2)画出元素f的原子结构示意图
(3)月壤中含有大量的g元素,g在周期表中的位置为
(4)元素d、e、i所形成的简单离子半径由大到小的顺序为
(5)元素e和i可以形成
(6)g、h、i三种元素的气态氢化物最稳定的是
(7)根据元素周期律,请你试着写出e元素所对应的单质与a和d元素所形成的简单化合物反应的离子方程式:
更新时间:2024-04-03 20:40:15
|
相似题推荐
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】下表为元素周期表的一部分,请参照给定元素的位置,回答下列问题:
(1)元素④、⑤、⑥的原子半径由大到小的顺序为_______ (用元素符号表示)。
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为_______ 。(用化学式表示)
(3)碱性强弱比较:元素⑤的氢氧化物_______ ⑥的氢氧化物(用<、=、>填空);两者相互反应的离子方程式为_______ 。
(4)由元素⑧形成的黄绿色气体单质能和溴化钠溶液发生化学反应,该反应的离子方程式为_______ ;该黄绿色气体单质也会使得湿润淀粉碘化钾试纸变蓝色,表明生成了碘单质(I2),由此推测元素⑧和碘元素形成的气态氢化物的稳定性强弱顺序为:_______ (用化学式表示)。
周期 族 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 1 | ① | |||||||
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)元素③、⑦的最高价含氧酸的酸性由强到弱的顺序为
(3)碱性强弱比较:元素⑤的氢氧化物
(4)由元素⑧形成的黄绿色气体单质能和溴化钠溶液发生化学反应,该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、X,Y、Z、R、W为六种短周期元素。A是短周期中半径最小的元素;X原子最外层电子数是核外电子层数的3倍;Y最高正价与最低负价代数和为4;Z的单质常用于漂白工业;R是短周期元素中金属性最强的元素,W是生活中的常见金属,其最高价氧化物的水化物既能与强酸反应也能与强碱反应。回答下列问题:
(1)Y元素的名称是____ ,在周期表中的位置是____ 。
(2)写出化合物AZX的电子式:____ ;化合物R2X2存在的化学键类型是____ 。
(3)比较X、Z、R三种元素对应的简单离子半径大小:____ (用离子符号和“>”表示)。
(4)下列事实能证明R比W金属性强的这一结论的是____ (填序号)。
a.R的熔点低于W b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性R>W d.最外层电子数:W>R
(5)用电子式表示RZ的形成过程:____ 。
(1)Y元素的名称是
(2)写出化合物AZX的电子式:
(3)比较X、Z、R三种元素对应的简单离子半径大小:
(4)下列事实能证明R比W金属性强的这一结论的是
a.R的熔点低于W b.常温下,R与水剧烈反应而W不能
c.最高价氧化物对应的水化物碱性R>W d.最外层电子数:W>R
(5)用电子式表示RZ的形成过程:
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
【推荐3】元素X、Y、Z、Q、R的原子序数依次增大且小于20,其原子半径和最外层电子数之间的关系如图所示。
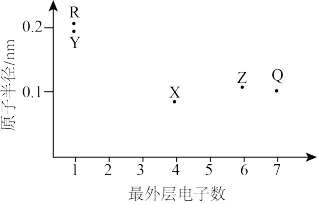
(1)Z离子的结构示意图是____ 。
(2)Q元素在周期表中位于第____ 周期____ 族;关于Q所在主族的单质及化合物的叙述错误的是____ (填标号)。
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(3)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是____ (填化学式)。
(4)Y与Q可以形成_____ (填“共价”或“离子”)化合物,用电子式表示其形成过程为____ 。
(5)Y与R金属性较强的是____ (填元素符号),请从原子结构的角度解释原因____ 。

(1)Z离子的结构示意图是
(2)Q元素在周期表中位于第
A.从上到下,单质颜色越来越深,熔、沸点越来越高
B.单质均可与水发生反应生成两种酸
C.单质均具有强氧化性,能将Fe氧化至Fe3+
D.氢化物均易溶于水,且均为强酸
(3)X、Z、Q三种元素的最高价氧化物对应的水化物酸性由强到弱的顺序是
(4)Y与Q可以形成
(5)Y与R金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐1】a、b、c、d、e、f、g为七种由短周期元素构成的微粒,它们都有10个电子,其结构特点如下:
其中,d是由极性键构成的四原子极性分子;c与f可形成共价型g分子两个。试写出:
(1)a微粒的结构示意图______ ;
(2)d溶于水的电离方程式_________________ ;
(3)c与f形成g的离子方程式___________________________________________ ;
(4)元素b与元素e的单质相比,金属性较强的是____________ (用元素符号表示),下列表述中能证明这一事实的是_________ (填编号);
A.常温下b单质的表面比e单质的表面更亮
B.b的单质投入e的氯化物水溶液能置换出e
C.b、e的最高价氧化物对应的水化物的碱性前者大
还可以用化学实验的事实加以证明,方法为_______________________ 。
| 微粒代码 | a | b | c | d | e | f | g |
| 原子核数 | 单核 | 单核 | 双核 | 多核 | 单核 | 多核 | 多核 |
| 带电荷数(单位电荷) | 0 | +1 | 1- | 0 | 2+ | 1+ | 0 |
(1)a微粒的结构示意图
(2)d溶于水的电离方程式
(3)c与f形成g的离子方程式
(4)元素b与元素e的单质相比,金属性较强的是
A.常温下b单质的表面比e单质的表面更亮
B.b的单质投入e的氯化物水溶液能置换出e
C.b、e的最高价氧化物对应的水化物的碱性前者大
还可以用化学实验的事实加以证明,方法为
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐2】如图所示是部分短周期主族元素单质熔点的变化图,根据此图回答下列问题:
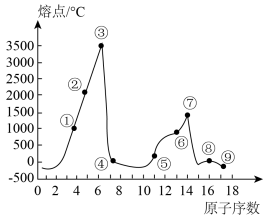
(1)③号元素在元素周期表中的位置是__________________________________ ,该元素的一种同素异形体能导电,该同素异形体的名称是__________________________________ 。
(2)⑤⑥两种元素的最高价氧化物对应的水化物之间相互反应的离子方程式为______________________ 。
(3)⑦号元素的原子结构示意图为____________________________________________________ 。
(4)②④两种元素形成的化合物晶体有两种结构,其中一种结构与金刚石相似,具有该结构的晶体属于______________________ 晶体,若使其熔化,需破坏的是________________________________ 。
(5)写出⑤和⑧形成的常见化合物的电子式________________________________________________ 。

(1)③号元素在元素周期表中的位置是
(2)⑤⑥两种元素的最高价氧化物对应的水化物之间相互反应的离子方程式为
(3)⑦号元素的原子结构示意图为
(4)②④两种元素形成的化合物晶体有两种结构,其中一种结构与金刚石相似,具有该结构的晶体属于
(5)写出⑤和⑧形成的常见化合物的电子式
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】几种主族元素在周期表中的位置如下
(1)④⑦化合物属于_______ (填“离子化合物”或“共价化合物”),其电子式为:_______ 。
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为:_______ 。
(3)比较⑤、⑥简单氢化物稳定性:_______ ;(填化学式,下同)比较①、⑥、⑦三种简单离子的半径大小:_______ 。
(4)下列可以判断①和③金属性强弱的是_______(填字母)。
(5)金属镓(Ga)常用作光学玻璃、真空管、半导体的原料。
预测Ga的化学性质并填写表格:
以上预测都是依据_______ 。
| 族 周期 | IA | 0 | ||||||
| 1 | ④ | IIA | IIIA | IVA | VA | VIA | VIIA | |
| 2 | ⑤ | ⑥ | ||||||
| 3 | ① | ③ | ⑦ | |||||
| 4 | ② | Ga | ⑧ | |||||
(2)以上元素的最高价氧化物对应的水化物的酸性最强的分子式为:
(3)比较⑤、⑥简单氢化物稳定性:
(4)下列可以判断①和③金属性强弱的是_______(填字母)。
| A.单质的熔点:①<③ |
| B.化合价:①<③ |
| C.单质与水反应的剧烈程度:①>③ |
| D.最高价氧化物对应水化物的碱性:①>③ |
预测Ga的化学性质并填写表格:
| 预测性质(所填物质类别不同) | 反应后可能的生成物(填化学式) |
| Ga能与 | 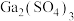 、 、 |
| Ga能与 |  、 、 |
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
【推荐1】下表是元素周期表的一部分,按要求填空(填元素符号 或化学式 ):
(1)写出③和⑧的单质反应产物的电子式________ 。
(2)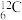 在周期表中的位置
在周期表中的位置________ ,它与氧气完全燃烧的产物的电子式________ ;
(3)在③与④的单质 中,化学性质较活泼的是________ ,判断的实验依据是________ ;
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)
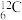 在周期表中的位置
在周期表中的位置(3)在③与④的
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
名校
解题方法
【推荐2】A、B、C、D、E是五种短周期的主族元素,它们的原子序数依次增大,A、D都能与C按原子个数比为1:1或2:1形成化合物,A、B组成的气态化合物的水溶液呈碱性,E与C的最外层电子数相同。
(1)画出D的原子结构示意图___ ,E元素在周期表中的位置是____ 。
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为____ 。
(3)D与C按原子个数比为1:1形成化合物的电子式是____ 。
(4)B、C所形成氢化物的稳定性由强到弱的顺序是____ (填化学式)。
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式____ 。
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl____ ΔH2(填“>”或“<”或“=”)。
(1)画出D的原子结构示意图
(2)A与C形成原子个数比为1:1的化合物甲,其中含有化学键类型为
(3)D与C按原子个数比为1:1形成化合物的电子式是
(4)B、C所形成氢化物的稳定性由强到弱的顺序是
(5)F是一种历史悠久、应用广泛的金属元素。若将F金属投入到盐酸溶液中,生成了浅绿色溶液M。写出M的酸性溶液和A与C形成的化合物甲反应的离子方程式
(6)E(s)+O2(g)=EO2(g)ΔH1;E(g)+O2(g)=EO2(g) ΔH2,则ΔHl
您最近一年使用:0次
解答题-无机推断题
|
较易
(0.85)
解题方法
【推荐3】元素周期表揭示了元素间的内在联系,使元素构成了一个较为系统的体系。下图为人们在研究元素间关系的过程中构建的一种表现形式,请你根据图中信息回答下列问题:
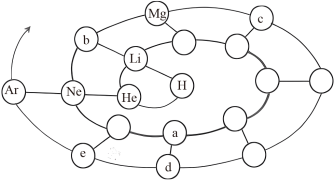
(1)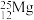 中含有的中子数为
中含有的中子数为_______ 。
(2)元素e的名称为_______ 。
(3)元素a和元素b的原子半径较大的为_______ (填元素符号)。
(4)元素a、d分别形成的简单氢化物中,稳定性较强的为_______ (填氢化物的化学式)。化合物 中化学键类型为
中化学键类型为_______ 。
(5)c单质与元素b的最高价氧化物对应的水化物的溶液反应的化学方程式为_______ 。

(1)
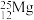 中含有的中子数为
中含有的中子数为(2)元素e的名称为
(3)元素a和元素b的原子半径较大的为
(4)元素a、d分别形成的简单氢化物中,稳定性较强的为
 中化学键类型为
中化学键类型为(5)c单质与元素b的最高价氧化物对应的水化物的溶液反应的化学方程式为
您最近一年使用:0次



