氧化还原反应是从元素化合价是否有变化的角度对化学反应进行分类的结果。结合你的认识完成下列题目。
(1)煤的气化是煤炭综合利用的重要途径之一,主要反应为:C+H2O CO+H2。氧化剂是
CO+H2。氧化剂是_______ (填化学式),碳元素的化合价_______ (填“升高”或“降低”)。
(2)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为_______ ,被还原的物质是_______ (填化学式,下同),被氧化的元素是_______ 。
(3)已知下列反应:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。被还原的HNO3与参加反应的HNO3的个数之比为_______ 。
(4)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有_______ (填“氧化性”或“还原性”)。
(5)下列各种微粒中,只具有氧化性的是_______ (填序号,下同),只具有还原性的是_______ 。
①Mg ②Cu ③Cu2+ ④H2O2 ⑤Cl- ⑥Cl2
(6)某危险品仓库中存放的化工原料氰化钠(NaCN,N元素化合价-3)有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是_______ (填序号)。
①铁粉 ②双氧水 ③臭氧(O3) ④氯化钠
(1)煤的气化是煤炭综合利用的重要途径之一,主要反应为:C+H2O
 CO+H2。氧化剂是
CO+H2。氧化剂是(2)高温下铝粉与氧化铁的反应可用来焊接钢轨。其原理是:该反应放出大量的热,置换出的铁呈熔融态。熔融的铁流入钢轨的裂缝里,冷却后就将钢轨牢牢地焊接在一起。该反应的化学方程式为
(3)已知下列反应:Fe+4HNO3(稀)=Fe(NO3)3+NO↑+2H2O。被还原的HNO3与参加反应的HNO3的个数之比为
(4)维生素C又称“抗坏血酸”,在人体内有重要的功能。例如,能帮助人体将食物中摄取的、不易吸收的Fe3+转变为易吸收的Fe2+,这说明维生素C具有
(5)下列各种微粒中,只具有氧化性的是
①Mg ②Cu ③Cu2+ ④H2O2 ⑤Cl- ⑥Cl2
(6)某危险品仓库中存放的化工原料氰化钠(NaCN,N元素化合价-3)有剧毒,一旦进入城市排水系统,后果不堪设想。当仓库发生火灾爆炸事故时,工作人员一方面封堵氰化钠泄漏渠道,另一方面对已经泄漏的少量氰化钠做无害化处理。下列物质中,可用于处理泄漏的氰化钠的是
①铁粉 ②双氧水 ③臭氧(O3) ④氯化钠
更新时间:2024-03-17 23:03:48
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】饮用水中的 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,___________ 元素被氧化,___________ 元素被还原;氧化剂是___________ ,氧化产物是___________ 。
(2)用“双线桥法”表示反应中电子转移的方向和数目_________________________________ 。
 对人类健康会产生危害,为了降低饮用水中
对人类健康会产生危害,为了降低饮用水中 的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将
的浓度,某饮用水研究人员提出,在碱性条件下用铝粉将 还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
还原为N2,其化学方程式为10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:(1)上述反应中,
(2)用“双线桥法”表示反应中电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】黄铜矿 是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
(1)若 中
中 的化合价为
的化合价为 ,反应中被还原的元素是
,反应中被还原的元素是___________ (填元素符号)。
(2)过二硫酸钾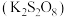 具有强氧化性,可将
具有强氧化性,可将 氧化为
氧化为 :
: 。通过改变反应途径,
。通过改变反应途径, 均可催化上述反应。试用离子方程式表示
均可催化上述反应。试用离子方程式表示 对上述反应催化的过程:
对上述反应催化的过程:___________ 、___________ 。
 是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物。冶炼铜的反应为:
(1)若
 中
中 的化合价为
的化合价为 ,反应中被还原的元素是
,反应中被还原的元素是(2)过二硫酸钾
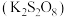 具有强氧化性,可将
具有强氧化性,可将 氧化为
氧化为 :
: 。通过改变反应途径,
。通过改变反应途径, 均可催化上述反应。试用离子方程式表示
均可催化上述反应。试用离子方程式表示 对上述反应催化的过程:
对上述反应催化的过程:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】实验室可用KMnO4和浓盐酸反应制取氯气,其变化可表述为2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl↑2+8H2O。
(1)请将上述化学方程式改写为离子方程式:__ 。
(2)浓盐酸在反应中显示出来的性质是__ (填编号)。
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)此反应中氧化产物是Cl2,若产生0.5molCl2,则转移电子的物质的量为__ mol。
(4)用双线桥法表示该反应电子转移的方向和数目__ 。
(1)请将上述化学方程式改写为离子方程式:
(2)浓盐酸在反应中显示出来的性质是
①只有还原性②还原性和酸性③只有氧化性④氧化性和酸性
(3)此反应中氧化产物是Cl2,若产生0.5molCl2,则转移电子的物质的量为
(4)用双线桥法表示该反应电子转移的方向和数目
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】 在氧化还原反应中,氧化剂______ 电子,发生的反应是______ 反应;还原剂______ 电子,发生的反应是______ 反应。铁与氯气反应的方程式为,2Fe+3Cl2=2FeCl3生成物中铁是______ 价,铁与盐酸的反应式为______ ,生成物中铁是______ 价,事实证明,氯气的氧化性比盐酸的氧化性(填“强”“弱”)______ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】工业上利用电解饱和食盐水生产氯气(Cl2)、烧碱和氢气的化学方程式是:2NaCl+2H2O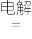 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑
(1)用单线桥表示出电子转移的方向和数目__ ,题干中反应改写成离子方程式是___ 。
(2)电解食盐水的过程中,被氧化的元素是__ ,被还原的元素是___ ,氧化产物是___ 。
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO 、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
①氯化钡、纯碱、烧碱分别除去的离子是___ 、____ 、____ 。
②盐酸与滤液反应的离子方程式:___ 、___ 。
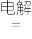 2NaOH+Cl2↑+H2↑
2NaOH+Cl2↑+H2↑(1)用单线桥表示出电子转移的方向和数目
(2)电解食盐水的过程中,被氧化的元素是
(3)电解食盐水要求对粗食盐水进行精制,以除去粗食盐水中含有的泥沙和SO
 、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。
、Ca2+、Mg2+等杂质离子。精制时依次加入氯化钡溶液、纯碱、烧碱,充分反应后过滤,在滤液中加入盐酸中和至中性。①氯化钡、纯碱、烧碱分别除去的离子是
②盐酸与滤液反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】《南村辍耕录》中记载:“杭人削松木为小片,其薄如纸,熔硫磺涂木片顶端分许,名曰发烛。”《资治通鉴》中记载:“陈宣帝太建九年,齐后妃贫苦,至以卖烛为业。”文中的“发烛”就是原始的火柴。已知K2Cr2O7用于工业中制造火柴头。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)___ (填元素名称 )元素被氧化,__ (填化学式 ,下同)是氧化剂。
(2)__ 是氧化产物,__ 发生氧化反应。
(3)参加反应的盐酸,表现了__ 性质。(填“还原性”“氧化性”或“酸性”)
(4)该反应中每生成3分子Cl2转移电子个数为__ 个。
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目___ 。

K2Cr2O7+HCl(浓)→KCl+CrCl3+Cl2↑+H2O(未配平)
(1)
(2)
(3)参加反应的盐酸,表现了
(4)该反应中每生成3分子Cl2转移电子个数为
(5)配平上述反应,并用单线桥表示出该反应电子转移的方向和数目
您最近一年使用:0次



