按要求写出或完成下列方程式。(共15分)
(1)HNO3的电离方程式:___________ 。
(2)Na2CO3的电离方程式:___________ 。
(3)Zn与HCl反应的离子方程式:___________ 。
(4)HCl和NaOH反应的离子方程式:___________ 。
(5)将下列方程式配平:___________ 。
_______KMnO4+_______HCl(浓) _______KCl+_______MnCl2+_______H2O+_______Cl2↑
(1)HNO3的电离方程式:
(2)Na2CO3的电离方程式:
(3)Zn与HCl反应的离子方程式:
(4)HCl和NaOH反应的离子方程式:
(5)将下列方程式配平:
_______KMnO4+_______HCl(浓) _______KCl+_______MnCl2+_______H2O+_______Cl2↑
更新时间:2024-03-19 18:58:30
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】(1)下列物质中:①铝 ②Cl2 ③稀H2SO4 ④SO2 ⑤NH3 ⑥HCl ⑦CaCO3 ⑧Ba(OH)2 ⑨乙醇 ⑩NaCl溶液
属于电解质的是____ ,属于非电解质的是____ ,固态和熔化状态都不导电,溶于水后能导电且是非电解质的是____ (用序号填写)。
(2)Al2(SO4)3的电离方程式为_____ ,Ba(OH)2的电离方程式为____ 。
(3)①和③反应的离子方程式为____ ,④和⑧反应的离子方程式为_____ 。
(4)二氧化氮是造成光化学烟雾的罪魁祸首。目前有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨把二氧化氮还原为氮气和水。请写出该反应的化学方程式:____ 。
属于电解质的是
(2)Al2(SO4)3的电离方程式为
(3)①和③反应的离子方程式为
(4)二氧化氮是造成光化学烟雾的罪魁祸首。目前有一种治理方法是在400℃左右、有催化剂存在的情况下,用氨把二氧化氮还原为氮气和水。请写出该反应的化学方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】写出下列物质的电离方程式
(1)HNO3=____________
(2)KOH=_____________
(3)Fe2(SO4)3=___________
(4)NaCl=_____________
(1)HNO3=
(2)KOH=
(3)Fe2(SO4)3=
(4)NaCl=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】有下列物质:①NaCl固体 ②盐酸 ③ 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态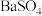 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):
(1)属于电解质的是_______ ;属于非电解质的是_______ 。
(2)上述状态下可导电的物质是_______ ;
(3) 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。
① 溶于水时的电离方程式
溶于水时的电离方程式_______ 。
②少量 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为_______ 。
③写出澄清石灰水与过量二氧化碳反应的离子方程式:_______ 。
 溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇(
溶液 ④铜 ⑤二氧化碳气体 ⑥硫酸氢钾固体 ⑦乙醇( ) ⑧液态硫酸 ⑨熔融态
) ⑧液态硫酸 ⑨熔融态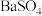 ⑩液态
⑩液态 。请回答下列问题(用序号):
。请回答下列问题(用序号):(1)属于电解质的是
(2)上述状态下可导电的物质是
(3)
 是一种酸式盐,可用作清洁剂、防腐剂等。
是一种酸式盐,可用作清洁剂、防腐剂等。①
 溶于水时的电离方程式
溶于水时的电离方程式②少量
 与
与 溶液混合,该反应的离子方程式为
溶液混合,该反应的离子方程式为③写出澄清石灰水与过量二氧化碳反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】描述下列反应的现象并写出反应的离子方程式。
(1)向FeCl3溶液中滴加NaOH溶液,现象:__________________ ,离子方程式:____________________
(2)向NaHCO3溶液中滴加稀H2SO4,现象:__________________ ,离子方程式:__________________
(3)稀HNO3和Ba(OH)2溶液混合,现象:__________________ ,离子方程式:____________________
(4)比较:上述三个离子反应发生的条件的不同点是______________________ ;相同点是________________
(1)向FeCl3溶液中滴加NaOH溶液,现象:
(2)向NaHCO3溶液中滴加稀H2SO4,现象:
(3)稀HNO3和Ba(OH)2溶液混合,现象:
(4)比较:上述三个离子反应发生的条件的不同点是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】现有以下物质:①NaCl晶体②液态HCl③ 固体④熔融KC1⑤蔗糖⑥铜⑦
固体④熔融KC1⑤蔗糖⑥铜⑦ ⑧KOH溶液⑨淀粉溶液(填序号)
⑧KOH溶液⑨淀粉溶液(填序号)
(1)以上物质中是非电解质的是___________ ,属于电解质的是___________ 。
(2)写出上述物质之间发生的中和反应的离子方程式___________ 。
(3)能用⑨检验的物质的化学式为___________ ,KOH的电离方程式为___________ 。
(4)熔融KC1与铜都能导电,导电原理分别是___________ 。
(5)KOH的水溶液和淀粉溶液共同具备的性质是___________(填序号)。
 固体④熔融KC1⑤蔗糖⑥铜⑦
固体④熔融KC1⑤蔗糖⑥铜⑦ ⑧KOH溶液⑨淀粉溶液(填序号)
⑧KOH溶液⑨淀粉溶液(填序号)(1)以上物质中是非电解质的是
(2)写出上述物质之间发生的中和反应的离子方程式
(3)能用⑨检验的物质的化学式为
(4)熔融KC1与铜都能导电,导电原理分别是
(5)KOH的水溶液和淀粉溶液共同具备的性质是___________(填序号)。
| A.都属于分散系 | B.都能产生丁达尔效应 |
| C.都可以利用半透膜分离出分散质 | D.都能与I2反应 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】下列几种物质:①NaHCO3晶体;②Na2O2;③NaHSO4溶液;④CO2;⑤Ba(OH)2溶液;⑥C2H5OH(酒精);⑦KMnO4;⑧氨水;⑨饱和FeCl3溶液。
根据要求回答下列问题:
(1)上述各物质属于电解质的是_______ (填物质编号,下同);属于非电解质的是_______ 。
(2)③中盐的电离方程式为_______ ;⑦在水中的电离方程式为_______ 。
(3)写出少量④通入⑤中反应的离子方程式:_______ ;③和⑧在水溶液中反应的离子方程式:_______
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:_______
(5)向③中加入⑤至溶液中恰好沉淀完全,写出该反应的离子方程式:_______ 。
根据要求回答下列问题:
(1)上述各物质属于电解质的是
(2)③中盐的电离方程式为
(3)写出少量④通入⑤中反应的离子方程式:
(4)将⑨加入到沸水中,继续加热溶液呈红褐色,即制得Fe(OH)3胶体,写出该反应的离子方程式:
(5)向③中加入⑤至溶液中恰好沉淀完全,写出该反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】回答下列问题:
(1)下列物质中,只存在离子键的是____ ,只存在共价键的是____ ,属于共价化合物的是____ (以上各空都填序号)。
①白磷 ②CaCl2 ③CH4 ④K2O2 ⑤AlCl3 ⑥MgO ⑦Ba(OH)2 ⑧HBr
(2)某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于或等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义。将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
根据表中数据计算该试样中x=____ 。
(3)煤燃烧排放的烟气含有SO2和NOx,能形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可使烟气中的NO转化为NO ,同时测得消耗90.5gNaClO2时,共转移了4mol电子,则反应的离子方程式为
,同时测得消耗90.5gNaClO2时,共转移了4mol电子,则反应的离子方程式为____ 。
(4)人体血液里Ca2+的质量浓度一般采用mg•cm-3来表示,抽取20.00mL血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙[CaC2O4]沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4)再用酸化的0.020mol·L-1KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL酸性KMnO4溶液。经过计算,血液样品中Ca2+的质量浓度为____ mg•cm-3(已知草酸与酸性KMnO4溶液反应的离子方程式为5H2C2O4+2MnO +6H+=2Mn2++10CO2↑+8H2O)。
+6H+=2Mn2++10CO2↑+8H2O)。
(1)下列物质中,只存在离子键的是
①白磷 ②CaCl2 ③CH4 ④K2O2 ⑤AlCl3 ⑥MgO ⑦Ba(OH)2 ⑧HBr
(2)某城市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于或等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等.因此,对PM2.5、SO2、NOx等进行研究具有重要意义。将PM2.5样本用蒸馏水处理制成待测试样。若测得该试样所含水溶性无机离子的化学组分及其平均浓度如表:
| 离子 | H+ | K+ | Na+ | NH | SO | NO | Cl- |
| 浓度/mol·L-1 | x | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
根据表中数据计算该试样中x=
(3)煤燃烧排放的烟气含有SO2和NOx,能形成酸雨,污染大气,采用NaClO2溶液在碱性条件下可使烟气中的NO转化为NO
 ,同时测得消耗90.5gNaClO2时,共转移了4mol电子,则反应的离子方程式为
,同时测得消耗90.5gNaClO2时,共转移了4mol电子,则反应的离子方程式为(4)人体血液里Ca2+的质量浓度一般采用mg•cm-3来表示,抽取20.00mL血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙[CaC2O4]沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4)再用酸化的0.020mol·L-1KMnO4溶液滴定,使草酸转化成CO2逸出,这时共消耗12.00mL酸性KMnO4溶液。经过计算,血液样品中Ca2+的质量浓度为
 +6H+=2Mn2++10CO2↑+8H2O)。
+6H+=2Mn2++10CO2↑+8H2O)。
您最近一年使用:0次
【推荐2】含氮废水进入水体中对环境造成的污染越来越严重。某校环保小组的同学认为可以用金属铝将水中的NO还原成N2,从而消除氮污染。
(1)配平以下有关的离子反应方程式: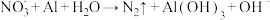
____________
(2)以上反应中失电子的物质是________ ,还原产物是________ ,每生成1 mol还原产物,将有___ 个电子发生转移。
(3)现需除去1 m3含氮0.3 mol的废水中的NO(设氮元素都以NO的形式存在),则至少 需要消耗金属铝的物质的量为________ 。
(1)配平以下有关的离子反应方程式:
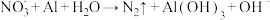
(2)以上反应中失电子的物质是
(3)现需除去1 m3含氮0.3 mol的废水中的NO(设氮元素都以NO的形式存在),则至少 需要消耗金属铝的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
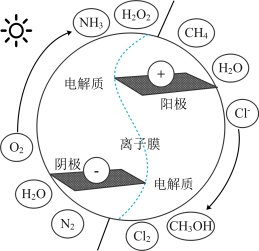
【推荐3】将地球储量丰富的小分子电催化转化为有高附加值的 、
、 、
、 及
及 (如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(1) 是一种绿色氧化剂,它的电子式为
是一种绿色氧化剂,它的电子式为___________ ;目前工业上采用蒽醌法生产 的原理为:
的原理为:
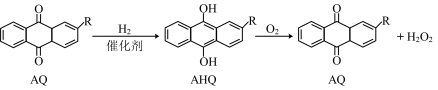 。
。
该总反应的原子利用率为___________ %;测定 的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为
的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为___________ 。
(2) 还原
还原 制取X(方程式中部分物质的化学计量数已略)可表示为
制取X(方程式中部分物质的化学计量数已略)可表示为
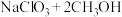


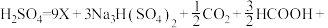

 ,则X为
,则X为___________ (填化学式)。
(3)电催化制取有高附加值物质的方法有很多。
①下列说法错误的是___________ (填标号)。
A. 及
及 电催化制
电催化制 时,
时, 在阴极区生成
在阴极区生成
B. 及
及 电催化制
电催化制 时,
时, 在阳极区生成
在阳极区生成
C.隔膜电解槽电解饱和食盐水制 时,用阴离子交换膜
时,用阴离子交换膜
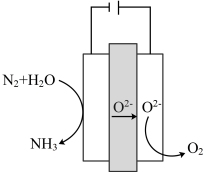
②一种合成氨的装置如图所示,阴极的电极反应式为___________ ,电解总反应为___________ 。
 、
、 、
、 及
及 (如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(如图所示)等具有巨大的经济效益和环境效益。回答下列问题:
(1)
 是一种绿色氧化剂,它的电子式为
是一种绿色氧化剂,它的电子式为 的原理为:
的原理为: 。
。该总反应的原子利用率为
 的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为
的纯度可用酸性高锰酸钾溶液滴定法,该反应的离子方程式为(2)
 还原
还原 制取X(方程式中部分物质的化学计量数已略)可表示为
制取X(方程式中部分物质的化学计量数已略)可表示为
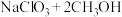


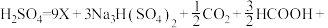

 ,则X为
,则X为(3)电催化制取有高附加值物质的方法有很多。
①下列说法错误的是
A.
 及
及 电催化制
电催化制 时,
时, 在阴极区生成
在阴极区生成B.
 及
及 电催化制
电催化制 时,
时, 在阳极区生成
在阳极区生成C.隔膜电解槽电解饱和食盐水制
 时,用阴离子交换膜
时,用阴离子交换膜②一种合成氨的装置如图所示,阴极的电极反应式为

您最近一年使用:0次



