现有下列9种物质:① ;②
;② ;③HCl;④
;③HCl;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;按要求填空(填序号)。
;按要求填空(填序号)。
(1)只由离子键构成的物质是_____________ 。
(2)由极性键和非极性键构成的物质是_____________ 。
(3)由离子键和非极性键构成的物质是__________________________ 。
(4)属于共价化合物的物质是_____________ 。
(5)③溶于水时破坏_____________ (填离子键或共价键,下同),⑥熔化时破坏_____________ 。
(6)向⑥的溶液中滴加少量⑧的溶液,反应的离子方程式为_____________________ 。
 ;②
;② ;③HCl;④
;③HCl;④ ;⑤
;⑤ ;⑥
;⑥ ;⑦
;⑦ ;⑧
;⑧ ;⑨
;⑨ ;按要求填空(填序号)。
;按要求填空(填序号)。(1)只由离子键构成的物质是
(2)由极性键和非极性键构成的物质是
(3)由离子键和非极性键构成的物质是
(4)属于共价化合物的物质是
(5)③溶于水时破坏
(6)向⑥的溶液中滴加少量⑧的溶液,反应的离子方程式为
更新时间:2024-04-03 21:42:15
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】完成下列问题
(1)完成下列反应的离子方程式,注意难溶、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸:___________ 。
②向AlCl3溶液中滴加过量的氨水:___________ 。
③小苏打溶液与乙酸溶液混合:___________ 。
④向NaHSO3溶液中加入过量NaHSO4溶液:___________ 。
(2)按要求完成下列反应的离子方程式,注意微溶物质、NH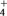 与碱反应的条件。
与碱反应的条件。
①向澄清石灰水中加入稀盐酸:___________ 。
②石灰乳与Na2CO3溶液反应:___________ 。
③Na2SO4溶液与AgNO3溶液混合:___________ 。
④NH4Cl与NaOH两种稀溶液混合:___________ 。
(3)完成下列反应的离子方程式,注意单质、氧化物、浓盐酸、浓硝酸、浓硫酸的书写形式。
①过氧化钠溶于水:___________ 。
②FeCl3溶液腐蚀铜箔:___________ 。
③用MnO2与浓盐酸共热制Cl2:___________ 。
④铜与浓硝酸反应:___________ 。
⑤硫化钠溶液与浓硫酸反应:___________ 。
(4)多重反应。完成下列反应的离子方程式。
①Ba(OH)2+H2SO4:___________ 。
②CuSO4+Ba(OH)2:___________ 。
③向HI溶液中加入少量Fe(OH)3:___________ 。
④FeO溶于稀硝酸中:___________ 。
(1)完成下列反应的离子方程式,注意难溶、气体、难电离微粒的书写形式。
①氧化镁溶于稀硫酸:
②向AlCl3溶液中滴加过量的氨水:
③小苏打溶液与乙酸溶液混合:
④向NaHSO3溶液中加入过量NaHSO4溶液:
(2)按要求完成下列反应的离子方程式,注意微溶物质、NH
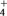 与碱反应的条件。
与碱反应的条件。①向澄清石灰水中加入稀盐酸:
②石灰乳与Na2CO3溶液反应:
③Na2SO4溶液与AgNO3溶液混合:
④NH4Cl与NaOH两种稀溶液混合:
(3)完成下列反应的离子方程式,注意单质、氧化物、浓盐酸、浓硝酸、浓硫酸的书写形式。
①过氧化钠溶于水:
②FeCl3溶液腐蚀铜箔:
③用MnO2与浓盐酸共热制Cl2:
④铜与浓硝酸反应:
⑤硫化钠溶液与浓硫酸反应:
(4)多重反应。完成下列反应的离子方程式。
①Ba(OH)2+H2SO4:
②CuSO4+Ba(OH)2:
③向HI溶液中加入少量Fe(OH)3:
④FeO溶于稀硝酸中:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐2】有下列物质:①氢氧化钡固体 ②Al2(SO4)3③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铁 ⑦碳酸钠粉末 ⑧蔗糖 ⑨熔融氯化钠 ⑩ 。 请回答下列问题:
。 请回答下列问题:
(1)可以导电的有______________ ,属于电解质的有____________ ,属于非电解质的有__________ ,
(2)②在水中的电离方程式为__________________________________________ ,
(3)请写出④与⑥反应的离子方程式____________________________________ ,
(4)请写出⑤与①的溶液反应的离子方程式____________________________________ 。
(5)请写出⑤通入⑦溶液反应的离子方程式____________________________________ 。
(6)物质③HCl具有_______________ (填写“氧化性”、“还原性”或者“氧化性和还原性”),理由是____________________ ,物质⑥铁在氧化还原反应中应该只能表现___________ (填“氧化性”和“还原性”)。
 。 请回答下列问题:
。 请回答下列问题:(1)可以导电的有
(2)②在水中的电离方程式为
(3)请写出④与⑥反应的离子方程式
(4)请写出⑤与①的溶液反应的离子方程式
(5)请写出⑤通入⑦溶液反应的离子方程式
(6)物质③HCl具有
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】实验室药品橱柜中摆列着如下试剂和药品:①稀盐酸,②氢氧化钠固体,③氢氧化钠溶液,④铜,⑤氯化钠固体,⑥硝酸银溶液,⑦酒精,⑧碳酸钠固体,⑨碳酸钾固体;回答下面问题:
(1)氯化钠、碳酸钠与碳酸钾有如下关系:
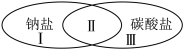
该分类属于___________ (填“树状分类法”或“交叉分类法”)。属于图II部分的是___________ (填“氯化钠”“碳酸钠”或“碳酸钾”)。
(2)上述9种试剂或药品中属于电解质的是___________ (填序号,下同),属于非电解质的是___________ ,能导电但既不属于电解质也不属于非电解质的是___________ 。
(3)写出①稀盐酸与③氢氧化钠溶液反应的离子方程式___________ 。写出①稀盐酸与⑥硝酸银溶液反应的离子方程式___________ 。
(4)过量①稀盐酸分别与⑧碳酸钠固体和⑨碳酸钾固体反应,离子方程式是否相同?___________ (填“是”或“否”)。写出该反应的离子方程式___________ (若离子方程式相同只写一个,若离子方程式不同写两个,注意易溶于水的电解质要先溶于水再发生反应)。
(1)氯化钠、碳酸钠与碳酸钾有如下关系:

该分类属于
(2)上述9种试剂或药品中属于电解质的是
(3)写出①稀盐酸与③氢氧化钠溶液反应的离子方程式
(4)过量①稀盐酸分别与⑧碳酸钠固体和⑨碳酸钾固体反应,离子方程式是否相同?
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】有以下9种物质:①Ne ②HCl ③P4 ④H2O2 ⑤Na2S ⑥NaOH ⑦Na2O2 ⑧NH4Cl ⑨AlCl3.请用上述物质的序号填空:
(1)不存在化学键的是___________ 。
(2)只存在极性共价键的是___________ 。
(3)只存在非极性共价键的是___________ 。
(4)既存在非极性共价键又存在极性共价键的是___________ 。
(5)只存在离子键的是___________ 。
(6)既存在离子键又存在共价键的是___________ 。
(1)不存在化学键的是
(2)只存在极性共价键的是
(3)只存在非极性共价键的是
(4)既存在非极性共价键又存在极性共价键的是
(5)只存在离子键的是
(6)既存在离子键又存在共价键的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】I.有下列物质:①Na2O ②NaOH ③NH4Cl ④CO2 ⑤H2S ⑥Ar
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是___________ ,属于共价化合物的是___________ 。
(2)只含有离子键的是___________ ,既含有离子键又含有共价键的是___________ 。
(3)不存在化学键的是______________ 。
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于_ 晶体,KBr可能属于__ 晶体。
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于__ 晶体,写出BaCl2的电子式:____ 。
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是____ 晶体,而SiC可能是____ 晶体。
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;_____ 。
(8)______MnO +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;_____
⑦H2SO4 ⑧KCl (填序号)
(1)属于离子化合物的是
(2)只含有离子键的是
(3)不存在化学键的是
Ⅱ.
(4)BBr3的熔点是-46 ℃,KBr的熔点是734 ℃,其水溶液能导电。根据熔点分析,BBr3可能属于
(5)BaCl2是无色晶体,熔点963 ℃,沸点1 560 ℃,易溶于水,在熔化状态能导电。它可能属于
(6)SiC和CO2物质中的化学键均为共价键,SiC的熔点高且硬度大,而CO2的晶体干冰却松软而且极易升华。由此可判断,CO2是
Ⅲ.配平下列氧化还原反应方程式:
(7)______Fe+_____HNO3=______Fe(NO3)3+______NO↑+______H2O;
(8)______MnO
 +_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
+_____Cl-+____H+ = Mn2++______Cl2↑+______H2O;
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
解题方法
【推荐3】填写下列空白:
(1)写出表示含有8个质子、10个中子的原子的化学符号:________ 。
(2)周期表中位于第8纵行的铁元素属于第________ 族。
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)_________ ;只含有极性共价键的化合物是________ ;
(4)HClO的结构式______ ,I2的电子式______ 。
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是_____ ;
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是_____________
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
(1)写出表示含有8个质子、10个中子的原子的化学符号:
(2)周期表中位于第8纵行的铁元素属于第
(3)下列几种物质:①Ca(OH)2②H2O2③He④H2S ⑤MgCl2 ,只含有离子键的是(选填序号,下同)
(4)HClO的结构式
(5)下列变化中:①干冰气化;②硝酸钾熔化;③KHSO4熔融;④蔗糖溶液水⑤硫酸溶于水;未破坏化学键的是
(6)下列不能说明氯元素原子得电子能力比硫元素原子得电子能力强的是
①HCl的溶解度比H2S的大 ②HCl的酸性比H2S的强 ③HCl的稳定性比H2S的强④Cl2与铁反应生成FeCl3,而S与铁反应生成FeS ⑤HClO4的酸性比H2SO4的强 ⑥Cl2能与H2S反应生成S
您最近一年使用:0次



