Cu2O溶于浓氨水中形成无色的[Cu(NH3)2]+,该无色溶液接触空气会很快变成深蓝色。
(1)[Cu(NH3)2]+中NH3的N原子提供___________,与中心离子形成___________。
| A.空轨道、离子键 | B.孤电子对、离子键 |
| C.空轨道、配位键 | D.孤电子对、配位键 |
| A.大于107° | B.小于107° | C.等于107° | D.等于120° |
完成并配平上述离子方程式。
更新时间:2024-03-27 09:07:56
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】按要求完成下列问题
(1)写出足量 与
与 的离子反应方程式
的离子反应方程式_______ 。
(2) 与过量
与过量 反应的离子反应方程式
反应的离子反应方程式_______ 。
(3)配平该反应_______ 。
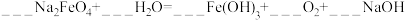
(4)_______ 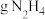 所含原子数与
所含原子数与 含原子数相同。
含原子数相同。
(1)写出足量
 与
与 的离子反应方程式
的离子反应方程式(2)
 与过量
与过量 反应的离子反应方程式
反应的离子反应方程式(3)配平该反应
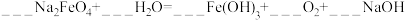
(4)
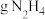 所含原子数与
所含原子数与 含原子数相同。
含原子数相同。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】Ⅰ.铁原子结构示意图及元素周期表中铁元素的部分信息如图。
(1)下列有关说法正确的是_______ 。
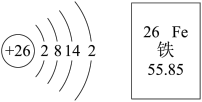
a.铁元素位于元素周期表的第六周期 b.Fe3+的电子数为24
c.1 mol铁的质量为55.85 g e.加热下,铁与硫反应生成Fe2S3
Ⅱ.碱式氯化铜[CuaClb(OH)c∙xH2O]制备需要的CuCl2可用Fe3+作催化剂得到,其催化原理如图所示。

(2)上述转化过程中Cu2+与O2个数比______ 。
(3)图中M、N分别为______ ,______ 。
(4)a、b、c之间的等式关系式为_________ 。
(5)N参加的反应离子方程式为_________ 。
(1)下列有关说法正确的是
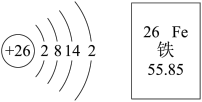
a.铁元素位于元素周期表的第六周期 b.Fe3+的电子数为24
c.1 mol铁的质量为55.85 g e.加热下,铁与硫反应生成Fe2S3
Ⅱ.碱式氯化铜[CuaClb(OH)c∙xH2O]制备需要的CuCl2可用Fe3+作催化剂得到,其催化原理如图所示。

(2)上述转化过程中Cu2+与O2个数比
(3)图中M、N分别为
(4)a、b、c之间的等式关系式为
(5)N参加的反应离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求书写方程式
(1) 在水溶液中的电离方程式
在水溶液中的电离方程式___________ 。
(2)碳酸钙溶解在醋酸中的离子反应方程式___________ 。
(3)除去 粉末中混有少量
粉末中混有少量 的化学方程式
的化学方程式___________ 。
(4)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是___________ 。
(5)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的高锰酸钾,配平该反应的离子方程式:________ 。

(1)
 在水溶液中的电离方程式
在水溶液中的电离方程式(2)碳酸钙溶解在醋酸中的离子反应方程式
(3)除去
 粉末中混有少量
粉末中混有少量 的化学方程式
的化学方程式(4)“84”消毒液与除垢剂(有效成分是盐酸)混合使用会产生黄绿色、有刺激性气味的气体,该反应的离子方程式是
(5)衣服上不小心沾到了蓝色墨水,可以先涂上酸性高锰酸钾溶液,即可除去蓝墨水中的鞣酸亚铁,再用乙二酸的稀溶液擦洗,可以迅速除去过量的高锰酸钾,配平该反应的离子方程式:

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】铜的化合物用途非常广泛。已知下列反应:[Cu(NH3)2]++NH3+CO ⇌ [Cu(NH3)3CO]+,2CH3COOH +2CH2=CH2+O2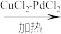 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。
(1)Cu2+基态核外电子排布式为______ 。
(2)NH3分子空间构型为_______ , 其中心原子的杂化类型是______ 。
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是_______ ,1mol CH3COOCH=CH2中含 键数目为
键数目为_____ 。
(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为__________ 。
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构示意图表示为____
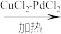 2CH3COOCH=CH2+2H2O。
2CH3COOCH=CH2+2H2O。(1)Cu2+基态核外电子排布式为
(2)NH3分子空间构型为
(3)CH3COOCH=CH2分子中碳原子轨道的杂化类型是
 键数目为
键数目为(4)CH3COOH可与H2O混溶,除因为它们都是极性分子外,还因为
(5)配离子[Cu(NH3)3CO]+中NH3及CO中的C与Cu(Ⅰ)形成配位键。不考虑空间构型,[Cu(NH3)3CO]+的结构示意图表示为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】非金属及其化合物在生产、生活中应用广泛。
Ⅰ.CO2的有效利用可以缓解温室效应和能源短缺问题,CO2的分子结构决定了其性质和用途。
(1)CO2的电子式是______ ,包含的化学键类型为______ 共价键(填“非极性”或“极性”)。
(2)在温度高于31.26 oC、压强高于7.29×106 Pa时,CO2处于超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有______ (答出一点即可)。
Ⅱ.氯水以及氯的化合物经常用于饮用水的消毒。
(3)将铁片插入盛有少量新制氯水的试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为______ 。
(4)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为___________ 。
②亚硫酸钠将水中多余次氯酸除去的反应的化学方程式为_______________ 。
Ⅰ.CO2的有效利用可以缓解温室效应和能源短缺问题,CO2的分子结构决定了其性质和用途。
(1)CO2的电子式是
(2)在温度高于31.26 oC、压强高于7.29×106 Pa时,CO2处于超临界状态,称为超临界CO2流体,可用作萃取剂提取草药中的有效成分。与用有机溶剂萃取相比,超临界CO2萃取的优点有
Ⅱ.氯水以及氯的化合物经常用于饮用水的消毒。
(3)将铁片插入盛有少量新制氯水的试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为
(4)净水丸能对饮用水进行快速的杀菌消毒,药丸通常分内外两层。外层的优氯净Cl2Na(NCO)3先与水反应,生成次氯酸起杀菌消毒作用;几分钟后,内层的亚硫酸钠(Na2SO3)溶出,可将水中的余氯(次氯酸等)除去。
①优氯净中氯元素的化合价为
②亚硫酸钠将水中多余次氯酸除去的反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】完成下列问题
(1) 的键角大于
的键角大于 的键角,解释其原因:
的键角,解释其原因:_______ 。
(2)O、S的简单氢化物分子键角从大到小的顺序为_______ ,原因是_______ 。
(3) 中含有的化学键类型包括
中含有的化学键类型包括_______ ; 中
中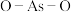 键角
键角_______ (填“>”或“<”) 中
中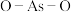 键角。
键角。
(4)配合物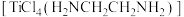 与游离的
与游离的 分子相比,其
分子相比,其 键角
键角_______ (填“较大”“较小”或“相同”),原因是_______ 。
(1)
 的键角大于
的键角大于 的键角,解释其原因:
的键角,解释其原因:(2)O、S的简单氢化物分子键角从大到小的顺序为
(3)
 中含有的化学键类型包括
中含有的化学键类型包括 中
中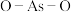 键角
键角 中
中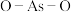 键角。
键角。(4)配合物
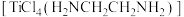 与游离的
与游离的 分子相比,其
分子相比,其 键角
键角
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】硫及其化合物广泛存在于自然界中,并被人们广泛利用。回答下列问题:
(1)当基态原子的电子吸收能量后,电子会发生___________ ,某处于激发态的S原子,其中1个3s电子跃迁到3p轨道中,该激发态S原子的核外电子排布式为___________ 。
(2)苯酚(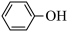 )中羟基被硫羟基取代生成苯硫酚(
)中羟基被硫羟基取代生成苯硫酚( ),苯硫酚的酸性比苯酚的酸性强,原因是
),苯硫酚的酸性比苯酚的酸性强,原因是___________ 。
(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH)。
①甲硫醇中C﹣S键与S﹣H键的键角___________ (填“小于”或“等于”)180°,甲硫醇分子中C原子杂化轨道类型是___________ ,S原子杂化轨道类型是___________ 。
②甲醇和甲硫醇的部分物理性质如下表:
甲醇和甲硫醇在水溶性方面性质差异的原因是___________ 。
(4)科学家通过X射线推测胆矾结构示意图:
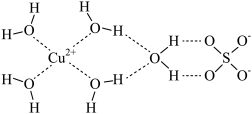
其中含有___________ 个配位键,___________ 个氢键。
(5)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]+xH+ ,交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.0015 mol [CrCl6(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+用浓度为0.1200 moI/LNaOH溶液25.00 mL,可知该配离子的化学式为___________ 。
(1)当基态原子的电子吸收能量后,电子会发生
(2)苯酚(
 )中羟基被硫羟基取代生成苯硫酚(
)中羟基被硫羟基取代生成苯硫酚( ),苯硫酚的酸性比苯酚的酸性强,原因是
),苯硫酚的酸性比苯酚的酸性强,原因是(3)甲醇(CH3OH)中的羟基被硫羟基取代生成甲硫醇(CH3SH)。
①甲硫醇中C﹣S键与S﹣H键的键角
②甲醇和甲硫醇的部分物理性质如下表:
| 物质 | 熔点/℃ | 沸点/℃ | 水溶液 |
| 甲醇 | ﹣97 | 64.7 | 互溶 |
| 甲硫醇 | ﹣123 | 6.8 | 不溶 |
(4)科学家通过X射线推测胆矾结构示意图:

其中含有
(5)在CrCl3的水溶液中,一定条件下存在组成为[CrCln(H2O)6-n]x+(n和x均为正整数)的配离子,将其通过氢离子交换树脂(R-H),可发生离子交换反应:[CrCln(H2O)6-n]x++xR-H→Rx[CrCln(H2O)6-n]+xH+ ,交换出来的H+经中和滴定,即可求出x和n,确定配离子的组成。将含0.0015 mol [CrCl6(H2O)6-n]x+的溶液,与R-H完全交换后,中和生成的H+用浓度为0.1200 moI/LNaOH溶液25.00 mL,可知该配离子的化学式为
您最近一年使用:0次
【推荐3】Fe、Cu都是重要的材料元素,其单质及化合物在诸多领域中都有广泛的应用。
(1)Fe位于元素周期表的___________ 区,基态 的价电子轨道表示式为
的价电子轨道表示式为___________ 。
(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用化学方程式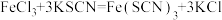 表示。经研究表明,
表示。经研究表明,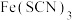 是配合物,
是配合物, 与
与 不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
① 与
与 的配合物中,主要是
的配合物中,主要是 与
与 以个数比1:1配合,所得离子显红色,则含该离子的配合物的化学式是
以个数比1:1配合,所得离子显红色,则含该离子的配合物的化学式是___________ 。
②铁的另一种配合物铁氰化钾 俗称赤血盐,可用于检验
俗称赤血盐,可用于检验 ,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理___________ ;该赤血盐配体的电子式为___________ 。
(1)Fe位于元素周期表的
 的价电子轨道表示式为
的价电子轨道表示式为(2)向黄色的三氯化铁溶液中加入无色的KSCN溶液,溶液变成红色。该反应在有的教材中用化学方程式
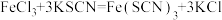 表示。经研究表明,
表示。经研究表明,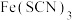 是配合物,
是配合物, 与
与 不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:
不仅能以1:3的个数比配合,还可以其他个数比配合。请按要求填空:①
 与
与 的配合物中,主要是
的配合物中,主要是 与
与 以个数比1:1配合,所得离子显红色,则含该离子的配合物的化学式是
以个数比1:1配合,所得离子显红色,则含该离子的配合物的化学式是②铁的另一种配合物铁氰化钾
 俗称赤血盐,可用于检验
俗称赤血盐,可用于检验 ,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
,两者反应生成带有特征蓝色的沉淀,请用离子方程式说明原理
您最近一年使用:0次

 中,
中, 的轨道杂化方式为
的轨道杂化方式为 分子中,
分子中, 原子的轨道杂化方式为
原子的轨道杂化方式为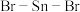 的键角
的键角 (填“
(填“ ”“
”“ ”或“
”或“ ”)。
”)。 )
) 二氧丙烷(
二氧丙烷( )
) )
)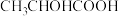 )
)

