如表所示为元素周期表的前四周期部分,根据图示结合所学知识回答下列问题:
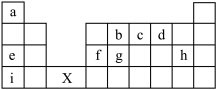
(1)h、i的简单离子半径由大到小的顺序为_______ (填离子符号)。
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是_______ (填化学式)。
(3)用电子式表示e和h形成离子化合物的过程:________ 。
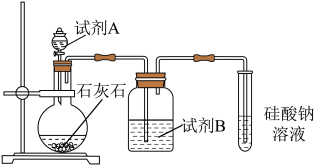
(4)非金属性:b_______ g(填“>”或“<”);以如图装置进行实验比较b、g对应的最高价氧化物对应水化物的酸性,则试剂A为_______ (填试剂名称),试剂B为_______ 。
(5)X处包含_______ 纵列,_______ 个族。
(6)i单质与d的简单氢化物反应的离子方程式为_______ 。

(1)h、i的简单离子半径由大到小的顺序为
(2)i、e、f的最高价氧化物对应的水化物的碱性由强到弱的顺序是
(3)用电子式表示e和h形成离子化合物的过程:
(4)非金属性:b

(5)X处包含
(6)i单质与d的简单氢化物反应的离子方程式为
更新时间:2024-04-04 00:43:15
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,参照元素A~I在表中的位置,用化学用语回答下列问题:
(1)D、E、H形成的简单离子的半径由大到小的顺序是____________________ 。
(2)E2D2的电子式为:______________ ,GD2形成晶体的类型为:___________________ 。
(3)将一定量HD2通入足量C的最高价氧化物的水化物稀溶液中,反应的离子方程式是______________ 。
(4)设计实验探究I、K两种元素非金属性的相对强弱。
可选用的试剂有:氯水、NaBr溶液、AgNO3溶液、CCl4。
请完成实验报告单:
 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 1 | A | |||||||
| 2 | B | C | D | |||||
| 3 | E | F | G | H | I | |||
| 4 | K | |||||||
(1)D、E、H形成的简单离子的半径由大到小的顺序是
(2)E2D2的电子式为:
(3)将一定量HD2通入足量C的最高价氧化物的水化物稀溶液中,反应的离子方程式是
(4)设计实验探究I、K两种元素非金属性的相对强弱。
可选用的试剂有:氯水、NaBr溶液、AgNO3溶液、CCl4。
请完成实验报告单:
| 实验内容 | 现象 |
| 步骤一:试管1:取少量氯水; 试管2:取少量NaBr溶液,滴加少量氯水。 | 试管2中的现象是: |
| 步骤二:分别向试管1、试管2中加少量 | 试管2中的现象是 |
| ①试管1的作用是 试管2中反应的离子方程式为: | |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下图是元素周期表的一部分,表中的①~⑩中元素,用元素符号或化学式填空回答:
(1)在这些元素中,化学性质最不活泼的原子的原子结构示意图为_______ 。
(2)地壳中含量最多的金属元素是____ ,写出元素⑥的简单气态氢化物的化学式______ 。
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是______ ,呈两性的氢氧化物是_______ 。
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是______ ,
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是______ 。
(6)元素⑦与元素⑩相比,非金属性较强的是____ ,能证明这一事实的依据是_____ 。
族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ⑥ | ① | ② | |||||
| 三 | ③ | ④ | ⑤ | ⑪ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
(2)地壳中含量最多的金属元素是
(3)这些元素中的最高价氧化物对应的水化物中,碱性最强的是
(4)写出②、③、⑤对应离子的离子半径由大到小的顺序是
(5)写出②、⑦、⑩对应阴离子还原性由强到弱的顺序是
(6)元素⑦与元素⑩相比,非金属性较强的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,表中所列的字母分别代表某一化学元素。
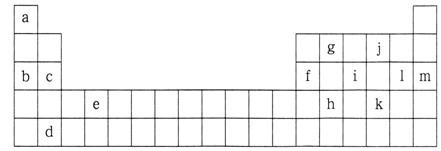
(1)表中所列元素中:
属于短周期元素的有__________ ;属于主族元素的有_________ ;e元素在元素周期表中的位置是________ 周期,_______ 族。
(2)下列___________ 组元素的单质可能都是电的良导体。
A.b,c,i B.a,g,k C.c,g,l D.d,e,f
(3)将元素a,b,c,f,1的原子半径按从小到大的顺序排列:________
(4) i元素属于_________ (填“金属”或“非金属”)元素,它的最高化合价是________ ,最低化合价是________ 。它能与氧气反应,生成一种吸水性很强的物质,这种物质在实验室里常用做干燥剂,写出i的单质与氧气反应的化学方程式:_____________

(1)表中所列元素中:
属于短周期元素的有
(2)下列
A.b,c,i B.a,g,k C.c,g,l D.d,e,f
(3)将元素a,b,c,f,1的原子半径按从小到大的顺序排列:
(4) i元素属于
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】元素是组成我们生活的世界中一切物质的“原材料”。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是___________ 。
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:
(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:
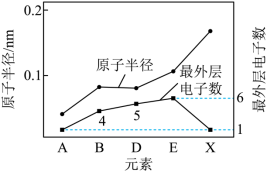
①E在周期表中的位置是___________ 。
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是___________ 。
③用电子式表示化合物XZ的形成过程是:___________ 。
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为___________ 。
⑤下列可以判断X和Y元素原子失电子能力强弱的是___________ (填字母序号)。
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:___________ 。
(1)砷(As)与N、P是同主族元素,远古时期人们就开始开发利用砷的性质,现代技术中砷仍然起着非常重要的作用。下列事实中,能说明As元素的非金属性弱于N元素的是
a.分解温度:AsH3<NH3 b.酸性:H3AsO4<HNO3
c.沸点:AsH3<NH3 d.相对分子质量:

(2)有A、B、D、E、X、Y、Z七种短周期元素。X与Y处于同一周期,Y的最高价氧化物对应的水化物与强酸、强碱均能反应。Z的单质常温下为气态,同条件下对于氢气的相对密度为35.5。其余元素的信息如图所示:

①E在周期表中的位置是
②A、D、Z三种元素所形成的化合物DA4Z中的化学键类型是
③用电子式表示化合物XZ的形成过程是:
④X的最高价氧化物对应水化物与Y的最高价氧化物对应水化物反应的离子方程式为
⑤下列可以判断X和Y元素原子失电子能力强弱的是
a.单质的熔点X比Y低
b.单质与水反应X比Y剧烈
c.单质与酸反应时,失电子数X比Y少
d.最高价氧化物的水化物的碱性X比Y强
⑥E和Z的最高价氧化物对应水化物的酸性前者弱于后者,利用原子结构解释产生差异的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】用“>”或“<”回答下列问题:
(1)酸性:H2CO3___________ H2SiO3,H2SiO3___________ H3PO4
(2)碱性:Ca(OH)2___________ Mg(OH)2,Mg(OH)2___________ Al(OH)3
(3)气态氢化物稳定性: H2O_______ H2S,H2S________ HCl。
(4)酸性:H2SO4_______ H2SO3,HClO4_______ HClO。
(5)还原性:H2O___________ H2S,H2S___________ HCl。
从以上答案中可以归纳出:
(6)元素的非金属性越强,其对应的最高价氧化物的水化物酸性越________ 。
(7)元素的金属性越强,其对应最高价氧化物水化物的碱性越_______ 。
(8)元素的_____ 性越强,其对应气态氢化物的稳定性越______ 。
(9)元素非金属性越强,其气态氢化物的还原性越_____ 。
(10)同种非金属元素形成的含氧酸,成酸元素价态越高,其酸性也越___________ 。
(1)酸性:H2CO3
(2)碱性:Ca(OH)2
(3)气态氢化物稳定性: H2O
(4)酸性:H2SO4
(5)还原性:H2O
从以上答案中可以归纳出:
(6)元素的非金属性越强,其对应的最高价氧化物的水化物酸性越
(7)元素的金属性越强,其对应最高价氧化物水化物的碱性越
(8)元素的
(9)元素非金属性越强,其气态氢化物的还原性越
(10)同种非金属元素形成的含氧酸,成酸元素价态越高,其酸性也越
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组设计如下实验探究KMnO4固体与草酸(H2C2O4)反应的产物,以其产物为原料制备氯气:室温下,取KMnO4固体于锥形瓶中,加入适量的草酸(H2C2O4)溶液,振荡,充分反应,可以观察到有黑色沉淀产生,溶液变为无色,同时生成无色无味的气体M,将燃着的木条靠近锥形瓶瓶口时木条熄灭。分析实验并回答相应问题。
(1)M的化学式是_____ ,组成草酸的三种元素中,非金属性最强的是_____ (填元素符号)。
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为_____ ,向滤液中加入盐酸时又产生无色无味气体,该反应的离子方程式为______ 。
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是_____ 。
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为_____ 。
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:______ 。
(1)M的化学式是
(2)将充分反应后的混合物过滤,检验滤液中金属阳离子的方法及现象为
(3)将过滤得到的滤渣洗涤干净,确认滤渣已洗涤干净的操作是
(4)将滤渣加入浓盐酸中加热,产生黄绿色气体,该反应的离子方程式为
(5)写出高锰酸钾与草酸溶液发生反应的化学方程式,并用单线桥法表示反应中电子的转移情况:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下表为元素周期表的一部分,请根据元素①~⑧所处的位置回答下列问题:
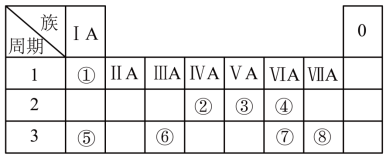
(1)元素④⑤⑧的离子半径由大到小的顺序为_______ (用离子符号表示)。
(2)元素④⑦的最简单氢化物的稳定性关系为_______ (用化学式表示)。
(3)由元素⑧和⑥组成的化合物是_______ (填“离子化合物”或“共价化合物”),可以证明你的判断正确的实验依据是_______ 。
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是_______ (填化学式),该酸与元素⑥的最高价氧化物对应的水化物反应的离子方程式是_______ 。
(5)由元素①③组成的含 的分子的电子式是
的分子的电子式是_______ 。

(1)元素④⑤⑧的离子半径由大到小的顺序为
(2)元素④⑦的最简单氢化物的稳定性关系为
(3)由元素⑧和⑥组成的化合物是
(4)元素②⑦⑧的最高价含氧酸的酸性最强的是
(5)由元素①③组成的含
 的分子的电子式是
的分子的电子式是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】下表是元素周期表的一部分,请用规范的化学用语回答有关问题:
(1)元素⑨在周期表中所处位置 ___________ 。
(2)表中化学性质最不活泼的元素,其原子结构示意图为___________ 。
(3)④⑦⑨元素形成的化合物中含有的化学键类型为___________ 。
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为___________ 。(填离子符号)
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是___________ 。
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式___________ 。
(7)②、③、④的简单氢化物中最稳定的是___________ ;写出⑧的最高价氧化物与⑥的最高价氧化物对应水化物反应的离子方程式___________ 。
(8)用电子式表示⑥与⑨形成的化合物的形成过程___________ 。
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 二 | ① | ② | ③ | ④ | ⑤ | |||
| 三 | ⑥ | ⑦ | ⑧ | ⑨ |
(2)表中化学性质最不活泼的元素,其原子结构示意图为
(3)④⑦⑨元素形成的化合物中含有的化学键类型为
(4)④、⑧、⑨三种元素的常见离子的半径由小到大的顺序为
(5)①、⑥、⑦三种元素的最高价氧化物的水化物中碱性最强的是
(6)写出⑥、⑧元素的最高价氧化物的水化物发生反应的离子方程式
(7)②、③、④的简单氢化物中最稳定的是
(8)用电子式表示⑥与⑨形成的化合物的形成过程
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】现有表格中短周期元素的数据(已知Be的原子半径为0.089nm):
(1)⑧号元素在元素周期表中的位置是。_______ 。
(2)①④⑦元素的简单气态氢化物中,热稳性定由高到低排序_______ (写化学式)。
(3)结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱_______ 。
(4)含锂材料在社会中应用广泛,如各种储氢材料Li2NH等)、便携式电源材料(LiCoO2等),根据下列要求回答问题:
①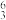 Li和
Li和 Li可作核反应堆最佳热载体,
Li可作核反应堆最佳热载体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法正确的是
LiD用作高温堆减速剂。下列说法正确的是_______ (填字母,下同)。
A.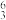 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.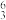 Li和
Li和 Li属于同种核素
Li属于同种核素
C. LiH和
LiH和 LiD中质子总数相同 D.
LiD中质子总数相同 D. LiH和
LiH和 LiD中电子总数相同
LiD中电子总数相同
②实验室中钠为避免接触空气保存在_______ 中;锂电池使用时需要注意防水,其原因用离子反应方程式表示为_______ 。
③下列说法不正确的是_______ 。
A.碱性:Be(OH)2<LiOH<NaOH<KOH
B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+
D.金属性:Cs>Rb>K>Na>Li>Be
| ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |
| 原子半径(nm) | 0.074 | 0.160 | 0.152 | 0.110 | 0.099 | 0.186 | 0.075 | 0.082 |
| 最高正价 | +2 | +1 | +5 | +7 | +1 | +5 | +3 | |
| 最低负价 | -2 | -3 | -1 | -3 |
(2)①④⑦元素的简单气态氢化物中,热稳性定由高到低排序
(3)结合原子结构解释③⑥元素的最高价氧化物对应的水化物的碱性强弱
(4)含锂材料在社会中应用广泛,如各种储氢材料Li2NH等)、便携式电源材料(LiCoO2等),根据下列要求回答问题:
①
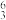 Li和
Li和 Li可作核反应堆最佳热载体,
Li可作核反应堆最佳热载体, LiH和
LiH和 LiD用作高温堆减速剂。下列说法正确的是
LiD用作高温堆减速剂。下列说法正确的是A.
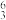 Li和
Li和 Li互为同位素 B.
Li互为同位素 B.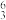 Li和
Li和 Li属于同种核素
Li属于同种核素C.
 LiH和
LiH和 LiD中质子总数相同 D.
LiD中质子总数相同 D. LiH和
LiH和 LiD中电子总数相同
LiD中电子总数相同②实验室中钠为避免接触空气保存在
③下列说法不正确的是
A.碱性:Be(OH)2<LiOH<NaOH<KOH
B.半径:K>Na>Li>Li+
C.氧化性:Li+<Na+<K+<Rb+<Cs+
D.金属性:Cs>Rb>K>Na>Li>Be
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】根据所学知识,回答下列问题:
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:___________ 。
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为___________ 。
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是___________ 。
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为___________ 。
(5)含有10个电子,9个质子的微粒___________ 。(至少2个)
(6)用电子式表示MgCl2的形成过程___________ 。
(7)配平___________
Mn2++PbO2+H+→MnO +Pb2++H2O
+Pb2++H2O
(1)自来水厂用氯气杀菌、消毒,其消毒原理主要是氯气溶于水后生成了HClO,写出HClO的电子式:
(2)6.0g氮的氧化物NOx中,含N物质的量为0.2mol,则NOx的摩尔质量为
(3)已知反应:3Cu+8HNO3(稀)=3Cu(NO3)2+2NO↑+4H2O。若有64gCu被氧化,则被还原的HNO3的物质的量是
(4)ClO2是一种黄绿色气体,被称为“第四代”饮用水消毒剂。制备ClO2的一种方法为在平底烧瓶中加入KClO3固体、足量草酸(H2C2O4)、稀硫酸,60℃~80℃水浴加热。该反应的化学方程式为
(5)含有10个电子,9个质子的微粒
(6)用电子式表示MgCl2的形成过程
(7)配平
Mn2++PbO2+H+→MnO
 +Pb2++H2O
+Pb2++H2O
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】下表列出了①~⑩十种元素在周期表中的位置:
请按要求回答下列问题:
(1)上述元素中,金属性最强的是___________ (填元素名称),最高价氧化物对应水化物酸性最强的是___________ (写出酸的化学式)。
(2)由元素③形成的单质的电子式为___________ ,由元素⑥和⑨形成化合物乙,请用电子式表示物质乙的形成过程___________ 。
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为___________ 。
(4)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| 族周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
| 4 | ⑩ | |||||||
(1)上述元素中,金属性最强的是
(2)由元素③形成的单质的电子式为
(3)由元素①、③、④、⑧形成的一种离子化合物,其水溶液显强酸性,该化合物的化学式为
(4)可以比较⑤、⑥两元素金属性强弱的实验是___________。
| A.比较这两种元素最高价氧化物对应的水化物的碱性 |
| B.将⑤的单质投入到⑥的盐溶液中 |
| C.将这两种元素的单质分别放入冷水中 |
| D.比较这两种元素的单质与酸反应时失电子的数目 |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】钠元素在自然界中以多种化合物的形式存在。NaCl、 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。
Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是___________ ,可治疗胃酸过多的是___________ 。
(2)查阅资料知: 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有___________ (填“氧化性”或“还原性”)
Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
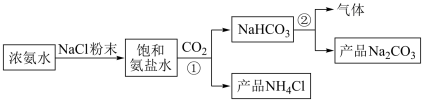
回答下列问题:
(3)产品 可用作氮肥,
可用作氮肥, 属于
属于___________ (填“离子”或“共价”)化合物。
(4)下图装置A和装置B均可用于实验室制备 ,其中装置A的优点是
,其中装置A的优点是___________ , 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为___________ 。

(5)向饱和氨盐水中通入 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是___________ 。
(6)步骤②生成 的化学方程式为
的化学方程式为___________ ,热稳定性
___________ (填“>”或“<”) 。
。
(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,___________ 。
 、
、 、
、 是重要的化工原料,具有多种用途。
是重要的化工原料,具有多种用途。Ⅰ.完成下列问题
(1)以上物质可在呼吸面具和潜水艇中作为氧气的来源的是
(2)查阅资料知:
 在一定条件下可以转化为
在一定条件下可以转化为 ,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食
,亚硝酸钠外观酷似食盐且有咸味,是一种常用的发色剂和防腐剂。误食 会导致血红蛋白中的
会导致血红蛋白中的 转化为
转化为 而中毒,误食
而中毒,误食 后可服用维生素C解毒,表明维生素C具有
后可服用维生素C解毒,表明维生素C具有Ⅱ.化工专家侯德榜发明的侯氏制碱法为我国经济发展做出了重要贡献。某化学兴趣小组在实验室中模拟并改进侯氏制碱法制备
 ,进一步处理得到产品
,进一步处理得到产品 和,实验流程如图:
和,实验流程如图:
回答下列问题:
(3)产品
 可用作氮肥,
可用作氮肥, 属于
属于(4)下图装置A和装置B均可用于实验室制备
 ,其中装置A的优点是
,其中装置A的优点是 和盐酸反应的离子方程式为
和盐酸反应的离子方程式为
(5)向饱和氨盐水中通入
 会产生
会产生 沉淀,从溶液中分离出
沉淀,从溶液中分离出 沉淀的操作名称是
沉淀的操作名称是(6)步骤②生成
 的化学方程式为
的化学方程式为
 。
。(7)该方法制得的纯碱中往往会含有NaCl杂质,为检验杂质的存在,简单的检验方案是:取少量试样溶于水后,
您最近一年使用:0次



