高铁酸钾(K2FeO4)是一种既能杀菌、消毒、又能絮凝净水的水处理剂。工业制备高铁酸钾的反应离子方程式为:2Fe(OH)3 + 3ClO- + 4OH- = 2 + 3Cl- + 2H2O。下列有关说法不正确的是
+ 3Cl- + 2H2O。下列有关说法不正确的是
A.由上述反应可知,C1O- 的氧化性强于FeO |
| B.高铁酸钾中铁显+6价 |
| C.上述反应中氧化剂和还原剂的物质的量之比为2:3 |
| D.K2FeO4处理水时,不仅能消毒杀菌,而且生成的Fe3+水解形成Fe(OH)3胶体能吸附水中的悬浮杂质 |
更新时间:2024-03-29 23:25:33
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】纳米级 (颗粒大小为1-100nm)是一种重要的水光解催化剂,可利用肼(
(颗粒大小为1-100nm)是一种重要的水光解催化剂,可利用肼( )与新制
)与新制 反应制备,方程式为:
反应制备,方程式为: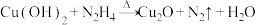 (未配平),下列有关说法中正确的是
(未配平),下列有关说法中正确的是
 (颗粒大小为1-100nm)是一种重要的水光解催化剂,可利用肼(
(颗粒大小为1-100nm)是一种重要的水光解催化剂,可利用肼( )与新制
)与新制 反应制备,方程式为:
反应制备,方程式为: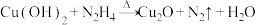 (未配平),下列有关说法中正确的是
(未配平),下列有关说法中正确的是A.纳米级 颗粒属于胶体 颗粒属于胶体 |
B.肼的电子式为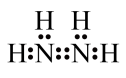 |
| C.理论上参与反应的n(氧化剂):n(还原剂)=1:4 |
D.在适宜条件下,利用葡萄糖代替 也可制得纳米级 也可制得纳米级 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】化学与生产生活及科技密切相关,下列相关说法正确的是
| A.豆浆中的蛋白质可在CuSO4的作用下聚沉而形成美味的豆腐 |
| B.碳纳米管可以看成由石墨片层卷成的,属于胶体 |
| C.糯米烧麦、白灼西兰花均含有天然高分子化合物 |
| D.现代建筑物大量使用的沙子和水泥都是硅酸盐材料 |
您最近一年使用:0次
【推荐1】用还原法可以将硝酸厂烟气中的大量氮氧化物( )转化为无害物质。常温下,将NO与
)转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法不正确的是
的混合溶液中,其转化过程如图所示。下列说法不正确的是

 )转化为无害物质。常温下,将NO与
)转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入 与
与 的混合溶液中,其转化过程如图所示。下列说法不正确的是
的混合溶液中,其转化过程如图所示。下列说法不正确的是
A.转化过程的总反应方程式为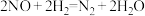 |
| B.反应Ⅰ中氧化剂与还原剂的个数之比为2:1 |
C.转化反应前后混合溶液内 和 和 的总数保持不变 的总数保持不变 |
| D.反应Ⅰ、Ⅱ中含Ce的物质均作氧化剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】设 为阿伏加德罗常数的值。硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是
为阿伏加德罗常数的值。硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是 。下列说法中错误的是
。下列说法中错误的是
 为阿伏加德罗常数的值。硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是
为阿伏加德罗常数的值。硫化钠广泛应用于冶金染料、皮革、电镀等工业。硫化钠的一种制备方法是 。下列说法中错误的是
。下列说法中错误的是A.反应过程中可能产生 气体 气体 |
B. 溶液中所含阴离子的数目小于 溶液中所含阴离子的数目小于 |
C.该反应生成 氧化产物,转移电子数目为 氧化产物,转移电子数目为 |
D.常温、常压下,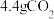 中共用电子对数目为 中共用电子对数目为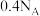 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 将浓硫酸滴入乙醇中,加热至 ,生成的气体通入酸性高锰酸钾溶液 ,生成的气体通入酸性高锰酸钾溶液 | 验证乙烯具有还原性 |
| B | 向0.1 H2O2溶液中滴加0.1 H2O2溶液中滴加0.1 KMnO4溶液,观察溶液颜色变化 KMnO4溶液,观察溶液颜色变化 | 探究H2O2具有氧化性 |
| C | 向某溶液中加入氢氧化钠溶液并加热,观察产生的气体能否使蓝色石蕊试纸变色 | 溶液中是否存在NH |
| D | 向 溶液中同时通入 溶液中同时通入 和 和 | 比较 和 和 的氧化能力 的氧化能力 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知反应:KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,据此判断下列说法正确的是
| A.反应生成物都属于电解质 | B.该反应表明氧化性Cl2比KClO3强 |
| C.HCl部分发生氧化反应 | D.1molKClO3在反应中得到6mole- |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列对氧化还原反应的认识正确的是( )
| A.具有氧化性的物质在化学反应中一定作氧化剂 |
| B.氧化还原反应的本质是化合价发生变化 |
| C.还原剂具有还原性,在反应中被还原,得到还原产物 |
| D.置换反应一定是氧化还原反应,复分解反应一定不属于氧化还原反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】某工厂采用废弃矿渣(主要含FeO、Cr2O3)制备Cr(OH)3,涉及工艺流程如图。测知在制备过程中Cr元素化合价发生了变化,下列说法错误的是
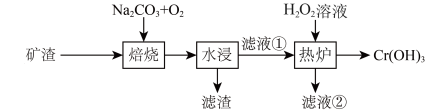
| A.该制备过程中主要涉及到三个氧化还原反应 | B.滤液①主要溶质是铬酸钠 |
| C.H2O2在热炉反应中作还原剂 | D.在焙烧和热炉两个环节电子转移数是相等的 |
您最近一年使用:0次

 胶体的制备实验示意图,相关表述不合理的是
胶体的制备实验示意图,相关表述不合理的是
 溶液
溶液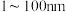 范围
范围 (胶体)
(胶体) 的混合溶液作吸收剂可吸收工厂排放的含
的混合溶液作吸收剂可吸收工厂排放的含 的废气,从而减少空气污染并回收
的废气,从而减少空气污染并回收 ,其过程如图所示(各步均进行完全)。下列叙述不正确的是
,其过程如图所示(各步均进行完全)。下列叙述不正确的是
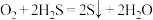
 、
、
 时,理论上需要消耗标准状况
时,理论上需要消耗标准状况
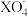 =2X2++5Z2+8H2O②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-根据上述反应,判断下列结论中错误的是
=2X2++5Z2+8H2O②2A2++B2=2A3++2B- ③2B-+Z2=B2+2Z-根据上述反应,判断下列结论中错误的是

