X、Y、Z、W、M、R、T七种短周期元素,周期表中位置如图:
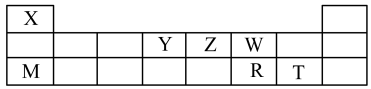
试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是______ (用元素符号表示)。
(2)W的简单氢化物的电子式为_______ 。
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为______ 。
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是______ (用化学式表示)。
(5)M和R最高价氧化物对应水化物反应的离子方程式为______ 。

试回答下列问题:
(1)X、Z、W三种元素的原子半径由大到小的排列顺序是
(2)W的简单氢化物的电子式为
(3)由X、Z、W三种元素可组成一种强酸,该强酸的稀溶液能与铜反应,则该反应的化学方程式为
(4)R、T两种元素简单氢化物的稳定性由强到弱的的顺序是
(5)M和R最高价氧化物对应水化物反应的离子方程式为
更新时间:2024-04-03 18:42:15
|
相似题推荐
填空题
|
较易
(0.85)
解题方法
【推荐1】在浓硝酸中放入铜片:
(1)反应开始时的化学方程式为________________ ,实验现象为_______________ 。
(2)若铜有剩余,则反应将要结束时的化学方程式为__________________________ 。
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是______ 。
(1)反应开始时的化学方程式为
(2)若铜有剩余,则反应将要结束时的化学方程式为
(3)待反应停止后,再加入少量25%的稀硫酸,这时铜片上又有气泡产生,其原因是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】请回答:
(1)CO2的电子式是______ ;福尔马林的溶质是______ (用结构式表示)。
(2)向FeSO4溶液中滴加NaOH溶液,可观察到的现象是_______ 。
(3)铜和稀硝酸反应的离子方程式:_______ 。
(1)CO2的电子式是
(2)向FeSO4溶液中滴加NaOH溶液,可观察到的现象是
(3)铜和稀硝酸反应的离子方程式:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】根据元素周期表中短周期的下列内容回答问题:
(1)元素①~⑨形成的单质中,化学性质最稳定的是_____ (填化学式)。④在元素周期表中的位置是________ ,⑥的简单离子的结构示意图为________________
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为________________ ,⑤、⑧按原子个数比2:1形成的化合物的电子式为________________
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:________________
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为________________
| H | ① | ||||||
| ② | ③ | O | ④ | ||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(1)元素①~⑨形成的单质中,化学性质最稳定的是
(2)③、⑨和H元素可形成一种常见的盐,其中存在的化学键类型为
(3)写出一个可证明②和⑦非金属性强弱的离子方程式:
(4)在酸性溶液中,②的简单氢化物与O2组成燃料电池,其负极的电极反应式为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】下表是元素周期表的一部分,回答下列有关问题:
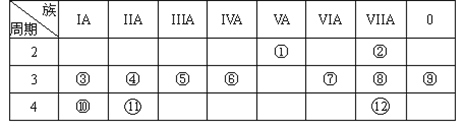
(1)写出元素符号:⑨________ (填化学式,下同)
(2)在这些元素中,最活泼的金属元素是________ 。
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是________ ,呈两性的氢氧化物是________ 。

(1)写出元素符号:⑨
(2)在这些元素中,最活泼的金属元素是
(3)在这些元素的最高价氧化物对应水化物中,酸性最强的是
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐1】磷酸铁锂(LiFePO4)电极材料主要用于各种锂离子电池。回答下列问题。
(1)Fe位于元素周期表中第______ 周期第______ 族,其价层电子排布式为______ 。
(2) 用“>”“<”或“=”填空:
离子半径:Li+______ H-;第一电离能:Li ______ Be;电负性:O ______ P。
(3)在周期表中,化学性质相似的邻族元素是______ 。
(4)下列Li原子轨道表示式表示的状态中,能量最低和最高的分别为______ 、______ (填字母)。
A.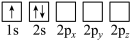 B.
B.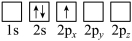
C. D.
D.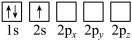
(5)基态P原子中未成对电子数为______ ,其原子核外电子占据的最高能级的电子云轮廓图为______ 形。
(1)Fe位于元素周期表中第
(2) 用“>”“<”或“=”填空:
离子半径:Li+
(3)在周期表中,化学性质相似的邻族元素是
(4)下列Li原子轨道表示式表示的状态中,能量最低和最高的分别为
A.
 B.
B.
C.
 D.
D.
(5)基态P原子中未成对电子数为
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐2】在下列原子(或离子)结构简图上表示的微粒中(用元素符号填空)
A. B.
B.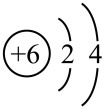 C.
C.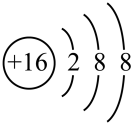 D.
D.
(1)半径最小的是_______ ;
(2)A、C 形成化合物的电子式_______ ;
(3)只有还原性的是_______ ;
(4)只有氧化性的是_______ ;
(5)得失电子能力均最弱的是_______ 。
A.
 B.
B. C.
C. D.
D.
(1)半径最小的是
(2)A、C 形成化合物的电子式
(3)只有还原性的是
(4)只有氧化性的是
(5)得失电子能力均最弱的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】5种元素原子的电子排布式如下:
A.1s22s22p63s23p63d54s2 B.1s22s22p63s2 C.1s22s22p6 D.1s22s22p63s23p2 E.[Ar]4s1
(1)属于稀有气体_______ ,元素符号是_______ 。
(2)A的元素符号是_______ ,写出A原子的简化电子排布式:_______ 。
(3)B、D、E三种元素的原子半径大小顺序是_______ (用元素符号表示)。
A.1s22s22p63s23p63d54s2 B.1s22s22p63s2 C.1s22s22p6 D.1s22s22p63s23p2 E.[Ar]4s1
(1)属于稀有气体
(2)A的元素符号是
(3)B、D、E三种元素的原子半径大小顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐1】在玻璃生产中,熔炉里原料发生的主要反应为:2Na2CO3+CaCO3+3SiO2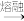 2Na2SiO3+CaSiO3+CO2↑
2Na2SiO3+CaSiO3+CO2↑
(1)某反应物在熔融状态下不导电,它属于___ 晶体。
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为___ 。
(3)碳和硅属于同族元素,该族元素的原子最外层轨道表示式为___ 。
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:___ 。
(5)CO2的电子式为___ 。
(6)反应物Na2CO3和CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由:___ 。
 2Na2SiO3+CaSiO3+CO2↑
2Na2SiO3+CaSiO3+CO2↑(1)某反应物在熔融状态下不导电,它属于
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为
(3)碳和硅属于同族元素,该族元素的原子最外层轨道表示式为
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:
(5)CO2的电子式为
(6)反应物Na2CO3和CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由:
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐2】硫原子的最外层电子排布式为___________ ,其原子核外有___________ 种不同能量的电子。在周期表中,与硫相邻的短周期元素原子半径由大到小的顺序是___________ 。
您最近一年使用:0次
填空题
|
较易
(0.85)
【推荐3】下表是元素周期表的一部分,针对表中的①~⑧元素,填写下列空白:
(1)①的气态氢化物分子的空间构型为_________________________ 。
(2)②的气态氢化物稳定性比⑦的气态氢化物__________ (填“强”、“弱”或“相同”)。
(3)由①与②形成的三原子分子的电子式为_______________________________ 。
由③与⑧形成的离子化合物的电子式为____________________________________ 。
(4)③、④、⑤离子半径依次__________________ 。(填“增大”、“减小”或“不变”)
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
_____________________________________________________________________ 。
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | ||
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ |
(1)①的气态氢化物分子的空间构型为
(2)②的气态氢化物稳定性比⑦的气态氢化物
(3)由①与②形成的三原子分子的电子式为
由③与⑧形成的离子化合物的电子式为
(4)③、④、⑤离子半径依次
(5)⑤的最高价氧化物对应水化物与③的最高价氧化物对应水化物反应离子方程式为:
您最近一年使用:0次



