在玻璃生产中,熔炉里原料发生的主要反应为:2Na2CO3+CaCO3+3SiO2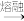 2Na2SiO3+CaSiO3+CO2↑
2Na2SiO3+CaSiO3+CO2↑
(1)某反应物在熔融状态下不导电,它属于___ 晶体。
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为___ 。
(3)碳和硅属于同族元素,该族元素的原子最外层轨道表示式为___ 。
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:___ 。
(5)CO2的电子式为___ 。
(6)反应物Na2CO3和CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由:___ 。
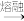 2Na2SiO3+CaSiO3+CO2↑
2Na2SiO3+CaSiO3+CO2↑(1)某反应物在熔融状态下不导电,它属于
(2)上述反应里所涉及的短周期元素原子半径由大到小的顺序为
(3)碳和硅属于同族元素,该族元素的原子最外层轨道表示式为
(4)写一个能比较碳元素和氧元素非金属性强弱的化学反应方程式:
(5)CO2的电子式为
(6)反应物Na2CO3和CaCO3均能制备二氧化碳,但是往往不是都能使用稀硫酸,请说明理由:
更新时间:2020-03-25 11:43:38
|
相似题推荐
填空题
|
较易
(0.85)
名校
【推荐2】下表为元素周期表的前三周期。
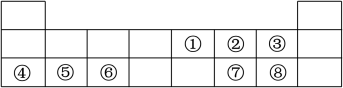
回答下列问题:
(1)写出元素符号⑤_______ ,⑦_______ 。
(2)表中所列元素中,金属性最强的元素是_______ (填元素符号,下同),非金属性最强的元素是_____ ;最高价氧化物对应水化物中,酸性最强的是________ (填化学式)。
(3)①、②、③三种元素的原子半径最大的是_________ (填元素符号);④号元素与⑧号元素形成化合物的电子式为________ 。

回答下列问题:
(1)写出元素符号⑤
(2)表中所列元素中,金属性最强的元素是
(3)①、②、③三种元素的原子半径最大的是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】如图是元素周期表的一部分。回答下列问题:
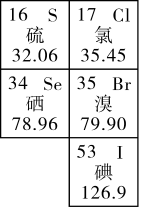
(1)溴被称为海洋元素。
①溴在元素周期表中位于第_______ 周期_______ 族。
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是_______ (填化学式)。
③能够证明溴单质的氧化性强于碘单质的离子方程式是_______ 。
(2)硒是人体必需的微量元素。
①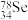 与
与 互称为
互称为_______ 。
② 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成硒单质和
气体发生反应,生成硒单质和 。写出
。写出 与
与 的反应方程式:
的反应方程式:_______ 。
(3)根据图下列说法正确的是_______ (填字母)。
a.原子半径r:r(Se)>r(Br)
b.Se元素的非金属性比Br的强
c.气态氢化物稳定性:H2Se>HBr

(1)溴被称为海洋元素。
①溴在元素周期表中位于第
②表中与溴同主族的元素中,最高价氧化物对应的水化物酸性最强的酸是
③能够证明溴单质的氧化性强于碘单质的离子方程式是
(2)硒是人体必需的微量元素。
①
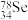 与
与 互称为
互称为②
 溶于水生成
溶于水生成 ,向所得溶液中通入
,向所得溶液中通入 气体发生反应,生成硒单质和
气体发生反应,生成硒单质和 。写出
。写出 与
与 的反应方程式:
的反应方程式:(3)根据图下列说法正确的是
a.原子半径r:r(Se)>r(Br)
b.Se元素的非金属性比Br的强
c.气态氢化物稳定性:H2Se>HBr
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】从宏观和微观两个角度认识元素的单质及其化合物是学好中学化学的重要基础。
(1)组成 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为___________ 。
(2) 、
、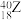 、
、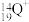 、
、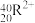 、
、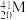 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有___________ 种
(3)下列各组物质中,含有化学键类型都相同的是___________。
(4)将HCl和NaCl分别溶于水。下列说法正确的是___________。
(5)能用于比较Cl与S非金属性强弱的依据是___________。
(1)组成
 的三种元素,其对应的简单离子半径由小到大的顺序为
的三种元素,其对应的简单离子半径由小到大的顺序为(2)
 、
、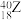 、
、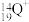 、
、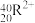 、
、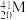 5种微粒,所属元素的种类有
5种微粒,所属元素的种类有(3)下列各组物质中,含有化学键类型都相同的是___________。
| A.HI和NaCl | B.NaF和KOH | C.CO和HCl | D. 和NaBr 和NaBr |
| A.HCl的离子键被破坏 | B.NaCl的共价键被破坏 |
| C.HCl和NaCl的化学键均遭破坏 | D.HCl和NaCl的化学键均未遭破坏 |
| A.熔沸点:硫单质>氯单质 | B.酸性: |
C.热稳定性: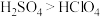 | D.氧化性: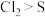 |
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】 俗称小苏打,常用于面包的发酵。回答下列问题。
俗称小苏打,常用于面包的发酵。回答下列问题。
(1)H 元素位于元素周期表的第_______ 周期第 IA 族。
(2)Na 元素位于第IA族H元素下方,Na的原子半径比H的_______ (填“大”或“小”)。
(3) 所含的三种非金属元素中,非金属性较强的是
所含的三种非金属元素中,非金属性较强的是_______ (填“ H ”或“O”或“C”)。
(4)Na 的最高价氧化物的化学式为_______ 。
 俗称小苏打,常用于面包的发酵。回答下列问题。
俗称小苏打,常用于面包的发酵。回答下列问题。(1)H 元素位于元素周期表的第
(2)Na 元素位于第IA族H元素下方,Na的原子半径比H的
(3)
 所含的三种非金属元素中,非金属性较强的是
所含的三种非金属元素中,非金属性较强的是(4)Na 的最高价氧化物的化学式为
您最近一年使用:0次
填空题
|
较易
(0.85)
名校
【推荐3】按要求填空:
(1)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子半径由大到小的顺序是__________________ 。
(2)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:___________ ,____________ 。
(3)已知: N2(g)+
N2(g)+ H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
N(g)+3H(g)=NH3(g)ΔH2=-bkJ·mol-1
NH3(g)=NH3(l)ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式____________________________ 。
(4)下列原子: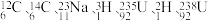 中共有
中共有____ 种元素,_____ 种核素。
(1)已知X+、Y2+、Zˉ、W2ˉ四种离子均具有相同的电子层结构,则X、Y、Z、W这四种元素的原子半径由大到小的顺序是
(2)A+、Bˉ、C、D四种粒子(分子或离子),它们都分别含10个电子,已知它们有如下转化关系:A++Bˉ
 C+D↑,则A+、Bˉ的电子式:
C+D↑,则A+、Bˉ的电子式:(3)已知:
 N2(g)+
N2(g)+ H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1
H2(g)=N(g)+3H(g)ΔH1=+akJ·mol-1N(g)+3H(g)=NH3(g)ΔH2=-bkJ·mol-1
NH3(g)=NH3(l)ΔH3=-ckJ·mol-1
写出N2(g)和H2(g)反应生成液氨的热化学方程式
(4)下列原子:
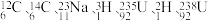 中共有
中共有
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】原子序数依次增大的四种元素A、B、C、D分别处于第一至第四周期.自然界存在多种A的化合物,B原子核外电子有6种不同的运动状态,B与C可形成正四面体形的分子,D的基态原子的最外能层只有一个电子,其他能层均已充满电子.请回答下列问题:
⑴这四种元素中电负性最大的元素的基态原子的价电子排布图为______ .
⑵由A与B两种元素形成的化合物中,其中B原子采用sp杂化的最简单化合物分子中,含有的δ键、π键数目之比为______ .
⑶D元素的常见离子的水溶液显色的原因是______ ,此离子中存在的化学键有______ (a.离子键 b.共价键c.配位键d.氢键e.范德华力f.金属键
⑴这四种元素中电负性最大的元素的基态原子的价电子排布图为
⑵由A与B两种元素形成的化合物中,其中B原子采用sp杂化的最简单化合物分子中,含有的δ键、π键数目之比为
⑶D元素的常见离子的水溶液显色的原因是

您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】回答下列问题:
(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,原因:____ 。
(2)乙炔分子中σ键与π键的个数比为____ 。
(3)乳酸CH3-CH(OH)-COOH____ (填“有”或“无”)手性分子。
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,该元素核外价电子 排布图____ 。
(5)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:____ 、____ 、____ 。
(6)SiO2的晶体类型:____ ,在加热融化时克服____ (填作用力名称)。
(1)H2O的沸点(100℃)比H2S的沸点(-61℃)高,原因:
(2)乙炔分子中σ键与π键的个数比为
(3)乳酸CH3-CH(OH)-COOH
(4)某元素原子共有3个价电子,其中一个价电子位于第三能层d轨道,该元素核外
(5)指出配合物K3[Co(CN)6]中的中心离子、配体及其配位数:
(6)SiO2的晶体类型:
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐1】二氧化硅晶体
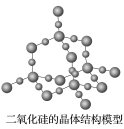
(1)二氧化硅晶体中,每个硅原子均以4个_____________ 对称地与相邻的_____________ 个氧原子相结合,每个氧原子与_____________ 个硅原子相结合,向空间扩展,形成三维骨架结构。晶体结构中最小的环上有_____________ 个硅原子和_____________ 个氧原子,硅、氧原子个数比为_____________ 。
(2)低温石英的结构中有顶角相连的_____________ 形成螺旋上升的长链,而没有封闭的_____________ 。这一结构决定了它具有_____________ 。

(1)二氧化硅晶体中,每个硅原子均以4个
(2)低温石英的结构中有顶角相连的
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐2】如图表示一些晶体中的某些结构,它们分别是NaCl、CsCl、干冰、金刚石、石墨结构中的某一种的某一部分。

(1)代表金刚石的是___ (填编号字母,下同),其中每个碳原子与___ 个碳原子最接近且距离相等。金刚石属于___ 晶体。
(2)代表石墨的是___ ,其中每个正六边形占有的碳原子数平均为___ 个。
(3)代表NaCl的是___ ,每个Na+周围与它最接近且距离相等的Na+有___ 个。
(4)代表CsCl的是___ ,它属于___ 晶体,每个Cs+与___ 个Cl-紧邻。
(5)代表干冰的是___ ,它属于___ 晶体,每个CO2分子与___ 个CO2分子紧邻。
(6)若说“离子晶体中只有离子键,分子晶体中没有化学键”是否正确,简述理由:___ 。
(7)NaCl晶体、HCl晶体、干冰、金刚石的熔点由高到低的顺序是___ ;其中在熔融或液态时能导电的电解质是___ ,液态不导电但为电解质的是___ ,在水溶液中能导电的非电解质是___ 。


(1)代表金刚石的是
(2)代表石墨的是
(3)代表NaCl的是
(4)代表CsCl的是
(5)代表干冰的是
(6)若说“离子晶体中只有离子键,分子晶体中没有化学键”是否正确,简述理由:
(7)NaCl晶体、HCl晶体、干冰、金刚石的熔点由高到低的顺序是
您最近一年使用:0次
填空题
|
较易
(0.85)
解题方法
【推荐3】⑴如图为碳的一种同素异形体C60分子,每个C60分子中含有σ键的数目为___________ ;

⑵如图为碳的另一种同素异形体——金刚石的晶胞结构,D与周围4个原子形成的空间结构是_______ ,所有键角均为_______ 。

⑶硼酸(H3BO3)的结构与石墨相似如图所示,层内的分子以氢键相连,含1 mol硼酸的晶体中有_____ mol氢键。

⑷每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有____ 个,每个Na+周围等距且紧邻的Na+有_____ 个。


⑵如图为碳的另一种同素异形体——金刚石的晶胞结构,D与周围4个原子形成的空间结构是

⑶硼酸(H3BO3)的结构与石墨相似如图所示,层内的分子以氢键相连,含1 mol硼酸的晶体中有

⑷每个Na+(Cl-)周围等距且紧邻的Cl-(Na+)有

您最近一年使用:0次

 是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。
是一种常见的催化剂,在氯酸钾分解、双氧水分解的反应中作催化作用。

