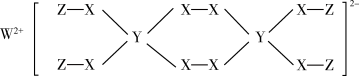X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍,Z和与其同主族的短周期元素可组成常见气体。下列说法不正确 的是
| A.原子半径:W>Y>Z>M>X | B.X、Y、Z三种元素可组成盐 |
C.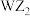 、 、 均可与水发生反应 均可与水发生反应 | D.Y、M、W的最高价氧化物对应的水化物的酸性:M>Y>W |
更新时间:2024-04-04 20:55:00
|
相似题推荐
多选题
|
适中
(0.65)
名校
【推荐1】下列有关离子方程式的书写正确的是
A.用过量氨水吸收工业尾气中的SO2:2NH3•H2O+SO2=2NH +SO +SO +H2O +H2O |
| B.将Na加入CuSO4溶液中:2Na+Cu2+=Cu+2Na+ |
C.NO2通入水中制硝酸:2NO2+H2O=2H++NO +NO +NO |
D.稀硫酸滴入Na2S2O3溶液中:2H++S2O =SO2↑+S↓+H2O =SO2↑+S↓+H2O |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐2】下列实验装置正确的是


| A.装置甲滴定HCl | B.装置乙检验氨气 |
| C.装置丙收集、吸收HCl气体 | D.装置丁验证NO2易溶水实验 |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】下列比较错误的是
| A.原子半径:N>O>F |
| B.酸性强弱:H2SO4>H2SiO3>H2CO3 |
| C.氢化物稳定性:PH3>H2S>HCl |
| D.碱性强弱:KOH>NaOH>Mg(OH)2 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】下列推测合理的是
A.由非金属性: ,推测HF、 ,推测HF、 、 、 的酸性依次增强 的酸性依次增强 |
B.由 与 与 化合生成 化合生成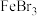 ,推测 ,推测 与 与 化合生成 化合生成 |
C.由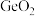 是两性氧化物,推测第ⅣA族元素的最高价氧化物均是两性氧化物 是两性氧化物,推测第ⅣA族元素的最高价氧化物均是两性氧化物 |
D.由 、 、 、 、 不能大量共存,推测 不能大量共存,推测 、 、 、 、 不能大量共存 不能大量共存 |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐1】X、Y、Z、W为短周期元素,它们在周期表中相对位置如图所示。若Y原子的最外层电子是内层电子数的3倍,下列说法正确的是


| A.原子半径:W >Z >X |
| B.非金属性:Z>Y |
| C.最高化合价:Z >X |
| D.最高价氧化物对应水化物的酸性:W>Z |
您最近一年使用:0次
多选题
|
适中
(0.65)
名校
【推荐2】根据下表(部分短周期元素的原子半径及主要化合价)信息,判断以下叙述正确的是( )
| 元素代号 | A | B | C | D | E |
| 原子半径/nm | 0.186 | 0.143 | 0.089 | 0.104 | 0.074 |
| 主要化合价 | +1 | +3 | +2 | +6、-2 | -2 |
| A.C2+与B3+的核外电子数不相等 |
| B.单质与稀盐酸反应的速率A<B |
| C.最高价氧化物对应水化物的碱性A<C |
| D.氢化物的稳定性H2D<H2E |
您最近一年使用:0次
多选题
|
适中
(0.65)
解题方法
【推荐1】X、Y、Z、R、W、Q为原子序数依次增大的短周期元素,其中X与W同主族,Y是形成化合物最多的元素,Q与Y同主族,W与Q同周期。已知常温下单质X与W的状态不同,R的核电荷数是Y的最外层电子数2倍,化合物QY是第三代半导体材料的典型代表。则下列推断中正确的是
| A.由X、Z、R三种元素组成的化合物可能是离子化合物 |
| B.Q与R形成的化合物性质很不活泼,不与任何酸反应 |
| C.原子半径由大到小的顺序是:W>Q>Z>R |
| D.元素的非金属性由强到弱的顺序是:R>Z>Q>Y |
您最近一年使用:0次
多选题
|
适中
(0.65)
【推荐2】有短周期的aXn+ 、bYm-两种元素的简单离子,若它们的电子层结构相同,则下列关系正确的是:
| A.b-a=n+m | B.a-b=n+m | C.核电荷数X>Y | D.质子数Y>X |
您最近一年使用:0次



 溶液滴加到相同浓度的
溶液滴加到相同浓度的 、
、 的混合溶液
的混合溶液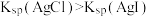
 溶液中通入
溶液中通入
 、
、 混合气体(已达平衡状态)的容器
混合气体(已达平衡状态)的容器
 、
、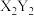 型化合物
型化合物