下列说法正确的是
| I1 | I2 | I3 | I4 | I5 | I6 | I7 |
| 578 | 1817 | 2745 | 11575 | 14830 | 18376 | 23293 |
| A.HF、HCl、H2S、PH3的稳定性依次增强 |
| B.在①P、S,②Mg、Ca,③Al、Si三组元素中,每组中第一电离能较大的元素的原子序数之和为41 |
| C.某主族元素的电离能I1~I7数据如表所示(单位:kJ·mol-1),可推测该元素位于元素周期表第VA族 |
| D.原子半径由小到大的顺序:F、N、Mg、Si |
更新时间:2024-04-11 16:42:28
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】W、X、Y、Z均为的短周期元素,原子序数依次增加,且原子核外L电子层的电子数分别为0、5、8、8,它们的最外层电子数之和为18.下列说法正确的是
A.氧化物的水化物的酸性: | B.单质的氧化性: |
| C.W和X可以形成碱性气体 | D.X与Y不能存在于同一离子化合物中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】硒(Se)是人体必需的微量元素。Se的原子结构示意图如图,下列说法中不正确 的是


| A.Se属于第4周期VIA族元素 |
| B.氢化物的稳定性:H2Se<H2S |
C.核素 Se原子核内的中子数是78 Se原子核内的中子数是78 |
| D.Se的最高价氧化物对应的水化物是H2SeO4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】X、Y、Z、W是原子序数依次递增的短周期主族元素,其中X可形成与He原子电子层结构相同的阴离子;X与Y形成的化合物是光合作用的原料之一;Y与Z两元素的单质反应可生成一种淡黄色的固体;Z、W最高正价相差6,下列说法正确的是
| A.X、Z两元素间可形成共价键 | B.W的氧化物对应的水化物均为强酸 |
| C.原子半径:Y<Z<W | D.Y的某种单质可用于消毒杀菌 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列化合物中,阴阳离子半径之比最大的是
| A.LiI | B.NaBr | C. | D.CsI |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列顺序不正确的是( )
| A.热稳定性:HF>HCl>HBr>HI |
| B.微粒的半径:Cl->Na+>Mg2+>Al3+ |
| C.电离程度(同温度同浓度中):HCl>CH3COOH>NaHCO3 |
| D.晶体的熔点:金刚石>食盐>干冰 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】肼(N2H4)又称为联氨,熔、沸点分别为1.4°C、113.5°C,可用如下方法制备肼:CO(NH2)2+ClO- +2OH- =N2H4+Cl-+CO +H2O。下列有关说法正确的是
+H2O。下列有关说法正确的是
 +H2O。下列有关说法正确的是
+H2O。下列有关说法正确的是| A.N2H4中只存在极性键 |
B. CO 的空间构型为三角锥形 的空间构型为三角锥形 |
| C.CO(NH2)2中C、N、O三种元素第一电离能大小顺序是:C<N<O |
| D.肼的相对分子质量与乙烯接近,但沸点远高于乙烯的原因是能形成分子间氢键 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列说法正确的是
| A.某主族金属元素气态基态原子的逐级电离能的数值分别为738、1451、7733、10540、13630、17995、21703……当它与氯气反应时生成的阳离子是X2+ |
B.在氨水中,大部分NH3与H2O以氢键结合形成NH3•H2O分子,则NH3•H2O的结构式为: |
| C.18g冰中所含的氢键数均为4mol |
| D.由于氢键的作用,NH3、H2O、HF中的沸点反常,且沸点高低顺序为HF>H2O>NH3 |
您最近一年使用:0次

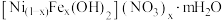 。下列说法不正确的是
。下列说法不正确的是 位于元素周期表中第Ⅷ族
位于元素周期表中第Ⅷ族 核外电子填充在15个轨道中
核外电子填充在15个轨道中 大的只有一种
大的只有一种

