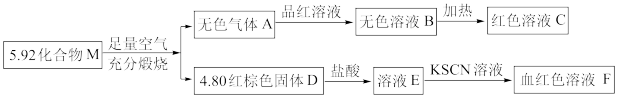
及其盐都是重要的化工原料。
及其盐都是重要的化工原料。(1)向生石灰中滴加浓氨水,可以快速制取氨气,发生反应的化学方程式为
 ,连接顺序为a→
,连接顺序为a→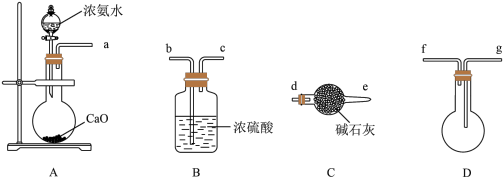
 性质实验的装置如图。
性质实验的装置如图。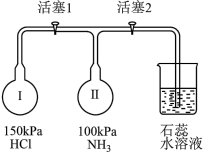
(3)某研究小组用磷酸(
 )吸收氨气制备干粉灭火剂磷酸氢二铵[
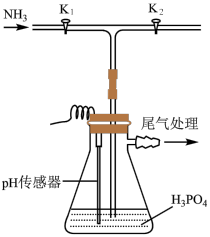
)吸收氨气制备干粉灭火剂磷酸氢二铵[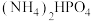 ],装置如图所示。当溶液pH为8.0~9.0时,停止通
],装置如图所示。当溶液pH为8.0~9.0时,停止通 ,即可制得[
,即可制得[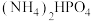 ]溶液。实验过程中,当出现
]溶液。实验过程中,当出现 ,打开
,打开 。
。
 和
和 混合物,称取该混合物固体样品3.62g,加入足量NaOH溶液,充分反应,生成
混合物,称取该混合物固体样品3.62g,加入足量NaOH溶液,充分反应,生成 896mL(标准状况),
896mL(标准状况),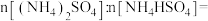
更新时间:2024-04-12 11:51:00
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】物质的量是高中化学中常用的物理量,请回答下列问题:
(1)某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO42-的物质的量是_____ mol。
(2)在标准状况下,4.48 L HCl气体溶于水配成500 mL溶液,其物质的量浓度为_____________ 。
(3)在标准状况下,1.7 g氨气所占的体积约为_________ L,与_____ mol H2S含有相同的氢原子数。
(4)7.8 g Na2X中含Na+ 0.2 mol,则X的摩尔质量是_____________________ 。
(5)实验室需要0.3 mol•L-1硫酸溶液480 mL。
①配制过程用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管、试剂瓶外,还需要______________ 。
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为______ mL。
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:_______________ 。
(1)某硫酸钠溶液中含有3.01×1023个Na+,则溶液中SO42-的物质的量是
(2)在标准状况下,4.48 L HCl气体溶于水配成500 mL溶液,其物质的量浓度为
(3)在标准状况下,1.7 g氨气所占的体积约为
(4)7.8 g Na2X中含Na+ 0.2 mol,则X的摩尔质量是
(5)实验室需要0.3 mol•L-1硫酸溶液480 mL。
①配制过程用到的玻璃仪器除烧杯、量筒、玻璃棒、胶头滴管、试剂瓶外,还需要
②需量取质量分数为98%、密度为1.84 g•cm-3的浓硫酸的体积为
③配制过程中需先在烧杯中将浓硫酸进行稀释,操作方法是:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】一水草酸钙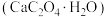 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:
(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在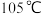 干燥得产品。
干燥得产品。
①已知 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:___________ 。
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取 样品加热,样品的固体残留率
样品加热,样品的固体残留率
 )随温度的变化如下图所示。
)随温度的变化如下图所示。

① 时残留固体的成分为
时残留固体的成分为___________ , 时残留固体的成分为
时残留固体的成分为___________ 。
②已知 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为___________ g, 的质量为
的质量为___________ g。
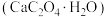 可用作分离稀有金属的载体。回答下列问题:
可用作分离稀有金属的载体。回答下列问题:(1)制备一水草酸钙的方法如下:
先用精制氯化钙稀溶液与草酸钠溶液共热反应,过滤,将固体溶于热盐酸中;再加氨水反应得一水草酸钙沉淀,过滤,热水洗涤,在
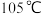 干燥得产品。
干燥得产品。①已知
 溶液的
溶液的 质量浓度为
质量浓度为 ,则该溶液中
,则该溶液中 的物质的量浓度为
的物质的量浓度为②写出上述再加入氨水反应生成一水草酸钙沉淀的化学方程式:
(2)为研究一水草酸钙的热分解性质,进行如下实验:准确称取
 样品加热,样品的固体残留率
样品加热,样品的固体残留率 )随温度的变化如下图所示。
)随温度的变化如下图所示。
①
 时残留固体的成分为
时残留固体的成分为 时残留固体的成分为
时残留固体的成分为②已知
 时固体的成分为
时固体的成分为 和
和 ,则
,则 的质量为
的质量为 的质量为
的质量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】氮氧化物(NOx)是大气污染物之一,处理工业废气中的NOx对于环境保护具有重要的意义。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。
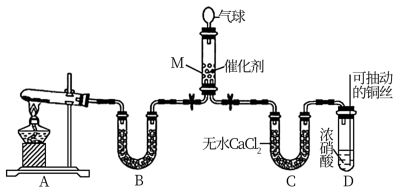
①用装置A制备NH3,其中发生反应的化学方程式为___________ 。
②装置D中铜丝可抽动的优点是___________ 。
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为___________ 。
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:(α表示NOx中NO2的含量):
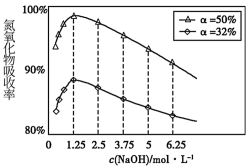
用NaOH溶液吸收氮氧化物的最佳条件为:___________ 。
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为___________ 。
(3)电化学气敏传感器可用于监测环境中 的含量,其工作原理如图。
的含量,其工作原理如图。
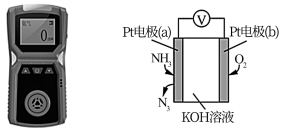
①离子导体中, 向Pt电极
向Pt电极___________ (填“a”或“b”)移动;
②写出Pt电极(a)上的电极反应式:___________ 。
(1)在一定条件下NH3可将NO2还原。甲同学在实验室对该反应进行了探究。实验设计如图(部分夹持装置省略)。

①用装置A制备NH3,其中发生反应的化学方程式为
②装置D中铜丝可抽动的优点是
③在装置M中NH3和NO2充分反应,生成两种对环境友好的物质,该反应中NH3和NO2的物质的量之比为
(2)用NaOH溶液吸收法处理NOx(仅含NO、NO2)。已知过程中发生的反应有:2NaOH+NO+NO2=2NaNO2+H2O;2NaOH+2NO2=NaNO3+NaNO2+H2O
①用不同浓度的NaOH溶液吸收NO2含量不同的尾气,关系如图:(α表示NOx中NO2的含量):

用NaOH溶液吸收氮氧化物的最佳条件为:
②若一定体积的NOx被250mL2mol·L-1的NaOH溶液恰好完全吸收,溶液质量增加19.8g,则x的值为
(3)电化学气敏传感器可用于监测环境中
 的含量,其工作原理如图。
的含量,其工作原理如图。
①离子导体中,
 向Pt电极
向Pt电极②写出Pt电极(a)上的电极反应式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表是元素周期表的一部分,请针对表中标号为①~⑩的元素回答下列问题。
(1)非金属性最强的元素是_______ (填元素符号,下同)。
(2)这些元素的最高价氧化物对应水化物中碱性最强的是_______ (填化学式,下同),具有两性的是_______ ,这两种物质发生反应的离子方程式为_______ 。
(3)写出⑤⑨形成化合物的电子式:_______ 。
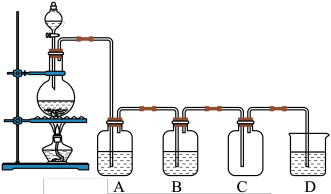
(4)某化学研究性学习小组利用以下装置制取并探究②的最简单氢化物的性质。在A装置中发生反应的化学方程式为_______ 。
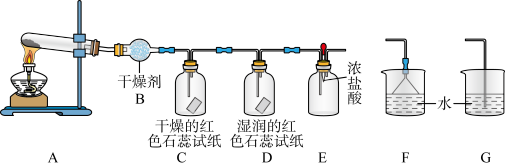
ⅰ.B装置中的干燥剂是_______ 。
ⅱ.C、D 装置中试纸颜色会发生变化的是_______ (填”C”或“D”)。
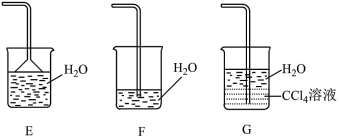
ⅲ.当实验进行段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是_______ 。
ⅳ.为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是_______ (填“F”或“G”)。
| 族 周期 | IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ③ | ④ | ||||
| 三 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
(2)这些元素的最高价氧化物对应水化物中碱性最强的是
(3)写出⑤⑨形成化合物的电子式:
(4)某化学研究性学习小组利用以下装置制取并探究②的最简单氢化物的性质。在A装置中发生反应的化学方程式为

ⅰ.B装置中的干燥剂是
ⅱ.C、D 装置中试纸颜色会发生变化的是
ⅲ.当实验进行段时间后,挤压E装置中的胶头滴管,滴入1-2滴浓盐酸,可观察到 E装置中的现象是
ⅳ.为防止过量氨气造成空气污染,需要在上述装置的末端增加一个尾气处理装置,合适的装置是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】元素周期表的一部分如图所示,请参照元素a~1在表中的位置,回答下列问题:
(1)常温下,单质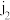 的颜色为
的颜色为_______ ,元素a~1中,金属性最强的元素为_______ (填化学名称)。
(2)实验室通常将f所形成的单质保存在_______ 中。
(3)实验室常采用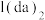 固体和
固体和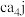 固体在加热条件下制备
固体在加热条件下制备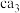 :
:
①实验室收集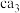 气体,可采用的方法为
气体,可采用的方法为_______ (填标号)。

②反应后所得生成物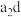 的空间结构为
的空间结构为_______ 。
③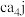 的电子式为
的电子式为_______ 。
(4)酸性: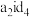
_______ (填“>”、“<”或“=”)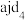 ,判断的理由为
,判断的理由为_______ 。
(5)写出 与fda溶液发生反应的离子方程式:
与fda溶液发生反应的离子方程式:_______ 。
族 周期 | IA | 0 | |||||||
| 1 | a | IIA | …… | IIIA | IVA | VA | VIA | VIIA | |
| 2 | b | …… | c | d | e | ||||
| 3 | f | …… | g | h | i | j | |||
| 4 | k | l | …… | ||||||
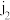 的颜色为
的颜色为(2)实验室通常将f所形成的单质保存在
(3)实验室常采用
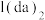 固体和
固体和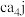 固体在加热条件下制备
固体在加热条件下制备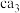 :
:①实验室收集
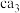 气体,可采用的方法为
气体,可采用的方法为
②反应后所得生成物
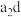 的空间结构为
的空间结构为③
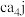 的电子式为
的电子式为(4)酸性:
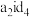
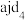 ,判断的理由为
,判断的理由为(5)写出
 与fda溶液发生反应的离子方程式:
与fda溶液发生反应的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】如图表示配制100mL0.100molL﹣1Na2CO3溶液的几个关键实验步骤和操作,据图回答下列问题:
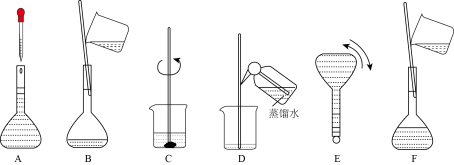
(1)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是_____ 。
①干燥的 ②瓶塞不漏水的 ③用欲配制的溶液润洗过的 ④以上三项均须要求的
(2)若用Na2CO3•10H2O来配制溶液,需要称量晶体_____ 克。若所称取的晶体已经有一部分失去了结晶水,则所配制的溶液浓度偏_____ 。(填“大/小”)
(3)写出配制溶液中所需要用到的玻璃仪器的名称:烧杯、_____ 。
(4)步骤B通常称为转移,步骤A通常称为_____ 。步骤D称为_____ ,若没有步骤D,则配制的浓度偏_____ 。(填“大/小”)。
(5)将上述实验步骤A﹣F按实验过程先后次序排列_____ 。

(1)用容量瓶配制一定物质的量浓度的溶液,该容量瓶必须是
①干燥的 ②瓶塞不漏水的 ③用欲配制的溶液润洗过的 ④以上三项均须要求的
(2)若用Na2CO3•10H2O来配制溶液,需要称量晶体
(3)写出配制溶液中所需要用到的玻璃仪器的名称:烧杯、
(4)步骤B通常称为转移,步骤A通常称为
(5)将上述实验步骤A﹣F按实验过程先后次序排列
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】Ⅰ. 现有6种物质:① 、②
、② 溶液、③
溶液、③ 溶液、④熔化的
溶液、④熔化的 、⑤
、⑤ 胶体、⑥
胶体、⑥ 晶体。
晶体。
(1)能导电的电解质有_______ (填序号)。
(2)实验室中①通常保存在_______ 中。
(3)检验⑥中阳离子常用的实验方法是_______ 。
(4)区分②和⑤常用的实验方法是_______ 。
Ⅱ.实验是化学研究的重要手段,现有如图所示仪器,请根据要求填空。

(5)C的名称是_______ 。
(6)公元前4000年前,古人就已掌握酿酒技术。蒸馏是现代酿酒不可缺少的工艺之一,上述仪器可以用于蒸馏的是_______ (填序号)。
(7)用仪器A配制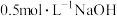 溶液时,需用托盘天平称取固体
溶液时,需用托盘天平称取固体_______ g;若定容时俯视刻度线,则对所配溶液的浓度有何影响?_______ (填“偏大”“偏小”或“无影响”)。
 、②
、② 溶液、③
溶液、③ 溶液、④熔化的
溶液、④熔化的 、⑤
、⑤ 胶体、⑥
胶体、⑥ 晶体。
晶体。(1)能导电的电解质有
(2)实验室中①通常保存在
(3)检验⑥中阳离子常用的实验方法是
(4)区分②和⑤常用的实验方法是
Ⅱ.实验是化学研究的重要手段,现有如图所示仪器,请根据要求填空。

(5)C的名称是
(6)公元前4000年前,古人就已掌握酿酒技术。蒸馏是现代酿酒不可缺少的工艺之一,上述仪器可以用于蒸馏的是
(7)用仪器A配制
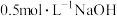 溶液时,需用托盘天平称取固体
溶液时,需用托盘天平称取固体
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室中常用二氧化锰与浓盐酸共热制取氯气。某化学兴趣小组为制取较为纯净、干燥的氯气,设计了如图实验装置。
请回答下列问题:
(1)Cl2是_______ 的气体;(填“黄绿色”或“无色”),Cl2气体收集方法为_______ ;(A.向上排空气法B.向下排空气法);实验室制取Cl2的离子方程式为_______ 。
(2)A中盛放的是_______ ,其作用为_______ 。
(3)B中盛放的是_______ ,其作用为_______ 。
(4)D中盛放的是_______ ,其作用为_______ ,相关反应的化学方程式为:_______

请回答下列问题:
(1)Cl2是
(2)A中盛放的是
(3)B中盛放的是
(4)D中盛放的是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】硫酰氯(SO2Cl2)是一种重要的化工试剂,实验室合成硫酰氯的实验装置如图所示:
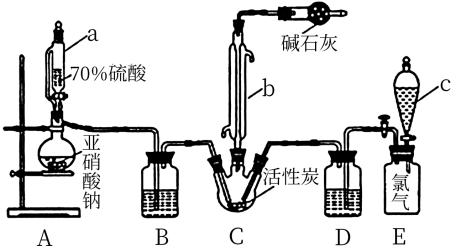
③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是__ 。
(2)仪器b的名称为___ ,干燥管中碱石灰的主要作用是___ 。
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为___ 。长期存放的硫酰氯会发黄,其原因可能为___ 。
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为___ ,分离这两种液态产物的方法是___ 。
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应。___ (简要描述实验步骤、现象和结论)。
(6)SO2Cl2纯度的测定:取1.50gSO2Cl2产品在密闭条件下溶于烧碱溶液,最后定容为250mL溶液,取25.00mL该溶液用0.1000moL/L的AgNO3标准溶液滴定(用K2CrO4作指示剂,滴定过程种SO 不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为___ 。

③100℃以上或长时间存放硫酰氯都易分解,生成二氧化硫和氯气。
(1)仪器a为恒压分液漏斗,与普通分液漏斗相比,其优点是
(2)仪器b的名称为
(3)装置E为储气装置,用于提供氯气,则分液漏斗c中盛放的试剂为
(4)氯磺酸(ClSO3H)加热分解,也能制得硫酰氯与另外一种物质,该反应的化学方程式为
(5)若将SO2、Cl2按照一定比例通入水中,请设计简单实验验证二者是否恰好完全反应。
(6)SO2Cl2纯度的测定:取1.50gSO2Cl2产品在密闭条件下溶于烧碱溶液,最后定容为250mL溶液,取25.00mL该溶液用0.1000moL/L的AgNO3标准溶液滴定(用K2CrO4作指示剂,滴定过程种SO
 不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
不参与反应),平行滴定三次,平均消耗AgNO3标准溶液22.00mL,则SO2Cl2产品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为探究Na与CO2反应产物,某化学兴趣小组按如图装置进行实验。已知:CO+2Ag(NH3)2OH=2Ag↓+(NH4)2CO3+2NH3。
回答下列问题:
(1)写出A中反应的离子方程式__________ ;
(2)仪器X的名称是_______ ,B中的溶液为_________ ;
(3)先称量硬质玻璃管的质量为mlg,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g。再进行下列实验操作,其正确顺序是_____ (填标号);
a.点燃酒精灯,加热b.熄灭酒精灯c.关闭K1和K2
d.打开K1和K2,通入CO2至E中出现浑浊e.称量硬质玻璃管
f.冷却到室温重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g。
(4)加热硬质玻璃管一段时间,观察到以下现象:①钠块表面变黑,熔融成金属小球;②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;③F中试管内壁有银白物质产生。产生上述②现象的原因是________ ;
(5)探究固体产物中元素Na的存在形式
假设一:只有Na2CO3;
假设二:只有Na2O;
假设三:Na2O和Na2CO3均有
完成下列实验设计,验证上述假设:
(6)根据上述实验现象及下表实验数据,写出Na与CO2反应的总化学方程式____ 。

回答下列问题:
(1)写出A中反应的离子方程式
(2)仪器X的名称是
(3)先称量硬质玻璃管的质量为mlg,将样品装入硬质玻璃管中,称得样品和硬质玻璃管的总质量是m2g。再进行下列实验操作,其正确顺序是
a.点燃酒精灯,加热b.熄灭酒精灯c.关闭K1和K2
d.打开K1和K2,通入CO2至E中出现浑浊e.称量硬质玻璃管
f.冷却到室温重复上述操作步骤,直至硬质玻璃管恒重,称得质量为m3g。
(4)加热硬质玻璃管一段时间,观察到以下现象:①钠块表面变黑,熔融成金属小球;②继续加热,钠迅速燃烧,产生黄色火焰。反应完全后,管中有大量黑色物质;③F中试管内壁有银白物质产生。产生上述②现象的原因是
(5)探究固体产物中元素Na的存在形式
假设一:只有Na2CO3;
假设二:只有Na2O;
假设三:Na2O和Na2CO3均有
完成下列实验设计,验证上述假设:
| 步骤 | 操作 | 结论 |
| 1 | 将硬质玻璃管中的固体产物溶于水后过滤; | 假设一成立 |
| 2 | 往步骤1所得滤液中 现象: |
| m1 | m2 | m3 |
| 66.7g | 69.0g | 72.1g |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】84消毒液的有效成分是NaClO,广泛应用于杀菌、消毒及化工领域。实验室中利用下图装置(部分装置省略)制备NaClO,并探究氯气的性质。经查阅到资料可知:“氯气与水的反应是放热反应,在加热条件下氯气与碱液发生如下反应:3Cl2+6NaOH 5NaCl+NaClO3+3H2O。
5NaCl+NaClO3+3H2O。

回答下列问题:
(1)装置A、D中发生反应的离子方程式分别为:A:_______ ;D:_______ ;
(2)装置B能否省去的_______ (填“能”或“不能”),理由是_______ ;
(3)装置D中采用冰水浴冷却的目的是_______ 。
(4)理论上制备14.9g次氯酸钠,需要Cl2_______ g,消耗MnO2_______ g。
(5)如图是检验Cl2性质的装置图示,完成下列问题。

①装置a中浓H2SO4的作用是_______ ;该装置能否省去_______ (填“能”或“不能)
②装置b、c实验现象分别为:b_______ ;c_______ ;对比b和c中现象得出的结论是_______ 。
 5NaCl+NaClO3+3H2O。
5NaCl+NaClO3+3H2O。
回答下列问题:
(1)装置A、D中发生反应的离子方程式分别为:A:
(2)装置B能否省去的
(3)装置D中采用冰水浴冷却的目的是
(4)理论上制备14.9g次氯酸钠,需要Cl2
(5)如图是检验Cl2性质的装置图示,完成下列问题。

①装置a中浓H2SO4的作用是
②装置b、c实验现象分别为:b
您最近一年使用:0次