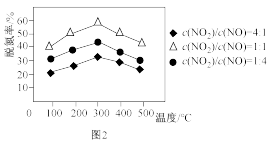
设计物质间的转化途径,是认识和研究物质及其变化的一种常用的科学方法。物质 能发生连续氧化,
能发生连续氧化,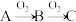 (其他反应条件未标出)
(其他反应条件未标出)
(1)若 为单质,
为单质, 与水反应生成二元强酸,写出
与水反应生成二元强酸,写出 反应的化学方程式
反应的化学方程式___________ ,B与一种黄绿色气体等体积通入到水中发生反应也可生成该二元强酸。写出该反应的离子方程式_________ 。
(2)若 为单质,
为单质, 与水反应生成一元强碱,
与水反应生成一元强碱, 中阴阳离子的个数比是
中阴阳离子的个数比是___________ ,C的电子式____________ , 反应消耗标准状况下
反应消耗标准状况下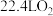 ,转移的电子数是
,转移的电子数是_________ 。
(3)若 氢化物,
氢化物, 与水反应生成一元强酸,
与水反应生成一元强酸, 的浓溶液可用于检查氯气管道是否发生泄露,如泄露看到的现象是
的浓溶液可用于检查氯气管道是否发生泄露,如泄露看到的现象是_____________ ,吸收 的装置合理的是
的装置合理的是_____________ (填序号)。
 能发生连续氧化,
能发生连续氧化,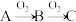 (其他反应条件未标出)
(其他反应条件未标出)(1)若
 为单质,
为单质, 与水反应生成二元强酸,写出
与水反应生成二元强酸,写出 反应的化学方程式
反应的化学方程式(2)若
 为单质,
为单质, 与水反应生成一元强碱,
与水反应生成一元强碱, 中阴阳离子的个数比是
中阴阳离子的个数比是 反应消耗标准状况下
反应消耗标准状况下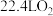 ,转移的电子数是
,转移的电子数是(3)若
 氢化物,
氢化物, 与水反应生成一元强酸,
与水反应生成一元强酸, 的浓溶液可用于检查氯气管道是否发生泄露,如泄露看到的现象是
的浓溶液可用于检查氯气管道是否发生泄露,如泄露看到的现象是 的装置合理的是
的装置合理的是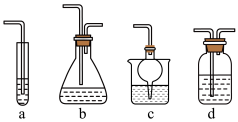
更新时间:2024-04-17 09:41:23
|
相似题推荐
填空题
|
适中
(0.65)
解题方法
【推荐1】离子反应是中学化学中重要的反应类型,回答下列问题:
(1)在发生离子反应的反应物或生成物中,一定存在_______ (填序号)。
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子: 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:
Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。
Ⅲ.取少许原溶液先滴加稀硝酸,再滴入 溶液,产生白色沉淀。
溶液,产生白色沉淀。
Ⅳ.取少许原溶液,滴入少量 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。
①根据以上现象判断,原溶液中肯定不存在的离子是_______ ;肯定存在的离子是_______ 。
②若原溶液中各种离子的浓度相等,确定该溶液中_______ (填“有”或“无”) ,判断依据是
,判断依据是_______ 。
③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:_______ 。
(1)在发生离子反应的反应物或生成物中,一定存在
①单质 ②氧化物 ③电解质 ④盐 ⑤化合物
(2)将两种化合物一起溶于水得到一种无色透明溶液,溶液中可能含有下列离子中的某些离子:
 、
、 、
、 、
、 、
、 、
、 、
、 和
和 。取该溶液进行如下实验:
。取该溶液进行如下实验:Ⅰ.取少许原溶液,滴入紫色石蕊溶液,溶液呈蓝色。
Ⅱ.取少许原溶液,滴入
 溶液,无白色沉淀产生。
溶液,无白色沉淀产生。Ⅲ.取少许原溶液先滴加稀硝酸,再滴入
 溶液,产生白色沉淀。
溶液,产生白色沉淀。Ⅳ.取少许原溶液,滴入少量
 溶液,有白色沉淀产生。
溶液,有白色沉淀产生。①根据以上现象判断,原溶液中肯定不存在的离子是
②若原溶液中各种离子的浓度相等,确定该溶液中
 ,判断依据是
,判断依据是③若原溶液中各离子的浓度相等,取一定量该溶液,加入等体积的稀硫酸(其中硫酸根浓度与原溶液中各离子浓度相等),写出发生反应的离子方程式:
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐2】(1)向某溶液中加入KSCN溶液无明显现象,再滴入数滴氯水后,溶液立即变成红色,则原溶液中一定含有_______ 离子,要除去FeCl3溶液中少量的氯化亚铁,可行的办法是_______ (填字母)。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式_______ 。
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式_______ 。
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是_______ (填字母)。
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是_______ nm,区别该液体和FeCl3溶液可用_______ 方法。
A.加入铜粉 B.加入铁粉 C.通入氯气 D.加入KSCN溶液
根据选用的试剂,写出除去FeCl3溶液中少量的氯化亚铁过程中发生反应的离子方程式
(2)电子工业常用30%的FeCl3溶液腐蚀铜箔,制造印刷线路板,写出FeCl3与金属铜反应的离子方程式
(3)使用过的腐蚀液会失效,但可以回收利用,某兴趣小组为了从使用过的腐蚀液中回收铜,应使用的试剂是
A.铜粉 B.氯气 C.铁粉 D.KSCN溶液
(4)向沸水中逐滴滴加1 mol·L-1FeCl3溶液至液体呈透明的红褐色,该分散系中微粒直径的范围是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】按要求完成下列填空
I.(1)给定条件下的下列四种物质:
a.10g氖气
b.含有40mol电子的NH3
c.标准状况下8.96LCO2
d.标准状况下112g液态水
则上述物质中所含分子数目由多到少的顺序是________________ (填序号)。
(2)标准状况下,0.51g某气体的体积为672mL,则该气体摩尔质量为______ 。
(3)将100mL H2SO4和HCl的混合溶液分成两等份,一份中加入含0.2molNaOH溶液时恰好中和完全,向另一份中加入含0.05molBaCl2溶液时恰好沉淀完全,则原溶液中c(Cl-)=____ mol/L。
II.现有以下物质:①铝;②二氧化硅;③液氯;④NaOH溶液;⑤液态HCl;⑥NaHCO3晶体;⑦蔗糖;⑧熔融Na2O;⑨Na2O2固体;⑩CO2。回答下列问题(用相应物质的序号填写):
(1)其中可以导电的有__________ 。
(2)属于电解质的有_______ ,非电解质有__________ 。
(3)写出向⑨与⑩反应的化学方程式___________ 。
(4)写出①与④的离子方程式_____________ 。
(5)写出⑤的水溶液与⑥的水溶液反应的离子方程式___________________ 。
(6)写出②与④反应的离子方程式_______________________________ 。
I.(1)给定条件下的下列四种物质:
a.10g氖气
b.含有40mol电子的NH3
c.标准状况下8.96LCO2
d.标准状况下112g液态水
则上述物质中所含分子数目由多到少的顺序是
(2)标准状况下,0.51g某气体的体积为672mL,则该气体摩尔质量为
(3)将100mL H2SO4和HCl的混合溶液分成两等份,一份中加入含0.2molNaOH溶液时恰好中和完全,向另一份中加入含0.05molBaCl2溶液时恰好沉淀完全,则原溶液中c(Cl-)=
II.现有以下物质:①铝;②二氧化硅;③液氯;④NaOH溶液;⑤液态HCl;⑥NaHCO3晶体;⑦蔗糖;⑧熔融Na2O;⑨Na2O2固体;⑩CO2。回答下列问题(用相应物质的序号填写):
(1)其中可以导电的有
(2)属于电解质的有
(3)写出向⑨与⑩反应的化学方程式
(4)写出①与④的离子方程式
(5)写出⑤的水溶液与⑥的水溶液反应的离子方程式
(6)写出②与④反应的离子方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】有一包白色固体,可能含有 、
、 、KCl、
、KCl、 和无水
和无水 ,按下列步骤做实验:
,按下列步骤做实验:
①将该白色固体溶于水,得到无色溶液;
②向所得的无色溶液中加入足量 溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
回答下列问题:
(1)该白色固体中一定存在的物质是___________ ,一定不存在的物质是___________ ,可能存在的物质是___________ 。
(2)称取该白色固体3.53 g,将其溶于水得到溶液A,在A中加入50 mL未知的 溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
①该白色固体中 的质量分数为
的质量分数为___________ (保留2位有效数字,下同)。
② 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为___________ 。
③该白色固体的成分是___________ 。
 、
、 、KCl、
、KCl、 和无水
和无水 ,按下列步骤做实验:
,按下列步骤做实验:①将该白色固体溶于水,得到无色溶液;
②向所得的无色溶液中加入足量
 溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。
溶液,得到白色沉淀,再加稀硝酸,白色沉淀部分溶解并有气泡产生,将气体通入澄清石灰水中,石灰水变浑浊。回答下列问题:
(1)该白色固体中一定存在的物质是
(2)称取该白色固体3.53 g,将其溶于水得到溶液A,在A中加入50 mL未知的
 溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。
溶液恰好完全反应,过滤得沉淀B,向B中加入足量稀硝酸,充分反应后剩余沉淀2.87g,同时放出0.224 L气体(标准状况)。①该白色固体中
 的质量分数为
的质量分数为②
 溶液中溶质的物质的量浓度为
溶液中溶质的物质的量浓度为③该白色固体的成分是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】下表为元素周期表的一部分,参照元素①~⑦在表中的位置,请用化学用语回答下列问题:
(1)④、⑥、⑦的离子半径由大到小的顺序为___________ 。
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式___________ 。
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为________ 。在酸性溶液中该物质能将Fe2+氧化,写出该反应的离子方程式___________ 。
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。
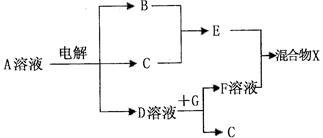
①写出D溶液与G反应的化学方程式_________________________________ 。
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为________ mol。
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有_______________ 。
| ⅠA | 0 | |||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ④ | ||||||
| 3 | ⑤ | ③ | ⑥ | ⑦ | ||||
(1)④、⑥、⑦的离子半径由大到小的顺序为
(2)1971年美国科学家通过细冰获得含元素④的含氧酸(HXO),在与水反应时,两种分子中的共价键分别断裂成两部分,再重新组合,写出该反应的化学方程式
(3)①、②两种元素的原子按1:1组成的常见液态化合物的电子式为
(4)由表中元素形成的物质可发生下图中的反应,其中B、C、G是单质,B为黄绿色气
体,D溶液显碱性。

①写出D溶液与G反应的化学方程式
②常温下,若电解l L 0.1 mol/L A溶液,一段时间后测得溶液pH为12(忽略溶液体积变化),则该电解过程中转移电子的物质的量为
③若仅电解l L 0.1 mol/L A溶液,图中各步反应均为完全转化,而各物质在反应过程中没有损耗,则混合物X中含有的物质有
您最近半年使用:0次
填空题
|
适中
(0.65)
【推荐1】研究氮的循环和转化对生产、生活有重要的价值。
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。

(1)设备1中发生反应的化学方程式是_______ 。
(2)设备2中通入的NO与A反应生成红棕色气体,该气体再与水反应生成硝酸,该过程中发生反应的化学方程式依次为_______ 、_______ 。
(3)若1molNH3经过以上流程恰好完全反应生成NH4NO3,则过程中参与反应的O2的物质的量为_______ 。
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
含NH 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水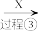 达标。
达标。
(4)过程①的目的是将NH 转化为NH3,该过程中鼓入大量空气的目的是
转化为NH3,该过程中鼓入大量空气的目的是_______ 。
(5)过程②加入NaClO溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为_______ 、_______ 。
(6)含余氯废水的主要成分是NaClO,X可选用Na2SO3将其除去,写出其离子反应方程式_______ 。
I.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。

(1)设备1中发生反应的化学方程式是
(2)设备2中通入的NO与A反应生成红棕色气体,该气体再与水反应生成硝酸,该过程中发生反应的化学方程式依次为
(3)若1molNH3经过以上流程恰好完全反应生成NH4NO3,则过程中参与反应的O2的物质的量为
II.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH
 和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:
和NH3·H2O的形式存在。某工厂处理氨氮废水的流程如下:含NH
 的废水
的废水 低浓度氨氮废水
低浓度氨氮废水 含余氯废水
含余氯废水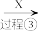 达标。
达标。(4)过程①的目的是将NH
 转化为NH3,该过程中鼓入大量空气的目的是
转化为NH3,该过程中鼓入大量空气的目的是(5)过程②加入NaClO溶液可将氨氮物质转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为
(6)含余氯废水的主要成分是NaClO,X可选用Na2SO3将其除去,写出其离子反应方程式
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】氮、磷、钾号称肥料的“三要素”,化学肥料的施用,使农业增产增收,经济效益显著。但是化学肥料的滥施乱用也对环境产生了许多不良影响。请根据相关知识和信息回答下列问题:
(1)如图是某品牌化肥包装袋中的部分文字

①写出以氨为原料制取该化肥的各步化学方程式_______ 。
②关于该氮肥的处置和施用正确的方法是_______ 。
A.与草木灰混合施用
B.如果结块,可用铁锤敲击
C.与钙镁磷肥混合施用
D.在经常排灌水的稻田中施用肥效最高
③若该化肥的杂质中不含氮元素,则该化肥的纯度是_______ 。
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
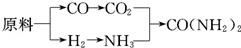
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?_______ 。
(3)近年来“水华”和“赤潮”时有发生,据专家分析,是因水体富营养化造成的,试分析水体富营养化的原因_______ 。
(1)如图是某品牌化肥包装袋中的部分文字

①写出以氨为原料制取该化肥的各步化学方程式
②关于该氮肥的处置和施用正确的方法是
A.与草木灰混合施用
B.如果结块,可用铁锤敲击
C.与钙镁磷肥混合施用
D.在经常排灌水的稻田中施用肥效最高
③若该化肥的杂质中不含氮元素,则该化肥的纯度是
(2)甲、乙、丙三个化肥厂生产尿素所用的原料不同,但生产流程相同:
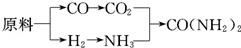
①甲厂以焦炭和水为原料;②乙厂以天然气和水为原料;③丙厂以石脑油(主要成分为C5H12)和水为原料。按工业有关规定,利用原料所制得的原料气H2和CO2的物质的量之比,若最接近合成尿素的原料气NH3(换算成H2的物质的量)和CO2的物质的量之比,则对原料的利用率最高。据此判断甲、乙、丙三个工厂哪个工厂对原料的利用率最高?
(3)近年来“水华”和“赤潮”时有发生,据专家分析,是因水体富营养化造成的,试分析水体富营养化的原因
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)请写出以下物质的电离方程式:
H2SO4_______ ;NaOH_____ ;NaHSO4_______ ;Al2(SO4)3_____ 。
(2)用双线桥法表示以下氧化还原反应中电子转移方向和数目_____ 。
2Na+2H2O =2NaOH+H2↑
(3)用单线桥法表示以下氧化还原反应中电子转移方向和数目_____ 。
Fe+2HCl=FeCl2+H2↑
(4)钠在空气中变质的最终产物是_______ 。(填化学式)
(1)请写出以下物质的电离方程式:
H2SO4
(2)用双线桥法表示以下氧化还原反应中电子转移方向和数目
2Na+2H2O =2NaOH+H2↑
(3)用单线桥法表示以下氧化还原反应中电子转移方向和数目
Fe+2HCl=FeCl2+H2↑
(4)钠在空气中变质的最终产物是
您最近半年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】按要求填空:
(1)写出 的结构式
的结构式___________ 。
(2)写出 的电子式
的电子式___________ 。
(3)将过量的 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式___________ 。
(4)向 溶液中,缓慢滴加
溶液中,缓慢滴加 溶液至过量,现象是
溶液至过量,现象是___________ 。
(5)金属钠受热燃烧的化学方程式为___________
(6)将铜片投入 溶液中反应的离子方程式
溶液中反应的离子方程式___________ 。
(7)将一定量 投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:
投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:___________ 。
(8)向 溶液中滴入
溶液中滴入 溶液,可观察到的现象是
溶液,可观察到的现象是___________ 。
(1)写出
 的结构式
的结构式(2)写出
 的电子式
的电子式(3)将过量的
 通入
通入 溶液中反应的离子方程式
溶液中反应的离子方程式(4)向
 溶液中,缓慢滴加
溶液中,缓慢滴加 溶液至过量,现象是
溶液至过量,现象是(5)金属钠受热燃烧的化学方程式为
(6)将铜片投入
 溶液中反应的离子方程式
溶液中反应的离子方程式(7)将一定量
 投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:
投入含有酚酞的水中,反应中有大量气泡生成,溶液颜色:(8)向
 溶液中滴入
溶液中滴入 溶液,可观察到的现象是
溶液,可观察到的现象是
您最近半年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】把一小块金属钠投入水中,观察到以下各种现象:钠浮在水面上,熔成闪亮的小球,四处游动,逐渐减少,直至消失.
(1)写出该反应的离子方程式_________________ ,其中钠熔成闪亮小球的原因是__________
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式_____________
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式_________ ;继续将沉淀过滤、洗涤、干燥、灼烧,此时得到的固体为_________ (填化学式)。
(1)写出该反应的离子方程式
(2)将所得溶液平均分成两份:
①一份加入足量的铝片充分反应,写出该反应的离子方程式
②向另一份溶液中滴加FeCl3溶液至沉淀不再增加,写出生成沉淀的反应的离子方程式
您最近半年使用:0次

 催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。
催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术,反应原理如图1所示。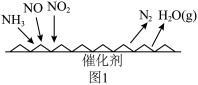
 反应的化学方程式
反应的化学方程式 对应的脱氮率如图2所示,脱氮效果最佳的
对应的脱氮率如图2所示,脱氮效果最佳的