回答下列问题。
(1)第117号元素Ts在周期表中的位置是___________ 。
(2)下图表示铷(Rb)及其化合物的产业链,回答相应问题。___________ (填“小于”或“大于”)钾的离子半径。
②写出由氧化铷制备氢氧化铷的化学方程式___________ 。
③离子推进火箭是通过电离原子气体,转化为阳离子,然后离子被电场力作用加速,通过排气口射出推进器,产生反作用力推动火箭。单质铷适合用于离子推进火箭的原因是___________ 。
(3)阅读短文,回答问题。
硅元素在地壳中的含量仅次于氧。人类很早就利用硅酸盐烧陶制瓷、获得玻璃制品。
1824年,人类成功提炼出硅单质。由石英砂制高纯硅的过程如下:
整个芯片制造过程需要许多高精密度的专业设备,其中不乏我国目前还未完全掌握而被“卡脖子”的技术。我国科学家正开发“碳基”芯片来替代硅基芯片,习近平主席评价此项研究“另辟蹊径,柳暗花明”。
①请依据以上短文,下列说法正确是___________ 。
A.硅元素在自然界中以游离态(单质)形式存在,石英砂的主要成分是SiO2
B.单晶硅做芯片的基底材料与硅元素储量丰富,单晶硅导电性好、耐腐蚀性能优异有关
C.制备单质硅的过程中焦炭过多容易生成副产物金刚砂
D.碳和硅在周期表中位于同一主族,性质相似,因此“碳基”芯片有望替代硅基芯片
②制备高纯硅过程必须严格控制无水无氧,因为SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式___________ 。
③有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似,化学性质活泼,可在空气中自燃,写出乙硅烷在空气中自燃的化学方程式___________ 。
(1)第117号元素Ts在周期表中的位置是
(2)下图表示铷(Rb)及其化合物的产业链,回答相应问题。
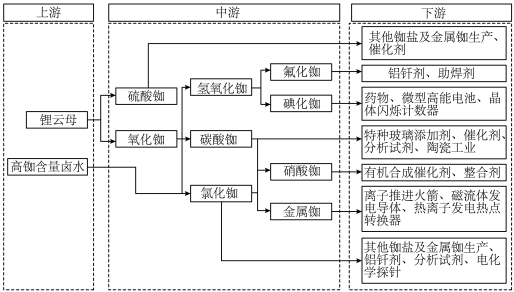
②写出由氧化铷制备氢氧化铷的化学方程式
③离子推进火箭是通过电离原子气体,转化为阳离子,然后离子被电场力作用加速,通过排气口射出推进器,产生反作用力推动火箭。单质铷适合用于离子推进火箭的原因是
(3)阅读短文,回答问题。
硅元素在地壳中的含量仅次于氧。人类很早就利用硅酸盐烧陶制瓷、获得玻璃制品。
1824年,人类成功提炼出硅单质。由石英砂制高纯硅的过程如下:
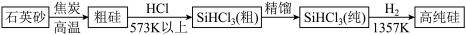
整个芯片制造过程需要许多高精密度的专业设备,其中不乏我国目前还未完全掌握而被“卡脖子”的技术。我国科学家正开发“碳基”芯片来替代硅基芯片,习近平主席评价此项研究“另辟蹊径,柳暗花明”。
①请依据以上短文,下列说法正确是
A.硅元素在自然界中以游离态(单质)形式存在,石英砂的主要成分是SiO2
B.单晶硅做芯片的基底材料与硅元素储量丰富,单晶硅导电性好、耐腐蚀性能优异有关
C.制备单质硅的过程中焦炭过多容易生成副产物金刚砂
D.碳和硅在周期表中位于同一主族,性质相似,因此“碳基”芯片有望替代硅基芯片
②制备高纯硅过程必须严格控制无水无氧,因为SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式
③有一类组成最简单的有机硅化合物叫硅烷,硅烷的组成、结构与相应的烷烃相似,化学性质活泼,可在空气中自燃,写出乙硅烷在空气中自燃的化学方程式
更新时间:2024-04-23 16:59:27
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】(一)工业上提纯硅有多种路线,其中一种工艺流程示意图及主要反应如下:
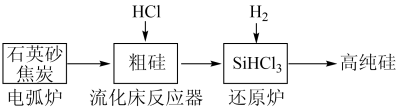
(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:___________ 。
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:___________ 。
(二)某化学兴趣小组利用下列图示装置探究氨气的性质。
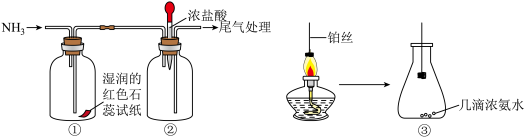
(3)①中湿润的红色石蕊试纸变蓝的原因:___________ (用化学方程式表示)。
(4)向②中滴入浓盐酸,现象为:___________ 。
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:___________ ,瓶中红棕色气体为___________ (填化学式)。
(三)某氨氮废水( 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:

(6)检验氨氮废水中含有 的方法是:
的方法是:___________ 。
(7)过程Ⅱ在硝化细菌作用下实现 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:___________ 。

(1)工业上用石英砂和焦炭在电弧炉中高温加热到1600℃-1800℃生成粗硅的化学方程式为:
(2)在流化床反应的产物中,SiHCl3大约占85%,还有SiCl4、SiH2Cl2、SiH3Cl等,粗硅生成SiHCl3的化学反应为:Si+3HCl
 SiHCl3+H2,生成物SiHCl3的结构式为:
SiHCl3+H2,生成物SiHCl3的结构式为:(二)某化学兴趣小组利用下列图示装置探究氨气的性质。

(3)①中湿润的红色石蕊试纸变蓝的原因:
(4)向②中滴入浓盐酸,现象为:
(5)将灼热的铂丝伸入③中锥形瓶,可观察到铂丝保持红热,有红棕色气体及少量白烟生成。该过程会同时发生多个反应,写出NH3和O2催化氧化的化学方程式:
(三)某氨氮废水(
 、
、 )的生物法处理流程如图所示:
)的生物法处理流程如图所示:
(6)检验氨氮废水中含有
 的方法是:
的方法是:(7)过程Ⅱ在硝化细菌作用下实现
 的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
的转化,称为硝化过程。在碱性条件下实现上述硝化过程的总反应的离子方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】下图是地壳中含量较大的九种元素分布图,图中X、Y、Z分别表示不同元素。
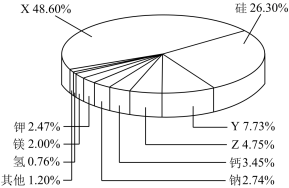
回答下列问题:
(1)X的名称为___________ 。
(2)Y的氧化物属于___________ 氧化物。(填“酸性”、“两性”或“碱性”)。
(3)常用 溶液作为刻制印刷电路时的“腐蚀液”、该反应的离子方程式为
溶液作为刻制印刷电路时的“腐蚀液”、该反应的离子方程式为___________ 。
(4)由粗硅制备硅烷( )的基本流程如下图所示(反应条件均省略):
)的基本流程如下图所示(反应条件均省略):
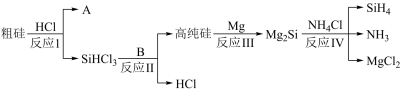
已知:反应Ⅰ、Ⅱ的化学方程式分别为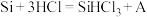 ,
,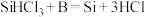 (均已配平)。
(均已配平)。
①A的化学式为___________ 。
②反应Ⅰ、Ⅱ、Ⅲ中,有___________ 个属于氧化还原反应。
③反应Ⅰ中氧化剂与还原剂的物质的量之比为___________ 。

回答下列问题:
(1)X的名称为
(2)Y的氧化物属于
(3)常用
 溶液作为刻制印刷电路时的“腐蚀液”、该反应的离子方程式为
溶液作为刻制印刷电路时的“腐蚀液”、该反应的离子方程式为(4)由粗硅制备硅烷(
 )的基本流程如下图所示(反应条件均省略):
)的基本流程如下图所示(反应条件均省略):
已知:反应Ⅰ、Ⅱ的化学方程式分别为
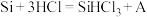 ,
,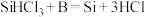 (均已配平)。
(均已配平)。①A的化学式为
②反应Ⅰ、Ⅱ、Ⅲ中,有
③反应Ⅰ中氧化剂与还原剂的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】碳和硅是ⅣA族的重要元素,碳可形成多种化合物,硅是信息时代的基石,下面是有关的化合物及其转化。
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
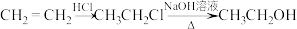
(1)乙烯的电子式为______ ,根据碳氧原子成键特点写出乙醇同分异构体的结构简式______ 。
(2)第二步是取代反应,写出该反应的化学方程式______ 。
Ⅱ. 高温(1100℃)还原
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
已知: 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸______ ,C中发生的反应为______ 。
(4)该装置存在的缺陷是______ 。
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳______ 硅(填“>”或“<”),下列能说明上述规律的是______ 。
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:
d.石灰石和石英高温制玻璃:
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
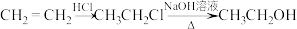
(1)乙烯的电子式为
(2)第二步是取代反应,写出该反应的化学方程式
Ⅱ.
 高温(1100℃)还原
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)已知:
 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸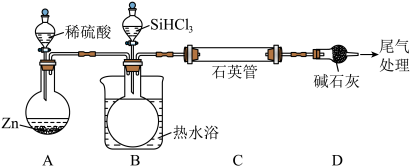
(4)该装置存在的缺陷是
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:

d.石灰石和石英高温制玻璃:

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下表为元素周期表的一部分。回答下列问题:
(1)表中元素原子半径最小的是(写元素符号)_______ 。
(2)Y元素在周期表中的位置为_______ 。
(3)硫的气态氢化物的电子式为_______ ,其水溶液在空气中放置易变浑浊,该变化说明硫的非金属性比氧_______ (填“强”或“弱”)
(4)25℃,两种酸的电离平衡常数如下表。
①HSO 的电离平衡常数表达式K=
的电离平衡常数表达式K=_______ 。
②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_______ 。
| 碳 | 氮 | Y | M |
| X | 硫 | Z |
(1)表中元素原子半径最小的是(写元素符号)
(2)Y元素在周期表中的位置为
(3)硫的气态氢化物的电子式为
(4)25℃,两种酸的电离平衡常数如下表。
| Ka1 | Ka2 | |
| H2SO3 | 1.3×10-2 | 6.3×10-8 |
| H2CO3 | 4.2×10-7 | 5.6×10-11 |
①HSO
 的电离平衡常数表达式K=
的电离平衡常数表达式K=②H2SO3溶液和NaHCO3溶液反应的主要离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】元素在周期表中的位置,反映了元素的原子结构和性质。下图是元素周期表的一部分,请按要求回答下列问题。
(1)元素⑤位于周期表中的第___________ 周期第___________ 族。
(2)④⑥两种元素形成的化合物可用作防腐剂,常用于腌制食物,该化合物的电子式为______ ,高温灼烧该化合物时,火焰呈________ 色。
(3)①②③三种元素中,原子半径最小的是___________ (填元素符号)。
(4)④⑦两种元素最高价氧化物对应的水化物碱性较强的是___________ (填化学式)。
(5)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,请写出该反应的化学方程式_____ 。
| He | |||||||||||||||||
| ① | ② | ③ | Ne | ||||||||||||||
| ④ | ⑤ | ⑥ | Ar | ||||||||||||||
| ⑦ | Kr |
(2)④⑥两种元素形成的化合物可用作防腐剂,常用于腌制食物,该化合物的电子式为
(3)①②③三种元素中,原子半径最小的是
(4)④⑦两种元素最高价氧化物对应的水化物碱性较强的是
(5)①⑥两种元素的简单氢化物相遇会迅速反应,产生大量白烟,请写出该反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】如表为元素周期表的一部分,标出了A—K共十种元素所在位置。请用元素符号或化学式 回答下列问题.
(1)10种元素中,化学性质最不活泼的是______ ,最活泼的金属是_____ 。
(2)C、E、F三种元素形成的简单离子半径最小的是_______ 。
(3)C、K形成的化合物中化学键的类型属于________ ,灼烧时火焰焰色为______ 。
(4)化合物C2B2的电子式为__________________ ;该化合物和AB2反应的化学方程式为__________________________________________ 。
(5)E的最高价氧化物属于________________ 性氧化物,它与氢氧化钠溶液反应的离子方程式为____________________________________________ 。
(6)D的单质在A、B形成化合物中燃烧的化学方程式为________________________ 。
(7)用电子式表示H与B组成的H2B型化合物的形成过程:_____________________ 。
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | A | B | ||||||
| 3 | C | D | E | F | G | |||
| 4 | H | I | K |
(1)10种元素中,化学性质最不活泼的是
(2)C、E、F三种元素形成的简单离子半径最小的是
(3)C、K形成的化合物中化学键的类型属于
(4)化合物C2B2的电子式为
(5)E的最高价氧化物属于
(6)D的单质在A、B形成化合物中燃烧的化学方程式为
(7)用电子式表示H与B组成的H2B型化合物的形成过程:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是___________ (填化学式)。
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因___________ 。
(3)工业上可利用水玻璃( )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式___________ 。
(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置___________ 。
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是___________ (填序号)。
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性: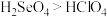
(1)可用于制作计算机芯片和太阳能电池的是
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因
(3)工业上可利用水玻璃(
 )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性:
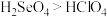
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】A、B、C、D、E、F均为短周期主族元素,且原子序数依次增大。短周期元素中C的原子半径最大,B、E同族,E的最外层电子数是电子层数的2倍,A的最高价氧化物水化物为H2AO3,D是地壳中含量最高的金属元素。
(1)A的元素符号是_______ ,C2B2的电子式为_______ 。
(2)B、C、D、F的离子半径由大到小的顺序是_______ (用离子符号表示)。
(3)E和F相比,非金属性强的是_______ (用元素符号表示),下列事实能证明这一结论的是_______ (用符号填空)。
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为_______ (填化学式)。
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为_________________________ 。
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为_______ , pH=10的乙溶液中由水电离产生的c(OH-)=_______ mol·L-1。
(1)A的元素符号是
(2)B、C、D、F的离子半径由大到小的顺序是
(3)E和F相比,非金属性强的是
①常温下E的单质呈固态,F的单质呈气态 ②气态氢化物的稳定性:F>E ③E和F形成的化合物中,E显正价 ④F单质能与E的氢化物发生置换反应 ⑤E和F的氧化物的水化物的酸性强弱 ⑥气态氢化物的还原性:E>F
(4)把CDB2溶液蒸干所得的固体物质为
(5)C和F可组成化合物甲,用惰性电极电解甲的水溶液,电解的化学方程式为
(6)A、B、C三种元素组成的常见化合物乙的溶液中,离子浓度由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)⑧的最高价氧化物的水化物的化学式是___________ 。
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序___________ (写离子符号)。
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是___________ (填化学式)。
(4)⑤和③的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(5)下列事实能判断⑤和⑥的金属性强弱的是___________ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是___________ 。
a. 只具有还原性
只具有还原性
b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比 强
强
(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为___________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是
(4)⑤和③的最高价氧化物的水化物之间发生反应的离子方程式为
(5)下列事实能判断⑤和⑥的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是
a.
 只具有还原性
只具有还原性 b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比
 强
强(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为
您最近一年使用:0次



