碳和硅是ⅣA族的重要元素,碳可形成多种化合物,硅是信息时代的基石,下面是有关的化合物及其转化。
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
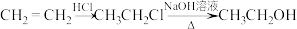
(1)乙烯的电子式为______ ,根据碳氧原子成键特点写出乙醇同分异构体的结构简式______ 。
(2)第二步是取代反应,写出该反应的化学方程式______ 。
Ⅱ. 高温(1100℃)还原
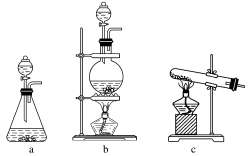
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
已知: 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸______ ,C中发生的反应为______ 。
(4)该装置存在的缺陷是______ 。
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳______ 硅(填“>”或“<”),下列能说明上述规律的是______ 。
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:
d.石灰石和石英高温制玻璃:
Ⅰ.乙烯是基本的化工原料,合成乙醇的路线如图
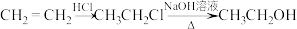
(1)乙烯的电子式为
(2)第二步是取代反应,写出该反应的化学方程式
Ⅱ.
 高温(1100℃)还原
高温(1100℃)还原 可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)
可得到高纯硅,实验室用下列装置模拟该过程(部分加热装置省略)已知:
 沸点33℃,遇水剧烈反应生成硅酸
沸点33℃,遇水剧烈反应生成硅酸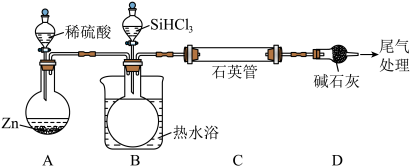
(4)该装置存在的缺陷是
(5)碳硅位于同一主族,根据同主族元素递变规律,非金属性碳
a.焦炭与石英砂高温反应制取粗硅;
b.二氧化碳通入水玻璃产生白色沉淀
c.碳化硅与浓强碱发生非氧化还原反应:

d.石灰石和石英高温制玻璃:

更新时间:2024-05-09 17:55:11
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】钠元素在自然界中普遍存在。
(1)画出钠的原子结构示意图___________ ,根据原子结构示意图,钠具有___________ (填“氧化性”或“还原性”)
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
(3)写出钠与水反应的化学方程式:___________ 。
(4)金属钠着火时用___________进行灭火
(1)画出钠的原子结构示意图
(2)钠与水反应的实验现象的原因有:
A.钠与水界面各部分产生H2的量不同,所受推力不均匀;
B.钠的密度比水小;
C.钠与水反应放热,使熔点低的钠熔化成小球;
D.钠不断与水反应,直到反应完全;
E.生成的氢氧化钠使酚酞试液变红。
请在下发填写。描述的现象相对应的原因。
| 实验现象 | 原因(填以上序号) |
| 钠浮在水面上 | |
| 熔成闪亮的小球 | |
| 小球向各个方向迅速游动,并发出“嘶嘶”的声音 | |
| 小球逐渐变小以后完全消失 | |
| 在反应后的溶液中滴入酚酞试液显红色 |
(3)写出钠与水反应的化学方程式:
(4)金属钠着火时用___________进行灭火
| A.水 | B.泡沫灭火器 | C.干粉灭火器 | D.干燥的沙土 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题:
(1)写出 的电子式:
的电子式:_______ ,它的阳离子价层电子对数为_______ 。
(2)Cu的基态原子结构示意图为_______ ,Cu的价层电子排布图为_______ , 的价层电子排布式为
的价层电子排布式为_______ , 和
和 较稳定的是
较稳定的是_______ (填离子符号),原因是_______ 。
(3)乙炔和乙烯分子,它们的 键个数之比为
键个数之比为_______ ,乙烯分子中C原子杂化轨道类型为_______ 。
(1)写出
 的电子式:
的电子式:(2)Cu的基态原子结构示意图为
 的价层电子排布式为
的价层电子排布式为 和
和 较稳定的是
较稳定的是(3)乙炔和乙烯分子,它们的
 键个数之比为
键个数之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】物质的类别和核心元素的化合价是研究物质性质的两个基本视角。

(1)Y的分子式________ 。
(2)图中X的电子式为_________ ;其水溶液长期在空气中放置容易变浑浊,原因是______________________ (用化学方程式表示)。该变化体现出:S非金属性比O__________ (填“强”或“弱”)。用原子结构解释原因:同主族元素最外层电子数相同,从上到下,__________ ,得电子能力逐渐减弱。
(3) Z与图表中某物质反应生成SO2的化学方程式_____________________________ 。

(1)Y的分子式
(2)图中X的电子式为
(3) Z与图表中某物质反应生成SO2的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】硅藻土由无定形的SiO2组成,含有少量Fe2O3、Al2O3及有机物等杂质。工业上按以下流程用硅藻土制备纳米二氧化硅。

(1)煅烧硅藻土的目的是__ 。
(2)在加热条件下加入烧碱时反应的化学方程式为__ 。
(3)加入过量硫酸后生成胶体的反应方程式为_________ 。

(1)煅烧硅藻土的目的是
(2)在加热条件下加入烧碱时反应的化学方程式为
(3)加入过量硫酸后生成胶体的反应方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】晶体硅是信息科学和能源科学中的一种重要材料,可用于制芯片和太阳能电池等。如图所示流程是工业上制取纯硅的一种方法。

请回答下列问题:
(1)在上述生产过程中,属于置换反应的有___________ (填标号)。
(2)写出反应①的化学方程式:___________ 。
(3)化合物W的用途很广,可用于制备硅胶和木材防火剂等,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至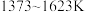 反应,可生成化合物W,其化学方程式是
反应,可生成化合物W,其化学方程式是_____ 。
(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是_____ (填化学式)。

请回答下列问题:
(1)在上述生产过程中,属于置换反应的有
(2)写出反应①的化学方程式:
(3)化合物W的用途很广,可用于制备硅胶和木材防火剂等,可作肥皂的填充剂,是天然水的软化剂。将石英砂和纯碱按一定比例混合加热至
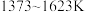 反应,可生成化合物W,其化学方程式是
反应,可生成化合物W,其化学方程式是(4)A、B、C三种气体在“节能减排”中作为减排目标的一种气体是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】硅是无机非金属材料的主角,硅的氧化物和硅酸盐占地壳的90%以上。
(1)下列不属于硅酸盐的是_______ 。
A.碳化硅陶瓷 B.黏土 C.玻璃 D. 石英
B.黏土 C.玻璃 D. 石英
(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为:8Na+CCl4+SiCl4=SiC+8NaCl,其中氧化剂为______ 。
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可以用作______ ;Na2SiO3可通过SiO2与纯碱混合高温下反应制得,反应时可以采用的坩埚为______ (填字母)。
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D. 铁坩埚
(4)制备纯硅的生产过程为如图:
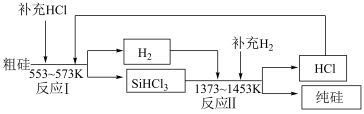
假设每一轮次制备1mol纯硅,生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比为______ 。
(1)下列不属于硅酸盐的是
A.碳化硅陶瓷
 B.黏土 C.玻璃 D. 石英
B.黏土 C.玻璃 D. 石英(2)科学家用金属钠、四氯化碳和四氯化硅制得了碳化硅纳米棒,反应的化学方程式为:8Na+CCl4+SiCl4=SiC+8NaCl,其中氧化剂为
(3)用Na2SiO3水溶液浸泡过的棉花不易燃烧,说明Na2SiO3可以用作
A.普通玻璃坩埚 B.石英玻璃坩埚 C.氧化铝坩埚 D. 铁坩埚
(4)制备纯硅的生产过程为如图:

假设每一轮次制备1mol纯硅,生产过程中硅元素没有损失,反应I中HCl的利用率为90%,反应Ⅱ中H2的利用率为93.75%。则在第二轮次的生产中,补充投入HCl和H2的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是元素周期表的一部分,请参照元素①~⑤在表中的位置,回答下列问题:
(1)⑧的最高价氧化物的水化物的化学式是___________ 。
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序___________ (写离子符号)。
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是___________ (填化学式)。
(4)⑤和③的最高价氧化物的水化物之间发生反应的离子方程式为___________ 。
(5)下列事实能判断⑤和⑥的金属性强弱的是___________ (填字母,下同)。
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是___________ 。
a. 只具有还原性
只具有还原性
b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比 强
强
(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为___________ 。
族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ||||
(2)④、⑤、⑥、⑦四种元素的离子半径由大到小排序
(3)元素③、④形成的简单气态氢化物的稳定性中较大的是
(4)⑤和③的最高价氧化物的水化物之间发生反应的离子方程式为
(5)下列事实能判断⑤和⑥的金属性强弱的是
a.常温下单质与水反应置换出氢的难易程度
b.最高价氧化物对应的水化物的碱性强弱
c.相同温度下,最高价氧化物对应的水化物的溶解度大小
(6)硒(Se)位于第四周期,与④同主族。下列推断正确的是
a.
 只具有还原性
只具有还原性 b.Se的最低负化合价是-2价
c.Se的最高价氧化物对应水化物的酸性比
 强
强(7)同温同压下,0.2mol的⑤、⑥、⑦单质分别与100mL1mol/L的盐酸充分反应,产生氢气的体积比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】硅是无机非金属材料的主角,硅的氧化物和硅酸盐约占地壳质量的90%以上。
(1)可用于制作计算机芯片和太阳能电池的是___________ (填化学式)。
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因___________ 。
(3)工业上可利用水玻璃( )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式___________ 。
(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置___________ 。
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是___________ (填序号)。
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性: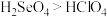
(1)可用于制作计算机芯片和太阳能电池的是
(2)实验室中盛放氢氧化钠溶液的试剂瓶不能用玻璃塞,用化学方程式说明原因
(3)工业上可利用水玻璃(
 )和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式
)和盐酸反应制备硅酸凝胶,进一步脱水处理可得到硅胶,写出水玻璃和盐酸反应的离子方程式(4)门捷列夫预言的“类硅”,多年后被德国化学家文克勒发现。已知主族元素“类硅”的最高化合价为+4价,其最高价氧化物对应的水化物为两性氢氧化物。写出“类硅”在元素周期表中的位置
(5)在元素周期表中,硒(Se)位于第4周期,与O同主族。下列关于Se的推断中,正确的是
①原子的最外层电子数为6
②元素的非金属性:Se>O
③原子半径:Se>S
④最高价氧化物对应的水化物酸性:
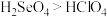
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】最早的全球定位系统(GPS)采取星载铷(Rb)原子钟和星载铯(Cs)原子钟相配合的方式,而较新的全球定位系统(比如北斗和伽利略)则采用星载铷原子钟与星载氢原子钟的组合方案。已知铷、铯的部分信息如表:
回答下列问题:
(1)铯元素在周期表中的位置为_______ 。
(2)Cs、Rb的原子序数之差为_______ 。
(3)碱性:RbOH______ CsOH(填“大于”“小于”或“等于”),判断依据是_______ (从原子结构角度解释)。
(4)相同条件下,铷、铯分别与水反应,较剧烈的是______ (填元素符号)。
(5)铷与水反应的离子方程式为_______ 。
(6)锂与铯位于同主族,氢化锂(LiH)是还原剂和供氢剂。已知Li+、H-的离子半径依次为76pm、205pm,试解释Li+半径小于H-半径的原因:______ 。
元素 | Rb | Cs |
在周期表中的位置 | 第5周期IA族 | |
原子结构示意图 |
|
(1)铯元素在周期表中的位置为
(2)Cs、Rb的原子序数之差为
(3)碱性:RbOH
(4)相同条件下,铷、铯分别与水反应,较剧烈的是
(5)铷与水反应的离子方程式为
(6)锂与铯位于同主族,氢化锂(LiH)是还原剂和供氢剂。已知Li+、H-的离子半径依次为76pm、205pm,试解释Li+半径小于H-半径的原因:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】下图是实验室用二氧化锰和浓盐酸制备氯气并进行一系列相关实验的装置(夹持设备已略)。

(1)该实验中A部分的装置是___________ (填写下列装置的序号)。发生反应的化学方程式是___________ 。
(2)装置B中饱和食盐水的作用是___________ ;同时装置B亦是安全瓶,监测实验进行时C中是否发生堵塞,请写出发生堵塞时B中的现象___________ 。
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入___________ 。
(4)装置F的作用为___________ 。若用NaOH溶液替代Na2SO3溶液,则发生反应的离子方程式为___________ 。

(1)该实验中A部分的装置是

(2)装置B中饱和食盐水的作用是
(3)装置C的实验目的是验证氯气是否具有漂白性,为此C中Ⅰ、Ⅱ、Ⅲ依次放入
| a | b | c | d | |
| Ⅰ | 干燥的有色布条 | 干燥的有色布条 | 湿润的有色布条 | 湿润的有色布条 |
| Ⅱ | 碱石灰 | 无水氯化钙 | 浓硫酸 | 无水氯化钙 |
| Ⅲ | 湿润的有色布条 | 湿润的有色布条 | 干燥的有色布条 | 干燥的有色布条 |
(4)装置F的作用为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】市场销售的某种精制食用盐包装袋上有如下说明:
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O,______________
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应后溶液显酸性,写出该反应的离子方程式:_____________________________ 。
②某同学设计回收四氯化碳的操作步骤如下,请将缺少的操作步骤补充完整。
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3溶液
c.____________________ d.分离出下层液体。
(3)已知:I2+2S2O32=2I-+S4O62-。某质量检验监督局测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,以6.0×10-4mol·L-1的Na2S2O3标准溶液滴定,消耗20.00mL标准液。
①判断c中滴定反应恰好完全的现象是_____________________ 。
②根据以上实验和包装袋说明,所测精制盐的碘含量是____ mg/kg。
(4)用惰性电极电解KI溶液可制备碘酸钾,则阳极反应式为_____________________ 。
| 产品标准 | GB5461 |
| 产品等级 | 一级 |
| 配料 | 食盐、碘酸钾、抗结剂 |
| 碘含量(以I计) | 20~50mg/kg |
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处)
KIO3+ KI+ H2SO4= K2SO4+ I2+ H2O,
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应后溶液显酸性,写出该反应的离子方程式:
②某同学设计回收四氯化碳的操作步骤如下,请将缺少的操作步骤补充完整。
a.将碘的四氯化碳溶液置于分液漏斗中; b.加入适量Na2SO3溶液
c.
(3)已知:I2+2S2O32=2I-+S4O62-。某质量检验监督局测定食用精制盐的碘含量,其步骤为:
a.准确称取12.7g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉为指示剂,以6.0×10-4mol·L-1的Na2S2O3标准溶液滴定,消耗20.00mL标准液。
①判断c中滴定反应恰好完全的现象是
②根据以上实验和包装袋说明,所测精制盐的碘含量是
(4)用惰性电极电解KI溶液可制备碘酸钾,则阳极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】实验室利用下列装置制氯气,请填空:

①制氯气的反应原理,请用化学方程式表示:______________ 。
②饱和食盐水的作用是_________________________________________________ 。
③浓硫酸的作用是_________________________________________________ 。
④氢氧化钠的作用是_________________________________________________ 。
⑤向上排空气法收集氯气的理由是_________________________________________________ 。

①制氯气的反应原理,请用化学方程式表示:
②饱和食盐水的作用是
③浓硫酸的作用是
④氢氧化钠的作用是
⑤向上排空气法收集氯气的理由是
您最近一年使用:0次




