某温度下,在一个 的密闭容器中,
的密闭容器中, 、
、 、
、 三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白: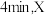 的平均反应速率为
的平均反应速率为___________ 。
(2)该反应的化学方程式为___________ 。
(3) 时,
时,
___________ 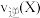 (填“
(填“ ”、“
”、“ ”或“
”或“ ”下同),
”下同), 时,转化率
时,转化率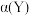
___________  。
。
(4)若 时向容器中通入氩气(容器体积不变),
时向容器中通入氩气(容器体积不变), 的化学反应速率将
的化学反应速率将___________ (填“增大”、“减小”或“不变”。下同), 时,压缩容器体积,反应速率会
时,压缩容器体积,反应速率会___________ 。
(5)若 均为气体(容器体积不变),下列能说明反应已达平衡的是___________。
均为气体(容器体积不变),下列能说明反应已达平衡的是___________。
(6)某合成氨速率方程为: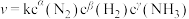 ,根据表中数据,
,根据表中数据,
___________ ;
 的密闭容器中,
的密闭容器中, 、
、 、
、 三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白:
三种气体的物质的量随时间的变化曲线如图所示。根据图中数据,填写下列空白: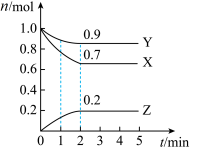
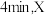 的平均反应速率为
的平均反应速率为(2)该反应的化学方程式为
(3)
 时,
时,
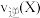 (填“
(填“ ”、“
”、“ ”或“
”或“ ”下同),
”下同), 时,转化率
时,转化率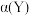
 。
。(4)若
 时向容器中通入氩气(容器体积不变),
时向容器中通入氩气(容器体积不变), 的化学反应速率将
的化学反应速率将 时,压缩容器体积,反应速率会
时,压缩容器体积,反应速率会(5)若
 均为气体(容器体积不变),下列能说明反应已达平衡的是___________。
均为气体(容器体积不变),下列能说明反应已达平衡的是___________。A. 三种气体的浓度相等 三种气体的浓度相等 |
B. 气体的体积分数不随时间变化 气体的体积分数不随时间变化 |
| C.混合气体的总压强不随时间变化 |
D.反应速率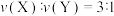 |
(6)某合成氨速率方程为:
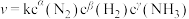 ,根据表中数据,
,根据表中数据,
| 实验 | 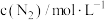 | 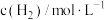 |  |  |
| 1 |  |  |  | 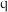 |
| 2 |  |  |  | 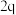 |
| 3 |  |  |  | 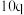 |
| 4 |  |  |  | 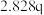 |
更新时间:2024-04-26 10:38:57
|
相似题推荐
【推荐1】工业生产中常常产生硫的氧化物和氮的氧化物,对环境产生重大影响,为减少对环境的污染,科学工作者采用“O3氧化法”和“光催化氧化法”对工业烟气脱硫、脱硝,原理如下。回答下列问题:
I.O3氧化法
(1)用O3氧化烟气中的SO2时,体系中存在以下反应:
a)SO2(g)+O3(g)⇌SO3(g)+O2(g) △H1=-241.6kJ/mol K1
b)2O3(g)⇌3O2(g) △H2=-286.6kJ/mol K2
c)2SO2(g)+O2(g)⇌2SO3(g) △H3 K3
根据盖斯定律,△H3=_______ ,K3=_______ (用含K1、K2的式子表示)。
(2)在密闭容器中充入1molN2O4和1molO3,发生以下反应:
d)N2O4(g)⇌2NO2(g) △H4=+57kJ/mol
e)N2O4(g)+O3(g)⇌N2O5(g)+O2(g) △H5
不同压强(P)下,N2O4平衡转化率α(N2O4)随反应温度(T)的变化关系如图1所示。_______ 0(填“>”或“<”),若缩小体积增大压强,B点可能向_______ 点移动(填“A”或“C”)。
②下列有关该反应体系的说法正确的是_______ (填标号)。
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在n(NO2)+n(N2O4)+n(N2O5)>1mol
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大N2O4的浓度,反应d的正反应速率增大,e的正反应速率减小
③某温度下,t分钟后达到平衡,此时N2O4的物质的量分数为1/3,且NO2与O2的物质的量分数相等,v(O2)=_______ mol/min
Ⅱ.光催化氧化法
光照条件下,催化剂TiO2表面产生电子(e-)和空穴(h+)。电子与O2作用生成离子自由基(·O ),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO
),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO 。变化过程如图2所示。
。变化过程如图2所示。_______ 。
(4)已知该过程中生成的HNO2可继续与·OH发生反应:HNO2+2·OH=H++NO +H2O;该反应可分两步进行,请补充反应i:
+H2O;该反应可分两步进行,请补充反应i:
i:_______ ;
ii.NO2+·OH=H++NO 。
。
I.O3氧化法
(1)用O3氧化烟气中的SO2时,体系中存在以下反应:
a)SO2(g)+O3(g)⇌SO3(g)+O2(g) △H1=-241.6kJ/mol K1
b)2O3(g)⇌3O2(g) △H2=-286.6kJ/mol K2
c)2SO2(g)+O2(g)⇌2SO3(g) △H3 K3
根据盖斯定律,△H3=
(2)在密闭容器中充入1molN2O4和1molO3,发生以下反应:
d)N2O4(g)⇌2NO2(g) △H4=+57kJ/mol
e)N2O4(g)+O3(g)⇌N2O5(g)+O2(g) △H5
不同压强(P)下,N2O4平衡转化率α(N2O4)随反应温度(T)的变化关系如图1所示。

②下列有关该反应体系的说法正确的是
A.恒压下,混合气体的密度保持不变时,说明反应体系已达到平衡
B.任意时刻,存在n(NO2)+n(N2O4)+n(N2O5)>1mol
C.恒容下,升高温度,该体系中气体颜色变浅
D.恒容下,增大N2O4的浓度,反应d的正反应速率增大,e的正反应速率减小
③某温度下,t分钟后达到平衡,此时N2O4的物质的量分数为1/3,且NO2与O2的物质的量分数相等,v(O2)=
Ⅱ.光催化氧化法
光照条件下,催化剂TiO2表面产生电子(e-)和空穴(h+)。电子与O2作用生成离子自由基(·O
 ),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO
),空穴与水电离出的OH-作用生成羟基自由基(·OH),·O-和·OH分别与NO反应生成NO 。变化过程如图2所示。
。变化过程如图2所示。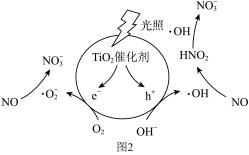
(4)已知该过程中生成的HNO2可继续与·OH发生反应:HNO2+2·OH=H++NO
 +H2O;该反应可分两步进行,请补充反应i:
+H2O;该反应可分两步进行,请补充反应i:i:
ii.NO2+·OH=H++NO
 。
。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】恒温下,将amolN2与bmolH2的混合气体通入一个2L的密闭容器中合成氨,当反应进行到5s时,有0.1molNH3生成,并且放出4.62kJ的热量。
(1)0~5s用H2表示该反应的平均反应速率v(H2)=____ mol·L-1·s-1。
(2)写出合成氨反应的热化学方程式:____ 。
(3)反应达平衡时n(N2)=3mol,n(H2)=8mol,n(NH3)=6mol。
①a=___ mol,b=____ mol平衡时N2的转化率为____ 。
②有人设想以N2和H2为反应物,以溶有NH4Cl的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氨的新型燃料电池,装置如图所示,写出该电池正极的电极方程式:____ 。

(1)0~5s用H2表示该反应的平均反应速率v(H2)=
(2)写出合成氨反应的热化学方程式:
(3)反应达平衡时n(N2)=3mol,n(H2)=8mol,n(NH3)=6mol。
①a=
②有人设想以N2和H2为反应物,以溶有NH4Cl的稀盐酸为电解质溶液,可制造出既能提供电能,又能固氨的新型燃料电池,装置如图所示,写出该电池正极的电极方程式:

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】学习小组利用草酸 溶液与
溶液与 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
已知:
回答下列问题:
(1)通过实验①、②,可探究_____ 的改变对化学反应速率的影响,其中
_____ ,
_____ 。
(2)通过实验_____ (填实验序号)可探究 变化对化学反应速率的影响,由此可以得出的实验结论是
变化对化学反应速率的影响,由此可以得出的实验结论是_____ 。
(3)实验③中, 内
内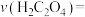
_____ (忽略溶液体积的变化,结果保留小数点后两位)。
(4)草酸溶液与酸性高锰酸钾溶液反应机理如图所示。 反应的离子方程式为
反应的离子方程式为_____ ;为验证催化剂对反应速率的影响,实验⑤中试剂 最好选用
最好选用_____ (填序号)。
a.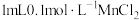 溶液
溶液
b. 溶液
溶液
c. 粉末
粉末
d. 粉末
粉末
 溶液与
溶液与 溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:
溶液的反应探究“外界条件的改变对化学反应速率的影响”,进行如下实验:| 实验序号 | 试验温度/K | 有关物质 | 紫色褪去所需时间 | ||||
  溶液 溶液 |   溶液 溶液 |   溶液 溶液 |  | 试剂X | |||
 |  |  |  | ||||
| ① | 298 | 2 | 4 | 1 | 1 | 无 |  |
| ② |  | 2 | 3 | 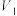 |  | 无 |  |
| ③ | 313 | 2 | 4 | 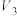 | 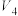 | 无 | 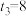 |
| ④ | 313 | 2 | 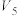 | 2 |  | 无 | 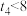 |
| ⑤ | 313 | 2 | 4 | 1 | 1 | 有 | 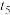 |

回答下列问题:
(1)通过实验①、②,可探究


(2)通过实验
 变化对化学反应速率的影响,由此可以得出的实验结论是
变化对化学反应速率的影响,由此可以得出的实验结论是(3)实验③中,
 内
内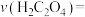
(4)草酸溶液与酸性高锰酸钾溶液反应机理如图所示。
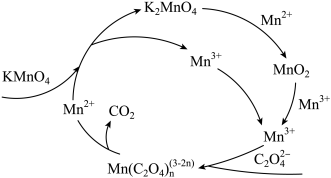
 反应的离子方程式为
反应的离子方程式为 最好选用
最好选用a.
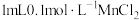 溶液
溶液b.
 溶液
溶液c.
 粉末
粉末d.
 粉末
粉末
您最近一年使用:0次
【推荐1】减少温室气体的排放对环境和社会都具有重要的意义。CH4- CO2催化重整反应的化学方程式为CH4(g)+ CO2(g)⇌2CO(g) + 2H2(g) ΔH。回答下列问题:
(1)已知:①CH4(g)+2O2(g)⇌CO2(g) +2H2O(g) ΔH1= -890.3 kJ·mol-1;
②2CO(g)+ O2(g)⇌2CO2(g) ΔH2= -566 kJ·mol-1;
③2H2(g)+ O2(g)⇌2H2O(g) ΔH3= -483.6 kJ·mol-1;
则上述催化重整反应的ΔH =___________ kJ·mol-1。
(2)恒容密闭容器中反应CH4(g)+ CO2(g) ⇌2CO(g)+ 2H2(g)达到平衡状态的标志是___________(填选项标号)
(3)容器容积为1 L,控制CH4和CO2初始投料量分别为2 mol和3 mol,发生CH4-CO2催化重整反应,甲烷的平衡转化率与温度、压强的关系如图所示。

①X、L代表温度或压强,则X代表___________ (填“温度”或“压强”);L1___________ (填“>”或“<”) L2,并说出理由___________ 。
②计算b点反应的平衡常数K=___________ 。
③当温度为T1°C时,K=100,实验测得v正= k正 c(CH4)·c(CO2),v逆=k逆c2(CO)·c2(H2),k正、k逆为速率常数。T1°C时,k正___________ (用k逆表示)。当温度改变为T2°C时,k正= l05 k逆,则T2°C时平衡压强___________ (填“>” 或“<”) T1°C时平衡压强。
(1)已知:①CH4(g)+2O2(g)⇌CO2(g) +2H2O(g) ΔH1= -890.3 kJ·mol-1;
②2CO(g)+ O2(g)⇌2CO2(g) ΔH2= -566 kJ·mol-1;
③2H2(g)+ O2(g)⇌2H2O(g) ΔH3= -483.6 kJ·mol-1;
则上述催化重整反应的ΔH =
(2)恒容密闭容器中反应CH4(g)+ CO2(g) ⇌2CO(g)+ 2H2(g)达到平衡状态的标志是___________(填选项标号)
| A.单位时间内生成1 mol CH4的同时消耗2 mol CO |
| B.混合气体的密度不再改变 |
| C.反应速率v(CH4):v(CO2):v(CO):v(H2)=1:1:2:2 |
| D.混合气体的平均相对分子质量不再改变 |

①X、L代表温度或压强,则X代表
②计算b点反应的平衡常数K=
③当温度为T1°C时,K=100,实验测得v正= k正 c(CH4)·c(CO2),v逆=k逆c2(CO)·c2(H2),k正、k逆为速率常数。T1°C时,k正
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】氨在国民经济中占有重要地位。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2kJ热量。
①工业合成氨的热化学方程式是___________ 。
②若起始时向容器内放入2 mol N2和6 mol H2,达平衡时放出的热量为Q,则Q(填“>”“<”或“=”)___________ 184.4kJ。
③已知:

1 mol N-H键断裂吸收的能量等于___________ kJ。
④理论上,为了增大平衡时H2的转化率,可采取的措施是___________ (填序号)。
a. 增大压强 b. 使用合适的催化剂
c. 升高温度 d. 及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g) CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的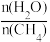 恒定时,温度、压强对平衡混合气中CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如下图所示:
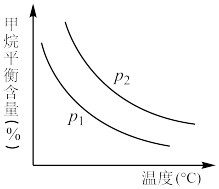
上图中两条曲线表示的压强的关系是:p1___________ p2(填“>”“=”或“<”)。
(3)原料气H2还可通过反应CO(g)+H2O(g) CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。
①T℃时,向容积固定为5L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则该温度下反应的平衡常数K为___________ 。
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是___________ (填序号)。
a. 混合气体的平均相对分子质量不随时间改变
b. 混合气体的密度不随时间改变
c. 单位时间内生成a mol CO2的同时消耗a mol H2
d. 混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
(4)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3(g)+CO2(g) CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
①焓变△H(填“>”“<”或“=”)___________ 0。
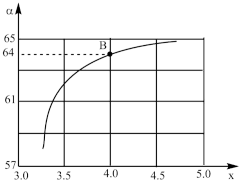
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比) =x,下图是氨碳比(x)与CO2平衡转化率(
=x,下图是氨碳比(x)与CO2平衡转化率( :%)的关系。下图中的B点处,NH3的平衡转化率为
:%)的关系。下图中的B点处,NH3的平衡转化率为___________ 。
(1)合成氨工业中,合成塔中每产生2 mol NH3,放出92.2kJ热量。
①工业合成氨的热化学方程式是
②若起始时向容器内放入2 mol N2和6 mol H2,达平衡时放出的热量为Q,则Q(填“>”“<”或“=”)
③已知:

1 mol N-H键断裂吸收的能量等于
④理论上,为了增大平衡时H2的转化率,可采取的措施是
a. 增大压强 b. 使用合适的催化剂
c. 升高温度 d. 及时分离出产物中的NH3
(2)原料气H2可通过反应CH4(g)+H2O(g)
 CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的
CO(g)+3H2(g)获取,已知该反应中,当初始混合气中的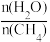 恒定时,温度、压强对平衡混合气中CH4含量的影响如下图所示:
恒定时,温度、压强对平衡混合气中CH4含量的影响如下图所示:
上图中两条曲线表示的压强的关系是:p1
(3)原料气H2还可通过反应CO(g)+H2O(g)
 CO2(g)+H2(g)获取。
CO2(g)+H2(g)获取。①T℃时,向容积固定为5L的容器中充入1 mol水蒸气和1 mol CO,反应达平衡后,测得CO的浓度为0.08mol•L-1,则该温度下反应的平衡常数K为
②保持温度仍为T℃,改变水蒸气和CO的初始物质的量之比,充入容器进行反应,下列描述能够说明体系处于平衡状态的是
a. 混合气体的平均相对分子质量不随时间改变
b. 混合气体的密度不随时间改变
c. 单位时间内生成a mol CO2的同时消耗a mol H2
d. 混合气中n(CO):n(H2O):n(CO2):n(H2)=1:16:6:6
(4)工业上以NH3和CO2为原料合成尿素[CO(NH2)2],反应的化学方程式为2NH3(g)+CO2(g)
 CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:
CO(NH2)2(1)+H2O(1),该反应的平衡常数和温度关系如下:| T/℃ | 165 | 175 | 185 | 195 |
| K | 111.9 | 74.1 | 50.6 | 34.8 |
②在一定温度和压强下,若原料气中的NH3和CO2的物质的量之比(氨碳比)
 =x,下图是氨碳比(x)与CO2平衡转化率(
=x,下图是氨碳比(x)与CO2平衡转化率( :%)的关系。下图中的B点处,NH3的平衡转化率为
:%)的关系。下图中的B点处,NH3的平衡转化率为
您最近一年使用:0次
【推荐3】工业上常用CO2和NH3通过如下反应合成尿素[CO(NH2)2]。在尿素合成塔中的主要反应有:
反应I: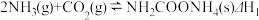
反应II: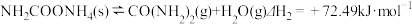
反应III(总反应):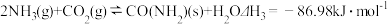
回答下列问题:
(1)∆H1=______ kJ●mol-1,在_______ (填“高温”或“低温”)情况下有利于反应II的自发进行。
(2)一定温度下,在恒容密闭容器中n(NH3):n(CO2)=2:1进行反应I,下列能说明反应I达到了平衡状态的是_________ (填标号)。
A.混合气体的平均相对分子质量不再变化 B.容器内气体总压强不再变化
C.NH3与CO2的转化率相等 D.容器内混合气体的密度不再变化
(3)t°C时,向容积恒定为2 L的密闭容器中加入0.40 mol NH3和0.10 mol CO2 ,发生反应,70min时达到平衡。反应中CO2的物质的量随时间的变化如表所示:
①30 min时CO2的转化率为______________________ 。
②t°C,该反应的平衡常数K=__________ L2●mol-1(列出计算式)。
③在100min时,保持其他条件不变,再向容器中充入0.20 mol NH3和0.050 molCO2,重新建立平衡后CO2的转化率与原平衡相比将_________ (填“增大”“减小”或“不变”)。
④根据表中数据在图中绘制出在t°C下NH3的转化率随时间变化的图象_______ 。
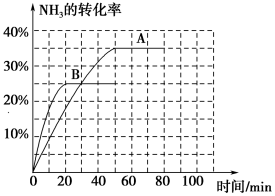
保持其他条件不变,则在(t+ 30)°C下,NH3的转化率随时间变化的正确图象可能是图中的曲线______ (填“A”或“B”)。
反应I:
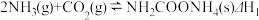
反应II:
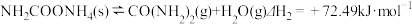
反应III(总反应):
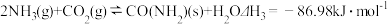
回答下列问题:
(1)∆H1=
(2)一定温度下,在恒容密闭容器中n(NH3):n(CO2)=2:1进行反应I,下列能说明反应I达到了平衡状态的是
A.混合气体的平均相对分子质量不再变化 B.容器内气体总压强不再变化
C.NH3与CO2的转化率相等 D.容器内混合气体的密度不再变化
(3)t°C时,向容积恒定为2 L的密闭容器中加入0.40 mol NH3和0.10 mol CO2 ,发生反应,70min时达到平衡。反应中CO2的物质的量随时间的变化如表所示:
| 时间/min | 0 | 30 | 70 | 80 | 100 |
| n(CO2)/mol | 0.10 | 0.060 | 0.040 | 0.040 | 0.040 |
①30 min时CO2的转化率为
②t°C,该反应的平衡常数K=
③在100min时,保持其他条件不变,再向容器中充入0.20 mol NH3和0.050 molCO2,重新建立平衡后CO2的转化率与原平衡相比将
④根据表中数据在图中绘制出在t°C下NH3的转化率随时间变化的图象

保持其他条件不变,则在(t+ 30)°C下,NH3的转化率随时间变化的正确图象可能是图中的曲线
您最近一年使用:0次



