近日,武汉市第十二中学的“化学妙妙屋”社团以黄铁矿FeS2(杂质为石英)为原料,设计了如下工艺流程:
(1)在空气中焙烧黄铁矿的化学方程式为:___________ 。
(2)检验反应Ⅱ所得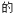 滤液中所含阴离子的方法是
滤液中所含阴离子的方法是___________ 。
(3)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:___________ 、___________ 、过滤、洗涤、干燥。
(4)反应③氢化SiCl4过程中所需的高纯度H2可通过电解精制的饱和食盐水制得,电解过程中同时生成一种黄绿色的气体和一种易溶、易电离的碱,电解反应的离子方程式是___________ 。粗盐水精制过程中,为有效除去 、
、 、
、 等杂质,要按
等杂质,要按___________ 顺序(填标号)加入下列溶液,过滤后再向滤液中加___________ 调节pH。
a.NaOH b.Na2CO3 c.BaCl2
(1)在空气中焙烧黄铁矿的化学方程式为:
(2)检验反应Ⅱ所得
 滤液中所含阴离子的方法是
滤液中所含阴离子的方法是(3)向红渣酸浸得到的滤液中加入适量铁粉还原,再由还原后的滤液制得FeSO4·7H2O的操作为:
(4)反应③氢化SiCl4过程中所需的高纯度H2可通过电解精制的饱和食盐水制得,电解过程中同时生成一种黄绿色的气体和一种易溶、易电离的碱,电解反应的离子方程式是
 、
、 、
、 等杂质,要按
等杂质,要按a.NaOH b.Na2CO3 c.BaCl2
更新时间:2024-04-27 22:10:11
|
相似题推荐
解答题-工业流程题
|
适中
(0.65)
【推荐1】以菱镁矿(主要成分为MgCO3,含少量SiO2、Fe2O3和A12O3)为原料制备高纯镁砂的工艺流程如下:
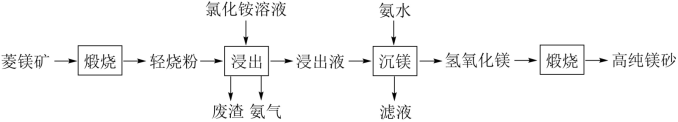
(注:轻烧粉为多种氧化物的混合物)
(1)废渣中除含Fe(OH)3、Al(OH)3外,还有_______ 。
(2)“浸出”时生成Mg2+的离子方程式为_______ 。
(3)已知常温时Ksp[Mg(OH)2]=1.0×10-11,“沉镁”时为了使Mg2+完全沉淀(浓度小于1.0×10-5mol/L),溶液的pH应不低于_______ 。
(4)氢氧化镁煅烧前要洗涤干净,证明其是否洗涤干净的操作为_______ 。
(5)上述流程中可循环使用的物质有_______ (填化学式)。
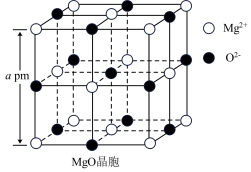
(6)氧化镁形成的一种立方晶胞如图所示。已知晶胞参数为apm,该晶胞中Mg2+的配位数为_______ ,晶体的密度为_______ g/cm3(NA为阿伏加德罗常数的值,用含a和NA的代数式表示)。

(注:轻烧粉为多种氧化物的混合物)
(1)废渣中除含Fe(OH)3、Al(OH)3外,还有
(2)“浸出”时生成Mg2+的离子方程式为
(3)已知常温时Ksp[Mg(OH)2]=1.0×10-11,“沉镁”时为了使Mg2+完全沉淀(浓度小于1.0×10-5mol/L),溶液的pH应不低于
(4)氢氧化镁煅烧前要洗涤干净,证明其是否洗涤干净的操作为
(5)上述流程中可循环使用的物质有
(6)氧化镁形成的一种立方晶胞如图所示。已知晶胞参数为apm,该晶胞中Mg2+的配位数为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以钛铁矿(主要成分为FeTiO3,还含有MgO、CaO、SiO2等杂质)为原料合成锂离子电池的电极材料钛酸锂(Li4Ti5O12)和磷酸亚铁锂(LiFePO4)的工艺流程如图: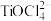 ;富铁液中铁元素主要以Fe2+形式存在;富钛渣中钛元素主要以
;富铁液中铁元素主要以Fe2+形式存在;富钛渣中钛元素主要以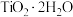 形式存在。
形式存在。
回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是_______ (答1条即可);“溶浸”过程 发生反应的离子方程式为
发生反应的离子方程式为______________ 。
(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为______________ 。
(3)“沉铁”过程发生反应的离子方程式为______________ 。
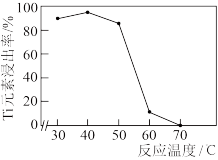
(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:_____________________ 。 为阿伏加德罗常数的值。Ti的价电子排布式为
为阿伏加德罗常数的值。Ti的价电子排布式为______________ ,该晶体的密度
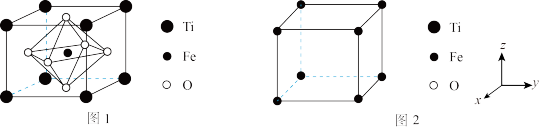
_______ (填含a的计算式)g·cm ;FeTiO3的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
;FeTiO3的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:______________  。
。

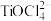 ;富铁液中铁元素主要以Fe2+形式存在;富钛渣中钛元素主要以
;富铁液中铁元素主要以Fe2+形式存在;富钛渣中钛元素主要以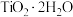 形式存在。
形式存在。回答下列问题:
(1)“溶浸”时为加快浸取速率,可以采取的措施是
 发生反应的离子方程式为
发生反应的离子方程式为(2)若在实验室模拟分离富钛渣和富铁液,则检验富钛渣洗涤干净的操作为
(3)“沉铁”过程发生反应的离子方程式为
(4)“溶钛”过程中Ti元素的浸出率与反应温度的关系如图所示,试分析40℃后Ti元素浸出率呈图像所示变化的原因:
 为阿伏加德罗常数的值。Ti的价电子排布式为
为阿伏加德罗常数的值。Ti的价电子排布式为
 ;FeTiO3的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置:
;FeTiO3的结构的另一种表示如图2(晶胞中未标出Ti、O原子),画出沿z轴向xy平面投影时氧原子在xy平面的位置: 。
。
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐3】某含砷(As)的有毒工业废水经下图流醒转化为粗As2O3,已知:亚砷酸钙微溶于水,砷酸钙难溶于水。

(1)砷是氮的同族元素,且比氮多2个电子层,则AsH3的电子式为_____ 。
(2)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐。H3AsO4转化为Na3AsO4反应的离子方程式为_____ 。
(3)加入试剂1的目的是_____ 。
(4)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有:
A.Ca(OH)2(s)⇌Ca2+(aq)+2OH﹣(aq)△H<0
B.5Ca2++OH﹣+3AsO43﹣⇌Ca5(AsO4)3OH△H>0
资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是_____ 。

(1)砷是氮的同族元素,且比氮多2个电子层,则AsH3的电子式为
(2)“碱浸”的目的是将废水中的H3AsO3和H3AsO4转化为盐。H3AsO4转化为Na3AsO4反应的离子方程式为
(3)加入试剂1的目的是
(4)“沉砷”是将砷元素转化为Ca5(AsO4)3OH沉淀,发生的主要反应有:
A.Ca(OH)2(s)⇌Ca2+(aq)+2OH﹣(aq)△H<0
B.5Ca2++OH﹣+3AsO43﹣⇌Ca5(AsO4)3OH△H>0
资料表明:“沉砷”的最佳温度是85℃,温度高于85℃,随温度升高沉淀率下降,从平衡移动角度分析其原因是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室以CoCl2溶液为原料制备CoCO3,再加热CoCO3的方法制备Co3O4。
(1)CoCO3制备装置如图所示。已知:Ksp[Co(OH)2]=1.6x10-15,Ksp(CoCO3)=1.4x10-13
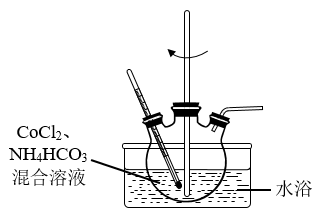
①控制反应温度在60~70℃,搅拌,反应3小时。其反应的离子方程式为_______ 。
②制备CoCO3时不宜用Na2CO3溶液代替NH4HCO3溶液,其原因是_______ 。
③证明CoCO3固体已洗涤干净的实验操作是_______ 。
(2)制备Co3O4.将CoCO3固体在空气中充分灼烧,得到Co3O4固体,反应的化学方程式为_______ 。
(3)测定产品CoCO3中钴的质量分数。采用电位滴定法的实验步骤如下:准确称取6.000g产品溶于盐酸并配成100mL溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入2.000mol-L-1 K3[Fe(CN)6]溶液12.50mL(过量)充分反应后,然后用1.000mol·L-1的Co2+标准溶液电位滴定过量的K3[Fe(CN)6],滴定至终点时消耗Co2+标准溶液15.00mL,则产品中钴的质量分数为_______ 。(写出计算过程)。已知:Co2++[Fe(CN)6]3-=Co3++[Fe(CN)6]4-
(1)CoCO3制备装置如图所示。已知:Ksp[Co(OH)2]=1.6x10-15,Ksp(CoCO3)=1.4x10-13

①控制反应温度在60~70℃,搅拌,反应3小时。其反应的离子方程式为
②制备CoCO3时不宜用Na2CO3溶液代替NH4HCO3溶液,其原因是
③证明CoCO3固体已洗涤干净的实验操作是
(2)制备Co3O4.将CoCO3固体在空气中充分灼烧,得到Co3O4固体,反应的化学方程式为
(3)测定产品CoCO3中钴的质量分数。采用电位滴定法的实验步骤如下:准确称取6.000g产品溶于盐酸并配成100mL溶液;取出20.00mL配得的溶液加入锥形瓶中,向其中加入2.000mol-L-1 K3[Fe(CN)6]溶液12.50mL(过量)充分反应后,然后用1.000mol·L-1的Co2+标准溶液电位滴定过量的K3[Fe(CN)6],滴定至终点时消耗Co2+标准溶液15.00mL,则产品中钴的质量分数为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】某无色溶液中含有K+、Cl-、OH-、SO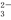 、SO
、SO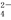 ,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
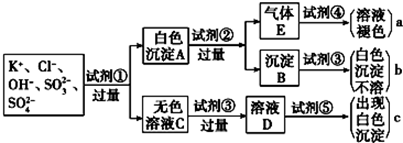
(1)图中试剂①~⑤溶质的化学式分别是
①________ ,②________ ,③________ ,④__________ ,⑤__________ 。
(2)图中现象a、b、c表明检验出的离子分别是a________ 、b________ 、c________ 。
(3)白色沉淀A加试剂②反应的离子方程式_________________ 。
(4)无色溶液C加试剂③的主要目的是_____________________ 。
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是____________________ 。
(6)气体E通入试剂④发生反应的离子方程式是____________________ 。
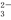 、SO
、SO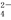 ,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
,为检验溶液中所含的某些阴离子,限用的试剂有:盐酸、硝酸、硝酸银溶液、硝酸钡溶液、溴水和酚酞溶液。检验其中OH-的实验方法省略,检验其他阴离子的过程如下图所示。
(1)图中试剂①~⑤溶质的化学式分别是
①
(2)图中现象a、b、c表明检验出的离子分别是a
(3)白色沉淀A加试剂②反应的离子方程式
(4)无色溶液C加试剂③的主要目的是
(5)白色沉淀A若加试剂③而不加试剂②,对实验的影响是
(6)气体E通入试剂④发生反应的离子方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】实验室有一包白色固体粉末,由Ba(NO3)2、Mg(NO3)2、K2SO4、NaOH、NaCl、CuSO4中的四种物质组成,为确定其成分,进行如下实验:
①取一定量粉末加入水中,振荡,得到白色沉淀和无色滤液;
②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生;
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是___________ ,一定不含有的物质是___________ ,(写化学式)
(2)实验②中发生的离子方程式:___________
(3)为进一步确定白色粉末的组成,向①过滤得到的无色滤液中,加入下列物质,可判断原白色粉末的组成的是___________(填序号)。
①取一定量粉末加入水中,振荡,得到白色沉淀和无色滤液;
②向①的沉淀物中加入足量稀硝酸,白色沉淀完全消失,没有气泡产生;
根据上述实验事实,回答下列问题:
(1)原白色粉末中一定含有的物质是
(2)实验②中发生的离子方程式:
(3)为进一步确定白色粉末的组成,向①过滤得到的无色滤液中,加入下列物质,可判断原白色粉末的组成的是___________(填序号)。
| A.Na2SO4溶液 | B.AgNO3溶液 | C.KCl溶液 | D.BaCl2溶液 |
您最近一年使用:0次



