a.有下列物质:①氢氧化钡 ②KHSO4 ③液态HCl ④稀硫酸 ⑤二氧化碳 ⑥铜 ⑦碳酸钠 ⑧蔗糖
请回答下列问题:
(1)属于电解质的有___________ (填序号)
(2)属于非电解质的有___________ (填序号)
b.某同学用如下实验探究 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:
(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为___________ 。FeCl3溶液,加入1滴___________ 溶液,溶液变___________ 。
(4)FeCl2溶液与氯水反应的化学方程式为___________ 。
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程___________ 。
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量___________ mol。含有O数目___________ 。
(7)100 mL 0.2 mol/L Na2SO4溶液中 的物质的量浓度为
的物质的量浓度为___________ 。
(8)标准状况下11.2 L的CO2的物质的量是___________ mol。
请回答下列问题:
(1)属于电解质的有
(2)属于非电解质的有
b.某同学用如下实验探究
 、
、 的性质。请回答下列问题:
的性质。请回答下列问题:(3)在FeCl3溶液中需加入少量铁屑,发生反应的化学方程式为
(4)FeCl2溶液与氯水反应的化学方程式为
(5)某同学向盛有H2O2溶液的试管中加入几滴酸化的FeCl2溶液,溶液变成棕黄色,发生反应的离子方程
c.请回答下列问题:
(6)0.5 mol H2O含有H的物质的量
(7)100 mL 0.2 mol/L Na2SO4溶液中
 的物质的量浓度为
的物质的量浓度为(8)标准状况下11.2 L的CO2的物质的量是
更新时间:2024-04-29 07:08:16
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】(1)2 mol尿素[CO(NH2)2]含___ 个H原子,所含氧原子跟___ g H2O所含氧原子个数相等。
(2)①标准状况下22.4L CH4;②1.5mol NH3; ③1.806×1024个H2O;④标准状况下73gHCl。所含H原子个数由多到少的顺序是_________________ 。(填序号)
(3)30.9 g Na2R含有Na+ 0.3mol,则Na2R的摩尔质量为______________ 。
(4)标准状况下:① 0.3mol氨气 ②6.02×1022个CO2分子 ③7.3gHCl ④0.2molCH4。
体积最大的是_______ ;密度最大的是_______ ;质量最大的是________ 。(填序号)
(5)相同质量的NO与NO2,其物质的量之比为_________ ,氧元素的质量之比为__________ ,原子总数之比为____________ 。
(2)①标准状况下22.4L CH4;②1.5mol NH3; ③1.806×1024个H2O;④标准状况下73gHCl。所含H原子个数由多到少的顺序是
(3)30.9 g Na2R含有Na+ 0.3mol,则Na2R的摩尔质量为
(4)标准状况下:① 0.3mol氨气 ②6.02×1022个CO2分子 ③7.3gHCl ④0.2molCH4。
体积最大的是
(5)相同质量的NO与NO2,其物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】判断正误。
1.摩尔是表示物质的量多少的基本物理量。_____
2.物质的量就是1mol物质的质量。_____
3.1molH2O中含有2mol氢和1mol氧。_____
4.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。_____
5.1molOH-的质量为17g·moL-1。_____
6.在标准状况下,1mol气体的体积约是22.4L,在非标准状况下,1mol气体的体积一定不是22.4L。_____
7.标准状况下,18gH2O中含2NA个氧原子,体积约为22.4L。_____
8.将58.5gNaCl溶于1L水中配成溶液,所得溶质的物质的量浓度为1mol·L-1。_____
9.胶头滴管取完一种试液后,可直接取另一种不与其反应的试液。_____
10.将固体加入容量瓶中溶解并稀释至刻度线,配制成一定物质的量浓度的溶液。_____
11.蒸发时,应使混合物中的水分完全蒸干后,再停止加热。_____
12.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室。_____
13.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗。_____
14.2mol水的摩尔质量是1mol水的摩尔质量的2倍。_____
1.摩尔是表示物质的量多少的基本物理量。
2.物质的量就是1mol物质的质量。
3.1molH2O中含有2mol氢和1mol氧。
4.分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出。
5.1molOH-的质量为17g·moL-1。
6.在标准状况下,1mol气体的体积约是22.4L,在非标准状况下,1mol气体的体积一定不是22.4L。
7.标准状况下,18gH2O中含2NA个氧原子,体积约为22.4L。
8.将58.5gNaCl溶于1L水中配成溶液,所得溶质的物质的量浓度为1mol·L-1。
9.胶头滴管取完一种试液后,可直接取另一种不与其反应的试液。
10.将固体加入容量瓶中溶解并稀释至刻度线,配制成一定物质的量浓度的溶液。
11.蒸发时,应使混合物中的水分完全蒸干后,再停止加热。
12.实验结束后将所有的废液倒入下水道排出实验室,以免污染实验室。
13.浓硫酸溅到皮肤上时立即用稀氢氧化钠溶液冲洗。
14.2mol水的摩尔质量是1mol水的摩尔质量的2倍。
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】现有以下几种物质:A、熔融状态下的硝酸钾 B、硫酸(H2SO4) C.醋酸(CH3COOH) D、BaSO4固体 E、酒精 F、蔗糖 G、葡萄糖 H、干冰 I、铝
在空格中填写正确的序号。
(1)以上物质中能导电的是____________________ ;
(2)以上物质中属于电解质的是___________________ ;
(3)以上物质中属于非电解质的是____________________ 。
在空格中填写正确的序号。
(1)以上物质中能导电的是
(2)以上物质中属于电解质的是
(3)以上物质中属于非电解质的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有下列五种物质:①CO2;②NH3;③SO2;④H2SO4;⑤NaCl。
(1)其中,能使品红溶液褪色的是_____________ (填序号,下同);
(2)属于电解质的是_____________ ;
(3)只含离子键的是________________ ;
(4)利用下图装置并从B口进气,可收集的气体是___________ 。

(1)其中,能使品红溶液褪色的是
(2)属于电解质的是
(3)只含离子键的是
(4)利用下图装置并从B口进气,可收集的气体是

您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】请运用所学知识,按照要求完成以下填空:
燃料电池具有能量转化率高等优点,工作时从负极连续通入 、①
、① 等燃料,从正极连续通入
等燃料,从正极连续通入 ,二者在电池内部(还有②KOH或③
,二者在电池内部(还有②KOH或③ 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 、④
、④ 或⑤
或⑤ 溶液等,同时产生电能。
溶液等,同时产生电能。
(1)在上述短文标有序号的物质中,属于电解质的是_______ (填序号,下同):属于酸性氧化物的是_______ 。
(2)请写出一种与 互为同素异形的物质
互为同素异形的物质_______ 。
(3)写出上文有序号物质中一种酸的电离方程式_______ 。
(4)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备 胶体的化学反应方程式
胶体的化学反应方程式_______ 。
燃料电池具有能量转化率高等优点,工作时从负极连续通入
 、①
、① 等燃料,从正极连续通入
等燃料,从正极连续通入 ,二者在电池内部(还有②KOH或③
,二者在电池内部(还有②KOH或③ 等物质的溶液)发生反应生成
等物质的溶液)发生反应生成 、④
、④ 或⑤
或⑤ 溶液等,同时产生电能。
溶液等,同时产生电能。(1)在上述短文标有序号的物质中,属于电解质的是
(2)请写出一种与
 互为同素异形的物质
互为同素异形的物质(3)写出上文有序号物质中一种酸的电离方程式
(4)向煮沸的蒸馏水中逐滴加入饱和氯化铁溶液,制备
 胶体的化学反应方程式
胶体的化学反应方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】锰酸锂(LiMn2O4)在电池材料领域有重要用途,可用硫铁矿(主要成分为FeS2)、软锰矿(主要成分为MnO2,含有少量的Fe2O3、Al2O3等杂质)、回收的工业废酸(主要成分为H2SO4)为原料制备,其工业流程如下图所示:

下列关于沉锰制备高纯MnO2的说法中,正确的是_______ (填标号)。
a.若沉锰反应时加入足量浓盐酸并加热,MnO2的产率将降低
b.若沉锰后进行过滤操作,为了加快过滤速率,不断用玻璃棒搅拌
c.过滤所得MnO2须进行洗涤,为检验是否洗涤干净,可通过检测洗出液中是否存在 来判断
来判断

下列关于沉锰制备高纯MnO2的说法中,正确的是
a.若沉锰反应时加入足量浓盐酸并加热,MnO2的产率将降低
b.若沉锰后进行过滤操作,为了加快过滤速率,不断用玻璃棒搅拌
c.过滤所得MnO2须进行洗涤,为检验是否洗涤干净,可通过检测洗出液中是否存在
 来判断
来判断
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物,试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
(2)某同学把新制的氯水(主要成分Cl2)加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___________ 。
(3) 与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是___________ (填字母)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(1)人体正常的血红蛋白含有Fe2+,若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是___________(填字母)。
| A.亚硝酸盐被还原 | B.维生素C是还原剂 |
| C.维生素C将Fe3+还原为Fe2+ | D.亚硝酸盐是还原剂 |
(3)
 与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是
与过量稀硫酸反应可以制取FeSO4,若用反应所得的酸性溶液,将Fe2+转化为Fe3+,要求产物纯净,可选用的最佳试剂是a.Cl2 b.Fe c.H2O2 d.HNO3
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】某废催化剂中主要含SiO2、ZnO、CuS及少量的Fe3O4。某同学以该废催化剂为原料制备皓矾(ZnSO4• 7H2O)和蓝矾(CuSO4• 5H2O)的实验流程如图所示。已知:CuS不溶于稀硫酸。

(1)滤渣1的主要成分为________________ (填化学式)。
(2)实验室用浓H2SO4配制250mL0.50mol/L硫酸溶液时,不需要的仪器是_______ (填字母)。
a.玻璃棒b.胶头滴管c.漏斗d.容量瓶e.天平f.烧杯
(3)现有KMnO4溶液、NaOH溶液、碘水等试剂。用所提供的试剂检验滤液1中是否含有Fe2+的方法为___________ 。
(4)向盛有滤渣1的反应器中加入硫酸和H2O2溶液时发生反应的化学方程式为_______________ (已知滤渣2中含有S)

(1)滤渣1的主要成分为
(2)实验室用浓H2SO4配制250mL0.50mol/L硫酸溶液时,不需要的仪器是
a.玻璃棒b.胶头滴管c.漏斗d.容量瓶e.天平f.烧杯
(3)现有KMnO4溶液、NaOH溶液、碘水等试剂。用所提供的试剂检验滤液1中是否含有Fe2+的方法为
(4)向盛有滤渣1的反应器中加入硫酸和H2O2溶液时发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】化学工作者经常从不同的角度来预测某些物质的性质,然后进行实验验证,得出结论。某化学研究小组根据H2O2中氧元素的化合价,预测H2O2具有氧化性和还原性,并设计如下实验进行验证。请根据实验室提供的试剂以及相关实验内容选择合适的化学试剂进行实验验证,并对主要的实验现象进行描述,写出相关反应的离子方程式。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性_______ 。
提供的试剂有:FeCl2溶液,酸性KMnO4溶液,KSCN溶液
(1)请完成表中①~⑤的相关内容
| 验证H2O2的性质 | 选用的化学试剂 | 主要的实验现象 | 发生反应的离子方程式 |
| 还原性 | ① | ② | 略 |
| 氧化性 | ③ | ④ | ⑤ |
(2)请用一个化学方程式表示出H2O2既有氧化性又有还原性
您最近一年使用:0次
【推荐2】分析以下几个反应(未配平),填空:
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是___________ (填反应的序号)。
(2)写出反应①对应的一个化学反应方程式___________ 。
(3)反应②中每1molCl2完全反应转移电子为___________ mol。
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。______
___________Fe3++___________Fe=___________Fe2+
①Fe2++Zn→Zn2++Fe
②Fe2++Cl2→Fe3++Cl—
③Fe3++Fe→Fe2+
(1)Fe2+体现氧化性的是
(2)写出反应①对应的一个化学反应方程式
(3)反应②中每1molCl2完全反应转移电子为
(4)对反应③进行配平,并用单线桥标注电子转移的方向和数目。
___________Fe3++___________Fe=___________Fe2+
您最近一年使用:0次

 的化学性质实验用品:Zn、酸性
的化学性质实验用品:Zn、酸性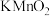 溶液、KOH溶液
溶液、KOH溶液

