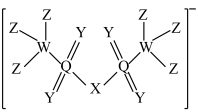
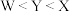下列判断及其解释都正确的是
| 选项 | 判断 | 解释 |
| A | 热稳定性: |  相对分子质量大 相对分子质量大 |
| B | 酸性: | 非金属性 大于S 大于S |
| C |  原子s电子云半径: 原子s电子云半径: | 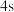 电子的能量高,在离核更远的区域出现的概率大 电子的能量高,在离核更远的区域出现的概率大 |
| D | 键角: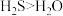 | 电负性O大于S, 中 中 键电子对之间的斥力小于 键电子对之间的斥力小于 中 中 键电子对之间的斥力 键电子对之间的斥力 |
| A.A | B.B | C.C | D.D |
更新时间:2024-04-29 12:47:34
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】有A、B、C、D四种元素,其中A、B、C属于同一周期,A原子最外层p能级的电子数等于次外层的电子总数;B原子最外层中有三个不成对的电子;C元素可分别与A、B、D生成RC2型化合物,其中的DC2与C3互为等电子体。下列叙述中不正确的是
| A.D原子的简化电子排布式为[Ar]3s23p4 |
| B.B、C两元素的第一电离能大小关系为B>C |
C.用电子式表示AD2的形成过程为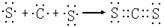 |
| D.由B60分子形成的晶体与A60相似,分子中总键能:B60 >A60 |
您最近半年使用:0次
【推荐2】乙二胺(H2NCH2CH2NH2)能与Mg2+、Cu2+等形成稳定环状离子,其中Cu2+与乙二胺形成的化合物稳定性更高。下列说法错误的是
| A.铜的第二电离能小于锌的第二电离能 |
| B.乙二胺中2个N原子均可与Cu2+形成配位键 |
| C.Cu2+与乙二胺形成的化合物稳定性更高是因为Cu2+半径大,配体之间的斥力小 |
| D.基态Mg原子中,电子占据的最高能层具有的原子轨道为9 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列说法中,正确的是
| A.NO2、BF3、NCl3分子中没有一个分子中各原子的最外层电子都达到8电子稳定结构 |
| B.P4、CH4都是正四面体分子,两种分子中化学键之间的夹角相等且均为109°28' |
| C.NH3、BF3、NF3都是四原子分子,都有三角锥形的立体结构 |
| D.含有极性键的分子未必是极性分子,非极性分子也未必含有非极性键 |
您最近半年使用:0次
【推荐2】科学家们合成了具有半导体特性的环状C18分子,其合成方法的示意图如图:
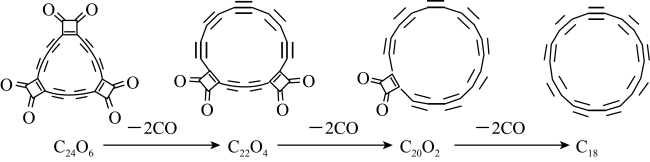
下列说法不正确的是

下列说法不正确的是
| A.键长:C≡C<C—C | B.键能:C—O > C—C |
| C.C22O4为非极性分子 | D.C18晶体为分子晶体 |
您最近半年使用:0次

 组成的磁性超导材料。下列说法正确的是
组成的磁性超导材料。下列说法正确的是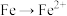 时失去
时失去 和
和 原子核外有3个未成对电子
原子核外有3个未成对电子 的空间结构为正四面体形
的空间结构为正四面体形