氮是自然界各种生物体生命活动不可缺少的重要元素,下列物质均含氮元素,回答下列问题:
(1)写出反应①的化学方程式___________ ;
(2)B在催化剂作用下生成C是工业制硝酸的基础,写出反应②的化学方程式___________ ;
(3)工业上用水吸收气体D生产硝酸,写出反应⑤的化学方程式___________ ,若生成标况下的C气体33.6L,转移电子数目为___________ .
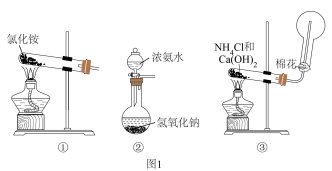
(4)从下图1的装置中选择一个可制备B气体的方法___________ ,并写出对应的化学方程式___________ . ___________ ,硝酸的浓度是___________ 。

(1)写出反应①的化学方程式
(2)B在催化剂作用下生成C是工业制硝酸的基础,写出反应②的化学方程式
(3)工业上用水吸收气体D生产硝酸,写出反应⑤的化学方程式
(4)从下图1的装置中选择一个可制备B气体的方法
更新时间:2024-04-30 05:28:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】A、B、C、D均为中学所学的常见物质且均含有同一种元素,它们之间的转化关系如下图所示(反应条件及其他物质已经略去):A B
B C
C D。
D。
(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式)A:___________ ,D:_________ .写出A→B转化的化学方程式:_______________ .
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.则A为___________ ,写出A→B转化的化学方程式:_______________________ .
 B
B C
C D。
D。(1)若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式)A:
(2)若A的水溶液能使湿润的红色石蕊试纸变蓝,D的稀溶液能使蓝色的湿润石蕊试纸变红.则A为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】NH3经一系列反应可以得到HNO3和NH4NO3,如图所示。
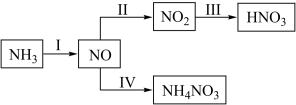
(1)氨气的结构式为_______ 。
(2)实验室里用NH4Cl和熟石灰共热制取氨气反应的化学方程式为_______ 。
(3)步骤I中NH3和O2存催化剂作用下反应生成NO,其化学方程式是_______ 。
(4)写出步骤Ⅲ发生反应的化学方程式_______ ,该反应中氧化剂与还原剂的物质的量之比是_______ 。
(5)通过实验检验试样中的NH 的方法:取少量试样于试管中,
的方法:取少量试样于试管中,_______ 。

(1)氨气的结构式为
(2)实验室里用NH4Cl和熟石灰共热制取氨气反应的化学方程式为
(3)步骤I中NH3和O2存催化剂作用下反应生成NO,其化学方程式是
(4)写出步骤Ⅲ发生反应的化学方程式
(5)通过实验检验试样中的NH
 的方法:取少量试样于试管中,
的方法:取少量试样于试管中,
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】A.B.C.D.E为中学化学常见物质,它们之间相互转化关系如图所示,部分反应条件和产物已经略去。回答下列问题:
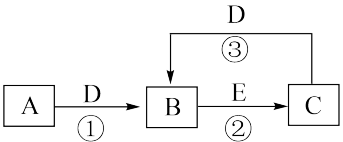
(1)若A、E是常见金属单质,D是一种黄绿色气体,则A___________ (填化学式),完成反应②的离子方程式___________ 。
(2)若A是最简单的有机物,B、C是氧化物,反应①的化学方程式是___________ ;该反应中还原剂是___________ ,生成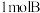 ,转移电子是
,转移电子是___________  。
。
(3)若A是气体,水溶液呈碱性,C、D是空气的主要成分,E是一种有毒气体能与血红蛋白结合。检验A气体的方法是___________ ;反应②的化学方程式是___________ 。
(4)若A、C是常见的非金属单质,B、C、D、E中含同一种元素,D的浓溶液可以使铝、铁钝化,反应①的化学方程式是___________ 。

(1)若A、E是常见金属单质,D是一种黄绿色气体,则A
(2)若A是最简单的有机物,B、C是氧化物,反应①的化学方程式是
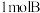 ,转移电子是
,转移电子是 。
。(3)若A是气体,水溶液呈碱性,C、D是空气的主要成分,E是一种有毒气体能与血红蛋白结合。检验A气体的方法是
(4)若A、C是常见的非金属单质,B、C、D、E中含同一种元素,D的浓溶液可以使铝、铁钝化,反应①的化学方程式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】实验室用如图所示装置进行氨气实验。
(1)实验室常用 NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为______ 。
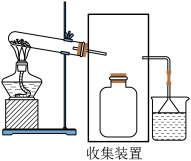
(2)若要收集一瓶氨气,请将下列甲装置补充完整,在虚框内画出连接图______ 。
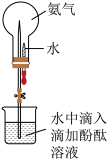
(3)用如图装置做喷泉实验。轻轻挤压滴管,使少量水进入烧瓶,打开止水夹,观察现象, 解释产生这一现象的原因______ 。
(4)如图为合成氨催化氧化制硝酸的流程示意图:
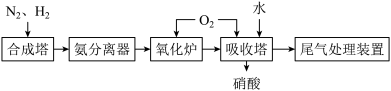
①合成塔中化学方程式为______ 。
②氧化炉中的化学方程式______ 。
③吸收塔 NO2 HNO3氧化剂与还原剂物质的量之比为
HNO3氧化剂与还原剂物质的量之比为______ 。
(1)实验室常用 NH4Cl 与Ca(OH)2制取氨气,该反应的化学方程式为
(2)若要收集一瓶氨气,请将下列甲装置补充完整,在虚框内画出连接图

(3)用如图装置做喷泉实验。轻轻挤压滴管,使少量水进入烧瓶,打开止水夹,观察现象, 解释产生这一现象的原因

(4)如图为合成氨催化氧化制硝酸的流程示意图:

①合成塔中化学方程式为
②氧化炉中的化学方程式
③吸收塔 NO2
 HNO3氧化剂与还原剂物质的量之比为
HNO3氧化剂与还原剂物质的量之比为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】侯德榜是我国制碱工业的先驱,他根据氨碱法制碱的缺点提出用饱和的NaCl溶液、CO2、NH3反应制取纯碱的联合制碱法。某学校课外活动小组根据侯氏制碱法的原理在实验室模拟制碱。请回答下列问题:
(1)写出实验室制取NH3的化学方程式:_______ 。

(2)上图B中的a接装置图____ (填图A或图C)
(3)用离子方程式表示装有饱和食盐水的集气瓶中的现象:_________ 。
(4)水槽中的冷水的作用除了可以增加气体物质在溶液中的溶解度外还有一个重要作用是:____ 。
(5)图B中c的作用是:___ 。
(1)写出实验室制取NH3的化学方程式:

(2)上图B中的a接装置图
(3)用离子方程式表示装有饱和食盐水的集气瓶中的现象:
(4)水槽中的冷水的作用除了可以增加气体物质在溶液中的溶解度外还有一个重要作用是:
(5)图B中c的作用是:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某学生利用以图装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。

请回答下列问题
(1)装置A产生氨气,则烧瓶内固体可选用___ (填字母)。
a.烧碱 b.二氧化锰 c.生石灰 d.氯化铵
(2)B装置的作用是___ ;E装置的作用是___ 。
(3)G处可能逸出黄绿色的气体,可将该气通入盛有___ 溶液的烧杯来处理,离子方程式为___ 。
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:___ 。

请回答下列问题
(1)装置A产生氨气,则烧瓶内固体可选用
a.烧碱 b.二氧化锰 c.生石灰 d.氯化铵
(2)B装置的作用是
(3)G处可能逸出黄绿色的气体,可将该气通入盛有
(4)氯气和氨气在常温下混合就能发生反应生成氯化铵和氮气,该反应的化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】研究氮及其化合物的性质,可以有效改善人类的生存环境。氮元素化合价-物质类别关系图如下。

回答下列问题:
(1)写出N原子的结构示意图_______ ;物质A的结构式_______ 。
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是_______ 。
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:_______ 。
(4)实验室中,检验溶液中含有NH 的操作方法是
的操作方法是_______ 。
(5)物质B为红棕色气体,写出该物质与水反应的离子方程式_______ ,当反应消耗3.36L(标准状况)物质B时,转移电子的物质的量为_______ mol。

回答下列问题:
(1)写出N原子的结构示意图
(2)在催化剂和加热的条件下,物质A生成NO是工业制硝酸的重要反应,化学方程式是
(3)在加热条件下,物质C的浓溶液与碳单质反应,写出反应的化学方程式:
(4)实验室中,检验溶液中含有NH
 的操作方法是
的操作方法是(5)物质B为红棕色气体,写出该物质与水反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】工业上制备的硝酸和自然界中硝酸的形成既有相同的地方,又有区别,图中步骤①②③④是工业制硝酸的主要流程,步骤Ⅰ、Ⅱ、Ⅲ是自然界雷电高能固氮过程中产生硝酸的途径,试回答下列问题。

(1)反应④的化学方程式是___________ ;每生成6.3 g  理论上转移电子的物质的量为
理论上转移电子的物质的量为___________ 。
(2)某课外小组同学用图所示装置进行实验(夹持装置已省略)用该装置制备 并研究其性质。收集一试管
并研究其性质。收集一试管 ,取下试管B倒立在水中,观察到的现象是
,取下试管B倒立在水中,观察到的现象是___________ ,实验室制取 的化学方程式为
的化学方程式为___________ 。

(3) 与硫酸反应的化学方程式是
与硫酸反应的化学方程式是___________ ,检验生成物中阳离子的方法是___________ 。
(4)NO、 可以用NaOH溶液吸收,化学方程式是
可以用NaOH溶液吸收,化学方程式是 ,有NO、
,有NO、 混合气体用100 mL 1 mol⋅L
混合气体用100 mL 1 mol⋅L NaOH溶液恰好吸收,NO、
NaOH溶液恰好吸收,NO、 在标准状况下的体积是
在标准状况下的体积是___________ 。

(1)反应④的化学方程式是
 理论上转移电子的物质的量为
理论上转移电子的物质的量为(2)某课外小组同学用图所示装置进行实验(夹持装置已省略)用该装置制备
 并研究其性质。收集一试管
并研究其性质。收集一试管 ,取下试管B倒立在水中,观察到的现象是
,取下试管B倒立在水中,观察到的现象是 的化学方程式为
的化学方程式为
(3)
 与硫酸反应的化学方程式是
与硫酸反应的化学方程式是(4)NO、
 可以用NaOH溶液吸收,化学方程式是
可以用NaOH溶液吸收,化学方程式是 ,有NO、
,有NO、 混合气体用100 mL 1 mol⋅L
混合气体用100 mL 1 mol⋅L NaOH溶液恰好吸收,NO、
NaOH溶液恰好吸收,NO、 在标准状况下的体积是
在标准状况下的体积是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】实验室利用下列装置模拟工业生产中氨气和氧气反应制备少量硝酸。
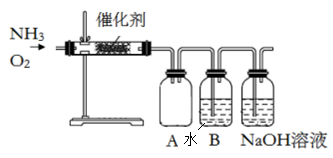
(1)NaOH溶液的作用是___________ 。
(2) B中反应的化学方程式为___________ 。
(3)下列试剂可用于干燥氨气是___________ 。(填字母)
A.浓H2SO4 B.碱石灰 C.无水CaCl2 D. P2O5
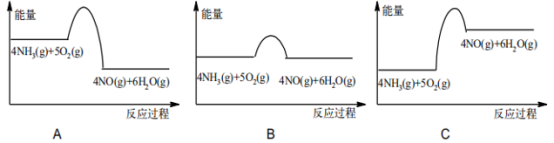
(4)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持温度可达到700℃以上,下列图示中, 能够正确表示该反应过程能量变化的是___________ (填字母)。
(5)控制氨气和氧气的比例是制备硝酸的关键,当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。白烟的化学式是___________ 。

(1)NaOH溶液的作用是
(2) B中反应的化学方程式为
(3)下列试剂可用于干燥氨气是
A.浓H2SO4 B.碱石灰 C.无水CaCl2 D. P2O5
(4)实验时先用酒精喷灯预热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持温度可达到700℃以上,下列图示中, 能够正确表示该反应过程能量变化的是

(5)控制氨气和氧气的比例是制备硝酸的关键,当比例不合适时,A中不仅有红棕色气体产生,还伴有白烟。白烟的化学式是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】某化学自主实验小组利用如图所示装置探究NO2能否被NH3还原(K1、K2为止水夹,夹持固定装置略去)。(夹持、固定装置均略去)。
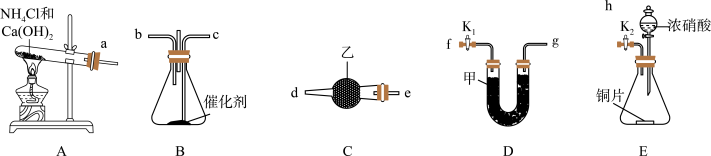
(1)A装置发生的化学反应方程式为______ 。
(2)如按装置由左向右,连接上述装置的正确顺序是_____ 。
a→f→g→_______→_______→_______→_______→h(填各接口字母)。
(3)装置B中NO2能够在催化剂作用下被NH3还原,生成氮气和水,写出发生反应的化学方程式:_____ 。
(4)甲是_____ (填药品名称),作用是______ 。
(5)此实验装置存在一个明显的缺陷是_____ 。
(6)若装置E反应过程中共产生标准状况下气体22.4L(不考虑NO2与N2O4的转化)则消耗的浓硝酸的物质的量为_____ 。

(1)A装置发生的化学反应方程式为
(2)如按装置由左向右,连接上述装置的正确顺序是
a→f→g→_______→_______→_______→_______→h(填各接口字母)。
(3)装置B中NO2能够在催化剂作用下被NH3还原,生成氮气和水,写出发生反应的化学方程式:
(4)甲是
(5)此实验装置存在一个明显的缺陷是
(6)若装置E反应过程中共产生标准状况下气体22.4L(不考虑NO2与N2O4的转化)则消耗的浓硝酸的物质的量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某同学认为碳与浓硝酸反应过程中还应有NO生成。为了验证是否有NO生成,利用下列实验装置进行实验。已知: 的沸点为21℃;D装置中盛放
的沸点为21℃;D装置中盛放 ,各装置的连接顺序为a→gf→de→cb→hi。
,各装置的连接顺序为a→gf→de→cb→hi。

回答下列问题:
(1)上图A中,仪器X的名称为_______ 。
(2)装置D的作用是_______ 。
(3)连接好顺序后,首先要打开装置A中的弹簧夹K,通入一段时间 ,其目的是
,其目的是_______ 。
(4)实验过程中,该同学根据_______ 和_______ 得出碳与浓硝酸反应过程中还应有NO生成的结论。(分别填写某个装置和对应的实验现象)
(5)若A中反应的两种还原产物物质的量之比为1:1,写出反应的化学方程式:_______ 。
 的沸点为21℃;D装置中盛放
的沸点为21℃;D装置中盛放 ,各装置的连接顺序为a→gf→de→cb→hi。
,各装置的连接顺序为a→gf→de→cb→hi。
回答下列问题:
(1)上图A中,仪器X的名称为
(2)装置D的作用是
(3)连接好顺序后,首先要打开装置A中的弹簧夹K,通入一段时间
 ,其目的是
,其目的是(4)实验过程中,该同学根据
(5)若A中反应的两种还原产物物质的量之比为1:1,写出反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】KI可用作利尿剂、治疗慢性支气管炎,实验室中制备一定量KI的过程及实验装置(加热及夹持装置已省略)如下:

回答下列问题:
(1)“碱溶”时,适宜的加热方式为_______ ,“还原”后分离出S的操作中用到的玻璃仪器除玻璃棒外还有_______
(2)仪器a的名称是_______ ,装置C的用途是_______ ,实验中不能用稀硝酸代替稀硫酸的根本原因是_______ 。
(3)“碱溶”时得到的氧化产物可用于加碘盐的生产中,则 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为_______ 。
(4)产品中可能会含有KOH杂质,可利用_______ 法提纯KI。为测定KI的纯度,称取0.5000 g样品溶于水,然后用0.05 mol·L 的酸性
的酸性 标准溶液滴定(
标准溶液滴定( ),终点时消耗11.60 mL标准溶液,则样品的纯度为
),终点时消耗11.60 mL标准溶液,则样品的纯度为_______ (保留两位有效数字),若滴定终点读数时俯视刻度线,则测定KI纯度的结果_______ (填“偏大”或“偏小”)。

回答下列问题:
(1)“碱溶”时,适宜的加热方式为
(2)仪器a的名称是
(3)“碱溶”时得到的氧化产物可用于加碘盐的生产中,则
 与KOH溶液反应的离子方程式为
与KOH溶液反应的离子方程式为(4)产品中可能会含有KOH杂质,可利用
 的酸性
的酸性 标准溶液滴定(
标准溶液滴定( ),终点时消耗11.60 mL标准溶液,则样品的纯度为
),终点时消耗11.60 mL标准溶液,则样品的纯度为
您最近一年使用:0次



