对下列事实的解释不正确 的是
| 选项 | 事实 | 解释 |
| A | 稳定性: | H-F键键能大于H-I键键能。 |
| B | 键角: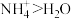 | 中心原子均采取 杂化,孤电子对有较大的斥力 杂化,孤电子对有较大的斥力 |
| C | 熔点:石英>干冰 | 石英是共价晶体,干冰是分子晶体;共价键比分子间作用力强 |
| D | 金属活动性: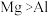 | 第一电离能: |
| A.A | B.B | C.C | D.D |
23-24高三上·北京·开学考试 查看更多[2]
更新时间:2024-05-02 22:53:52
|
相似题推荐
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】现有四种元素的基态原子的电子排布式如下,则下列判断正确的是
① ②
② ③
③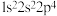 ④
④
①
 ②
② ③
③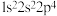 ④
④
| A.第一电离能:④>③ | B.电负性:③>② |
| C.离子半径:②>④ | D.氢化物的沸点:③>① |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】部分短周期元素原子半径的相对大小、最高正价或最低负价随原子序数的变化关系如图所示,下列说法正确的是


| A.离子半径的大小顺序:e>f>g>h |
| B.g、h的氧化物对应水化物的酸性:h>g |
| C.y、z、d三种元素第一电离能和电负性的大小顺序不一致 |
| D.e、f两种元素对应最高价氧化物的水化物之间不能发生反应 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐3】以下有关元素性质的说法中正确的是
| A.以下原子中,①1s22s22p63s23p2,②1s22s22p3,③1s22s22p2,④1s22s22p63s23p4,原子半径最大的是④ |
| B.下列原子中,①1s2,②1s22s22p6,③1s22s22p63s23p6对应的第一电离能最大的元素是③ |
| C.某短周期元素的逐级电离能(kJ/mol)分别为578、1817、2745、11575、14830、18376、23293,该元素可能位于第三周期IIA族 |
| D.①Na、K、Rb,②C、S、P,③Na、P、O元素的电负性依次递增的是③ |
您最近一年使用:0次
【推荐1】工业制硝酸转化器中发生反应:4NH3+5O2 4NO+6H2O。下列说法正确的是
4NO+6H2O。下列说法正确的是
 4NO+6H2O。下列说法正确的是
4NO+6H2O。下列说法正确的是| A.半径大小:r(N)<r(O) | B.电离能大小:I1(N)<I1(O) |
| C.电负性大小:χ(N)<χ(O) | D.热稳定性:H2O<NH3 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】尿素CO(NH2)2是一种高效化肥,也是一种化工原料。反应CO2+2NH3 CO(NH2)2+H2O可用于尿素的制备。下列有关说法
CO(NH2)2+H2O可用于尿素的制备。下列有关说法不正确 的是
 CO(NH2)2+H2O可用于尿素的制备。下列有关说法
CO(NH2)2+H2O可用于尿素的制备。下列有关说法| A.NH3与CO(NH2)2均为极性分子 |
B.N2H4分子的电子式为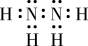 |
| C.NH3的键角大于H2O的键角 |
| D.尿素分子σ键和π键的数目之比为6∶1 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐1】下列化学用语表达中正确的是
A.甲基的电子式: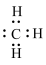 |
B.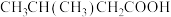 系统命名法为:2-甲基丁酸 系统命名法为:2-甲基丁酸 |
C. 的VSEPR模型为 的VSEPR模型为 |
D. 的空间结构:平面三角形 的空间结构:平面三角形 |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐2】工业上利用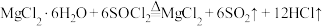 制备无水
制备无水 。下列说法正确的是
。下列说法正确的是
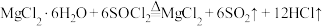 制备无水
制备无水 。下列说法正确的是
。下列说法正确的是A.S的原子结构示意图为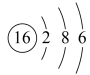 | B. 的电子式为: 的电子式为: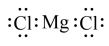 |
C. 分子的空间构型为平面三角形 分子的空间构型为平面三角形 | D. 的结构为 的结构为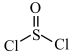 |
您最近一年使用:0次
单选题
|
较易
(0.85)
解题方法
【推荐1】某非线性光学晶体由钾元素(K)和原子序数依次增大的X、Y、Z、W四种短周期元素组成。X与Y、Z与W均为同周期相邻元素,X的核外电子总数为最外层电子数的2倍,Z为地壳中含量最多的元素。下列说法正确的是
| A.简单氢化物沸点:Z>W |
B.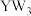 分子中各原子均满足8电子的稳定结构 分子中各原子均满足8电子的稳定结构 |
| C.简单离子半径:Z<W |
| D.第一电离能:Y>Z |
您最近一年使用:0次
单选题
|
较易
(0.85)
【推荐2】下列说法中正确的是
| A.NaCl 溶液在电流的作用下电离成 Na+和 Cl- |
| B.由非金属元素组成的化合物一定是共价化合物 |
| C.离子化合物中可能含有非极性键或极性键 |
| D.分子晶体中,分子间作用力越大,分子越稳定 |
您最近一年使用:0次

 为直线形分子,则
为直线形分子,则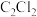 也为直线形分子
也为直线形分子 分子的空间结构为V形,则
分子的空间结构为V形,则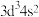 ,基态Cr的价层电子排布式为
,基态Cr的价层电子排布式为