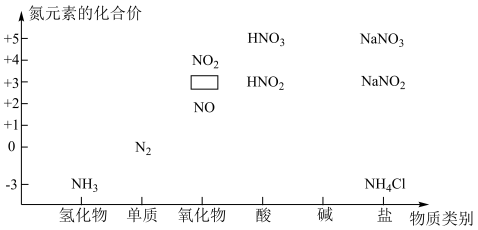
下图是氮的化合物的“价类二维图”。___________ 。
(2)图中方框中的化学式为___________ ,一水合氨电离可使溶液显碱性,写出一水合氨的电离方程式:___________ 。
(3)写出 和
和 在加热催化剂条件下生成
在加热催化剂条件下生成 的化学方程式:
的化学方程式:___________ 。
(4)向盛有少量 溶液的试管中加入
溶液的试管中加入 溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是___________ 。
(5)将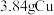 和稀硝酸充分反应,生成的气体体积为
和稀硝酸充分反应,生成的气体体积为___________ L(在标准状况下),用排水法收集该气体,将收集到的气体的试管倒立于水槽中缓缓通入___________ 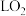 (标准状况)使
(标准状况)使 恰好完全反应。
恰好完全反应。
(2)图中方框中的化学式为
(3)写出
 和
和 在加热催化剂条件下生成
在加热催化剂条件下生成 的化学方程式:
的化学方程式:(4)向盛有少量
 溶液的试管中加入
溶液的试管中加入 溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是
溶液并加热,在试管口放一片湿润的红色石蕊试纸,实验现象是(5)将
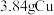 和稀硝酸充分反应,生成的气体体积为
和稀硝酸充分反应,生成的气体体积为 (标准状况)使
(标准状况)使 恰好完全反应。
恰好完全反应。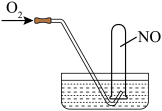
更新时间:2024-05-05 08:25:27
|
相似题推荐
【推荐1】近几年来关于氮污染的治理倍受关注。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、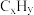 、
、 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。

在图示的转化中,被还原的元素是___________ ,X的化学式为___________ 。
(2)SCR技术可使 与
与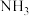 直接反应,实现无害转化。假设
直接反应,实现无害转化。假设 是NO时,发生反应的化学方程式是
是NO时,发生反应的化学方程式是_______ 。
(3)利用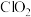 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: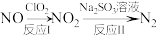 。反应I的化学方程式是
。反应I的化学方程式是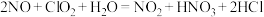 ,反应II的离子方程式是
,反应II的离子方程式是___________ 。
(4)加入过量次氯酸钠可使废水中 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。
①检验废水中是否存在 的方法是
的方法是___________ 。
②若处理废水产生了0.448L (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为___________ mL。
(1)三效催化剂是最为常见的汽车尾气催化剂,能同时实现汽车尾气中的CO、
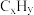 、
、 三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
三种成分的净化,其催化剂表面物质转化的关系如图1所示,化合物X可借助傅里叶红外光谱图(如图2所示)确定。
在图示的转化中,被还原的元素是
(2)SCR技术可使
 与
与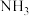 直接反应,实现无害转化。假设
直接反应,实现无害转化。假设 是NO时,发生反应的化学方程式是
是NO时,发生反应的化学方程式是(3)利用
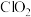 氧化氮氧化物反应过程如下:
氧化氮氧化物反应过程如下: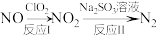 。反应I的化学方程式是
。反应I的化学方程式是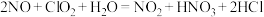 ,反应II的离子方程式是
,反应II的离子方程式是(4)加入过量次氯酸钠可使废水中
 完全转化为
完全转化为 ,而本身被还原为NaCl。
,而本身被还原为NaCl。①检验废水中是否存在
 的方法是
的方法是②若处理废水产生了0.448L
 (标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
(标准状况),则需消耗浓度为2mol/L的次氯酸钠的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求书写方程式:
(1)向NaAlO2溶液中通入过量CO2的离子方程式:____________________
(2)MnO2与浓盐酸制备氯气的离子方程式:__________________________
(3)工业上制备粗硅的化学方程式:___________________________________
(4)硫酸铵溶液与氢氧化钡溶液共热的离子方程式:___________________________ 。
(1)向NaAlO2溶液中通入过量CO2的离子方程式:
(2)MnO2与浓盐酸制备氯气的离子方程式:
(3)工业上制备粗硅的化学方程式:
(4)硫酸铵溶液与氢氧化钡溶液共热的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】I.某化学实验小组同学利用如图实验装置制取氨气,并探究氨气的性质(部分仪器已略去)。消回答:

(1)大试管中发生反应的化学方程式为_______
(2)仪器d的名称是_______ ,用装置B收集氨气时,应选择氨气的进气口是_______ (填“a”或“b”)。
(3)待d中收集满氨气,关闭止水夹a和b,_______ (在横线上补写实验操作),可观察到烧瓶内产生红色喷泉。
II.工业合成氨是人类科学技术的一项近大突破。
已知:

(4)理论上有利于提高合成氨平衡产率的条件有_______
A.高压 B.低压 C.高温 D.低温 E.使用高效催化剂
(5)在实际生产中,选择的温度为400-500℃,其重要原因是_______
(6)t℃下,在容积为1L的刚性容器中,通入2mol 和6mol
和6mol ,在一定条件下反应达到平衡时,容器中剩余1mol
,在一定条件下反应达到平衡时,容器中剩余1mol ,达到平衡时生成
,达到平衡时生成 的物质的量为
的物质的量为_______ mol,反应放出的热量为_______ kJ,t℃下,平衡后向同一容器中再充入1mol 1mol
1mol 2mol
2mol ,平衡
,平衡_______ (填“不”“正向”或“逆向”)移动。

(1)大试管中发生反应的化学方程式为
(2)仪器d的名称是
(3)待d中收集满氨气,关闭止水夹a和b,
II.工业合成氨是人类科学技术的一项近大突破。
已知:


(4)理论上有利于提高合成氨平衡产率的条件有
A.高压 B.低压 C.高温 D.低温 E.使用高效催化剂
(5)在实际生产中,选择的温度为400-500℃,其重要原因是
(6)t℃下,在容积为1L的刚性容器中,通入2mol
 和6mol
和6mol ,在一定条件下反应达到平衡时,容器中剩余1mol
,在一定条件下反应达到平衡时,容器中剩余1mol ,达到平衡时生成
,达到平衡时生成 的物质的量为
的物质的量为 1mol
1mol 2mol
2mol ,平衡
,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】氮元素的单质和常见化合物在工、农业生产中用途广泛。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是___________ 。
(2)___________ 实验证明氨气极易溶于水。通常用___________ (填名称)干燥氨气。
(3)铵盐大多在农业上用作化肥,固体 与固体
与固体 加热反应可生成氨气,其化学方程式为
加热反应可生成氨气,其化学方程式为___________ 。
(4)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式___________ 。
(5)如图为合成氨以及氨氧化制硝酸的流程示意图。
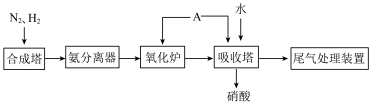
①写出合成塔中的化学反应方程式___________ 。向氧化炉和吸收塔中通入的A是___________ 。
②工业制硝酸的尾气是酸性气体,为防止环境污染,可以用___________ (填化学式)溶液吸收。
(1)氮气的化学性质很稳定,可用作灯泡填充气。解释其原因是
(2)
(3)铵盐大多在农业上用作化肥,固体
 与固体
与固体 加热反应可生成氨气,其化学方程式为
加热反应可生成氨气,其化学方程式为(4)硝酸是一种重要的含氮酸,书写铜和稀硝酸反应的离子方程式
(5)如图为合成氨以及氨氧化制硝酸的流程示意图。

①写出合成塔中的化学反应方程式
②工业制硝酸的尾气是酸性气体,为防止环境污染,可以用
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】某化学兴趣小组的同学利用下图所示实验装置进行某些气体的制备、性质探究等实验(图中夹持装置已省略)。
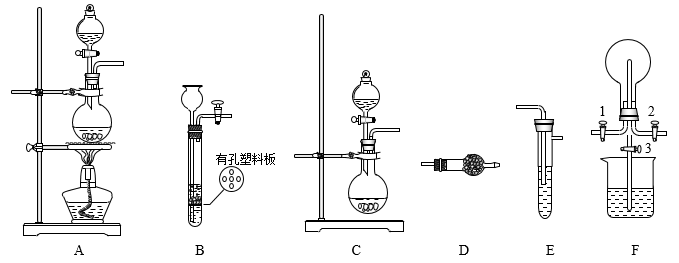
I.制备气体
(1)利用装置B可制取的气体有___________ (选填字母序号)。
a.CO2b.H2 c.SO2
II.探究Cl2与NH3的反应
(2)装置C与装置D连接可制取干燥的氨气,D装置内的药品是_______ ;装置A、E、D连接可制取纯净、干燥的Cl2,E装置的作用是___________ 。
(3)装置F可用于探究Cl2与NH3的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入______ ,然后关闭3,打开2,向烧瓶中慢慢通入一定量的另一种气体。实验开始一段时间后,烧瓶内出现浓厚的白烟并在容器内壁凝结,该反应的化学方程式为___________ 。
III.探究某些物质的性质
(4)利用装置C、E可设计实验比较碳元素和硅元素的非金属性强弱,实验方案是___________ 。
(5)将装置B、C分别与装置F相连后,进行H2S与SO2反应的实验。烧瓶中发生反应的化学方程式为___________ 。

I.制备气体
(1)利用装置B可制取的气体有
a.CO2b.H2 c.SO2
II.探究Cl2与NH3的反应
(2)装置C与装置D连接可制取干燥的氨气,D装置内的药品是
(3)装置F可用于探究Cl2与NH3的反应。实验时打开开关1、3,关闭2,先向烧瓶中通入
III.探究某些物质的性质
(4)利用装置C、E可设计实验比较碳元素和硅元素的非金属性强弱,实验方案是
(5)将装置B、C分别与装置F相连后,进行H2S与SO2反应的实验。烧瓶中发生反应的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】2019年,西班牙马德里市议会重新启动了二氧化氮(NO2)高污染议定书。该议定书旨在改善城市的空气质量,从而加强对公民健康的保护,使其免受高污染事件的有害影响,特别是对患有呼吸问题的人和孕妇的有害影响。
氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。


(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
①在反应①中,氧化剂是___________ ;在反应②中,氧化剂和还原剂的物质的量之比为___________ 。
②由反应②判断二氧化氮___________ (填“是”或“不是”)酸性氧化物。解释原因:___________ 。
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:___________ 。
(3)目前有一种治理方法是在一定条件下,用氨气将氮氧化物转化为无污染的物质。
①请写出NO2发生该反应的化学方程式:___________ 。生成1.4 mol N2时,转移电子的物质的量为___________ 。
②现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3,恰好使其完全转化为N2,则原混合气体中NO2和NO的物质的量之比为___________ 。
氮氧化物进入大气后,不仅会形成硝酸型酸雨,还可能形成光化学烟雾,因此必须对含有氮氧化物的废气进行处理。


(1)用氢氧化钠溶液可以吸收废气中的氮氧化物,反应的化学方程式如下:
NO2+NO+2NaOH=2NaNO2+H2O ①
2NO2+2NaOH=NaNO2+NaNO3+H2O ②
①在反应①中,氧化剂是
②由反应②判断二氧化氮
(2)汽车尾气中含有CO和NO,消除这两种物质对大气的污染的方法是安装催化转化器,使它们发生反应消除污染,试写出该反应的化学方程式:
(3)目前有一种治理方法是在一定条件下,用氨气将氮氧化物转化为无污染的物质。
①请写出NO2发生该反应的化学方程式:
②现有NO2和NO的混合气体3 L,通入3 L(同温同压下)NH3,恰好使其完全转化为N2,则原混合气体中NO2和NO的物质的量之比为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】16g铜投入一定浓度的硝酸溶液中,铜完全溶解,共收集到NO和NO2的混合气体4.48L气体(标准状况)。
①计算产生NO的体积(标准状况)__________ L。
②将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为__________ L。
①计算产生NO的体积(标准状况)
②将盛有此混合气体的容器倒扣在水中,通入标准状况下一定体积的O2,恰好使气体完全溶于水中,则通入O2的体积为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】十九大报告提出“要像对待生命一样对待生态环境”,对硫、氮元素形成的有毒、有害物质进行处理成为科学研究热点。
(1)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是______ (填字母)。
a.碳氧化物 b.硫氧化物 c.氮氧化物
(2) 是严重危害环境的气体,可采取多种方法减少
是严重危害环境的气体,可采取多种方法减少 的排放并加以资源利用。
的排放并加以资源利用。
①用 吸收
吸收 ,发生反应的离子方程式为
,发生反应的离子方程式为___________ 。
② 与
与 在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为
在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为___________ 。
(3) 氧化吸收法可用于处理氮氧化物。
氧化吸收法可用于处理氮氧化物。 可将NO氧化为
可将NO氧化为 ,并进一步将
,并进一步将 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图1所示),氮氧化物去除率与吸收器内碎瓷片填料的高度关系如图2所示。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图1所示),氮氧化物去除率与吸收器内碎瓷片填料的高度关系如图2所示。

① 和
和 反应的离子方程式为
反应的离子方程式为___________ 。
②随着吸收器内填料高度增加, 去除率升高的原因是
去除率升高的原因是___________ 。
(4)用碱液吸收氮氧化物( ):
):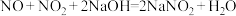 、
、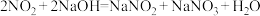 。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________(填字母)。
。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________(填字母)。
(1)防治环境污染,改善生态环境已成为全球共识。下列物质会形成酸雨的是
a.碳氧化物 b.硫氧化物 c.氮氧化物
(2)
 是严重危害环境的气体,可采取多种方法减少
是严重危害环境的气体,可采取多种方法减少 的排放并加以资源利用。
的排放并加以资源利用。①用
 吸收
吸收 ,发生反应的离子方程式为
,发生反应的离子方程式为②
 与
与 在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为
在高温下反应可生成氧硫化碳(COS),氧硫化碳分子中所有原子均满足最外层8电子稳定结构,其结构式为(3)
 氧化吸收法可用于处理氮氧化物。
氧化吸收法可用于处理氮氧化物。 可将NO氧化为
可将NO氧化为 ,并进一步将
,并进一步将 氧化为
氧化为 ,
, 则被还原为
则被还原为 。吸收时,
。吸收时, 溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图1所示),氮氧化物去除率与吸收器内碎瓷片填料的高度关系如图2所示。
溶液从吸收器顶部喷淋,氮氧化物从吸收器底部通入(如图1所示),氮氧化物去除率与吸收器内碎瓷片填料的高度关系如图2所示。
①
 和
和 反应的离子方程式为
反应的离子方程式为②随着吸收器内填料高度增加,
 去除率升高的原因是
去除率升高的原因是(4)用碱液吸收氮氧化物(
 ):
):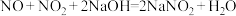 、
、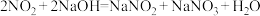 。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________(填字母)。
。根据上述原理判断,将下列气体通入过量NaOH溶液中,反应结束后一定有剩余的是___________(填字母)。A.1mol 和4mol 和4mol | B.1molNO和4mol |
C.1mol 和7molNO 和7molNO | D.6molNO和4mol |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】碘是人体必需的微量元素,也可用于工业、医药等领域。大量的碘富集于海藻灰〔主要成分是NaI)中,因此从海藻灰中提取碘,可有效利用海洋资源。
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为______ 。
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到______ (颜色)气体放出,______ (颜色)晶体析出。出于安全和环保考虑,该实验操作需在______ (条件)下进行。该反应的化学方程式为______ 。
(1)某兴趣小组以海藻灰为原料进行I2的制备实验。具体步骤如下:将海藻灰加热浸泡后,得到了NaI溶液,将适量Na2SO3固体溶于NaI溶液,再将CuSO4饱和溶液滴入上述溶液中,生成白色CuI沉淀,该反应的离子方程式为
(2)待I-沉淀完全后,过滤,将沉淀物置于小烧杯中,在搅拌下逐滴加入适量浓HNO3,观察到
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】足量的铜片与含4 mol HNO3的浓硝酸充分反应生成二氧化氮的分子数为2NA___
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】如图是氮元素的几种价态与物质类别的对应关系。请回答下列问题:

(1)写出N2的一种用途:___ 。
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为___ 。
(3)实验室制取物质B的化学方程式为____ 。
(4)NO2与水反应生成物质A的化学方程式为____ 。
(5)浓硝酸与木炭在加热条件下反应的化学方程式为___ 。

(1)写出N2的一种用途:
(2)HNO3与图中的物质C常用于检验Cl-的存在,则C的化学式为
(3)实验室制取物质B的化学方程式为
(4)NO2与水反应生成物质A的化学方程式为
(5)浓硝酸与木炭在加热条件下反应的化学方程式为
您最近一年使用:0次

 、N
、N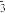 、NH
、NH 、N2H
、N2H 、N2H
、N2H 等。已知N2H5+的形成过程类似于NH
等。已知N2H5+的形成过程类似于NH

