利用废铝箔(主要成分为Al,含少量Mg、Fe等)制明矾 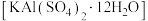 的一种工艺流程如下:
的一种工艺流程如下:
铝箔 甲溶液
甲溶液 Al(OH)3
Al(OH)3 乙溶液
乙溶液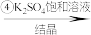 明矾
明矾
资料: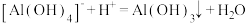 。
。
下列说法中,不正确的是
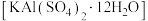 的一种工艺流程如下:
的一种工艺流程如下:铝箔
 甲溶液
甲溶液 Al(OH)3
Al(OH)3 乙溶液
乙溶液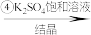 明矾
明矾资料:
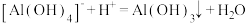 。
。下列说法中,不正确的是
A.乙溶液中含有的离子有Al3+、 、 、 |
| B.①体现了铝能与碱溶液反应的性质 |
C.由④可推测,室温下明矾的溶解度小于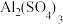 和K2SO4的溶解度 和K2SO4的溶解度 |
D.Al、Al(OH)3、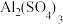 均具有两性 均具有两性 |
更新时间:2024-05-08 12:53:28
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】用稀H2SO4、NaOH溶液和单质铝为原料制取Al(OH)3,甲、乙、丙三个学生制备的途径分别是:
甲:Al Al2(SO4)3
Al2(SO4)3 Al(OH)3
Al(OH)3
乙:Al NaAlO2
NaAlO2 Al(OH)3
Al(OH)3
丙: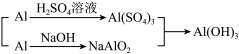
若要得到等量的Al(OH)3,则
甲:Al
 Al2(SO4)3
Al2(SO4)3 Al(OH)3
Al(OH)3乙:Al
 NaAlO2
NaAlO2 Al(OH)3
Al(OH)3丙:

若要得到等量的Al(OH)3,则
| A.三者消耗原料相同 | B.甲消耗的原料最少 |
| C.乙消耗原料最少 | D.丙消耗原料最少 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】把2.7 g铝投入100 mL 3 mol·L-1的NaOH溶液中充分反应后,再滴入1 mol·L-1的盐酸溶液400 mL,其结果错误的是
| A.溶液显酸性 | B.得到澄清透明溶液 |
| C.得到浑浊溶液 | D.溶液中铝元素有两种微粒存在形式 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】化学与社会、生活密切相关,下列有关物质的用途和原理分析正确的是
| 选项 | 物质的用途 | 原理和分析 |
| A | 漂白粉可用于食品漂白 | 漂白粉能使色素褪色 |
| B | Al(OH)3可中和胃酸 | Al(OH)3是两性氢氧化物,与酸发生中和反应 |
| C | Na2O2常作供氧化 | Na2O2在常温下能分解放出O2 |
| D | 明矾可作净水剂 | 明矾溶于水后能消毒杀菌 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】取一定体积的两种试剂进行反应,改变两种试剂的滴加顺序(试剂浓度均为0.1mol/L),反应现象没有明显差别的是
| 选项 | 试剂① | ② |
| A | Na2CO3溶液 | 盐酸 |
| B | AlCl3溶液 | NaOH溶液 |
| C | AgNO3溶液 | 氨水 |
| D | Na2S2O3溶液 | H2SO4溶液 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
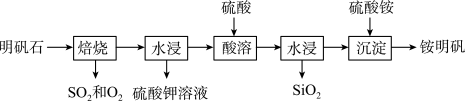
【推荐1】以高硫铝土矿(主要成分为 、
、 、
、 和少量
和少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下:
的部分工艺流程如下:

下列有关说法不正确的是
 、
、 、
、 和少量
和少量 )为原料,生产氧化铝并获得
)为原料,生产氧化铝并获得 的部分工艺流程如下:
的部分工艺流程如下:
下列有关说法不正确的是
A.步骤①,焙烧的目的是将 转化为 转化为 |
| B.步骤②,控制适当反应温度并不断搅拌,有利于提高铝、硅浸取率 |
C.步骤③,滤液中主要存在的阳离子有 、 、 |
D.步骤④,焙烧的反应为: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】钒是一种重要的合金元素,主要用于钢铁工业。以富钒炉渣(主要含FeV2O4,少量P2O5等杂质)为原料回收粗钒的流程如下,已知NH4VO3难溶于水。下列有关说法错误的是
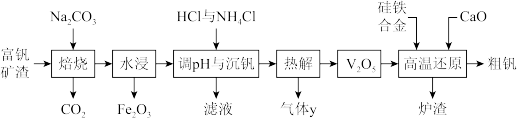

A.“焙烧”步骤中方程式为4FeV2O4+4Na2CO3+5O2 8NaVO3+2Fe2O3+4CO2 8NaVO3+2Fe2O3+4CO2 |
| B.“调pH与沉钒”步骤中磷元素以H3PO4的形式进入滤液中从而除杂 |
| C.“热解”步骤中气体产物为HCl |
| D.“高温还原”步骤中所得粗钒含有硅、铁杂质 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】用沉淀法除去粗盐中的 、Ca2+、Mg2+的操作为:称取一定质量的粗盐,放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌使粗盐完全溶解,向粗盐水中依次滴加过量的Na2CO3、BaCl2、NaOH溶液,静置,然后用玻璃棒引流至漏斗中过滤,向所得滤液中滴加盐酸直至没有气泡冒出,用胶头滴管吸取少量溶液滴在pH试纸上,测得滤液呈中性或微酸性,将滤液倒入坩埚中,用酒精灯加热,当出现较多固体并剩余少量水时停止加热,利用余热将滤液蒸干。实验中有几处错误?
、Ca2+、Mg2+的操作为:称取一定质量的粗盐,放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌使粗盐完全溶解,向粗盐水中依次滴加过量的Na2CO3、BaCl2、NaOH溶液,静置,然后用玻璃棒引流至漏斗中过滤,向所得滤液中滴加盐酸直至没有气泡冒出,用胶头滴管吸取少量溶液滴在pH试纸上,测得滤液呈中性或微酸性,将滤液倒入坩埚中,用酒精灯加热,当出现较多固体并剩余少量水时停止加热,利用余热将滤液蒸干。实验中有几处错误?
 、Ca2+、Mg2+的操作为:称取一定质量的粗盐,放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌使粗盐完全溶解,向粗盐水中依次滴加过量的Na2CO3、BaCl2、NaOH溶液,静置,然后用玻璃棒引流至漏斗中过滤,向所得滤液中滴加盐酸直至没有气泡冒出,用胶头滴管吸取少量溶液滴在pH试纸上,测得滤液呈中性或微酸性,将滤液倒入坩埚中,用酒精灯加热,当出现较多固体并剩余少量水时停止加热,利用余热将滤液蒸干。实验中有几处错误?
、Ca2+、Mg2+的操作为:称取一定质量的粗盐,放入烧杯中,加入适量蒸馏水,用玻璃棒搅拌使粗盐完全溶解,向粗盐水中依次滴加过量的Na2CO3、BaCl2、NaOH溶液,静置,然后用玻璃棒引流至漏斗中过滤,向所得滤液中滴加盐酸直至没有气泡冒出,用胶头滴管吸取少量溶液滴在pH试纸上,测得滤液呈中性或微酸性,将滤液倒入坩埚中,用酒精灯加热,当出现较多固体并剩余少量水时停止加热,利用余热将滤液蒸干。实验中有几处错误?| A.2处 | B.3处 | C.4处 | D.5处 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】海水中含有多种元素,开发利用这些资源是科学研究的重要课题。图为一种海水综合利用流程示意图。下列有关说法正确的是
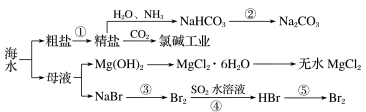

| A.要实现反应②可向NaHCO3溶液中加入过量石灰水 |
| B.溴元素在反应③、⑤中被氧化,在反应④中被还原 |
| C.工业上一般用金属钠与无水MgCl2反应制取Mg单质 |
| D.海水中含有碘元素,可将海水加热浓缩得到碘单质 |
您最近一年使用:0次

 +2H+=CO2↑+H2O
+2H+=CO2↑+H2O