A、B、C、D、E、F为短周期元素, 原子序数依次增大。非金属元素A 最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。E+与D2-具有相同的电子层结构。A单质在F单质中燃烧,产物溶于水得到一种强酸M。回答下列问题:
(1)画出E的离子结构示意图___________ 。
(2)F在周期表中的位置是___________ 。
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为___________ 。
(4)由这些元素组成的物质,相关信息如下:
①a的电子式为___________ 。 写出其与水反应的化学方程式:___________ 。
②b的一种常见用途为___________ 。
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为___________ 。
(1)画出E的离子结构示意图
(2)F在周期表中的位置是
(3)B、D、E组成的一种常见盐,其中D的质量分数约为 45%,该盐与少量M溶液反应的离子方程式为
(4)由这些元素组成的物质,相关信息如下:
| 物质 | 组成和结构信息 |
| a | 由 A、E组成的离子化合物 |
| b | 由D、E组成的含非极性键的离子化合物,阴阳离子数之比为1:2 |
| c | 化学式为BDF2的共价化合物 |
②b的一种常见用途为
③已知c中所有原子均满足8 电子稳定结构,该化合物的结构式为
更新时间:2024-05-08 12:53:29
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】有A、B、C、D四种元素,已知A元素原子的第一层和第三层电子数相同;B元素原子的第二层比第一层电子数多5个;C元素的+3价阳离子和氖原子具有相同的电子数;D元素的原子核外有4个电子层,第一层与第二层电子数之和等于第三层与第四层电子数之和。根据题意,完成下列填空:
(1)元素符号:A__ ,B__ ,C__ ,D___ 。
(2)A的原子结构示意图__ ,B的阴离子结构示意图___ ,C的阳离子结构示意图__ ,D的原子结构示意图__ 。
(1)元素符号:A
(2)A的原子结构示意图
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】有X、Y、Z、三种元素,X元素原子核内无中子,Y元素原子核内有8个质子,Z元素原子得到1个电子后与氩原子核外电子排布相同。
(1)写出X元素符号__________ ,画出Y元素的原子结构示意图___________ 。
(2)写出Z单质与X2Y反应化学方程式__________________________________ 。
(1)写出X元素符号
(2)写出Z单质与X2Y反应化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】A、B、C、D、E、F为短周期元素,其中C的原子序数最小,它们的最高正价与原子半径关系如图所示。

回答下列问题:
(1)F离子结构示意图为_______ ;化合物EF2的化学式为_______ 。
(2)从原子结构角度解释A金属性强于B的原因:_______ 。
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为_______ ,写出CE2在足量O2中燃烧的化学方程式_______ 。
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有_______ (填“离子键”、“极性键”或“非极性键”)。
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为_______ 。

回答下列问题:
(1)F离子结构示意图为
(2)从原子结构角度解释A金属性强于B的原因:
(3)CE2属于易燃易爆液体,严禁旅客携带,则CE2的结构式为
(4)化合物AD3常用于安全气囊,该化合物含有的化学键类型有
(5)在硝酸工业中,D的氢化物能发生催化氧化反应,写出该反应的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】用Cl2生产某些含氯有机物时会产生副产物HCl。利用反应A,可实现氯的循环利用。
反应A:4HCl+O2 2Cl2+2H2O
2Cl2+2H2O
已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。___________ 。
(2)反应A的热化学方程式是___________ (注意:不写条件)。
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为___________ kJ,H2O中H-O键比HCl中H-Cl键(填“强”或“弱”)___________ 。
(4)请回答:
H2(g)+Br2(l)=2HBr(g) ΔH=-72 kJ·mol-1,蒸发1mol Br2(1)需要吸收的能量为30kJ,则上表中a的数值为:___________ 。
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=___________ 。
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g) = -483.6 kJ·mol-1
= -483.6 kJ·mol-1
②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l) =-1366.8kJ·mol-1
=-1366.8kJ·mol-1
③H2O(l)=H2O(g) =+44.0kJ·mol-1
=+44.0kJ·mol-1
则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:___________ 。
反应A:4HCl+O2
 2Cl2+2H2O
2Cl2+2H2O已知:i.反应A中,4 mol HCl被氧化,放出115.6 kJ的热量。
ii.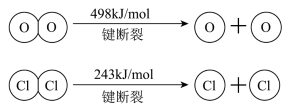
(2)反应A的热化学方程式是
(3)断开1 mol H-O键与断开1 mol H-Cl键所需能量相差为
(4)请回答:
| 参加反应的物质及状态 |  |  | 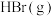 |
| 1mol分子中的化学键断裂时需要吸收的能量 | 436 | a | 369 |
(5)已知甲烷的燃烧热为890.3kJ·mol-1,H2O(g)=H2O(l) ΔH=-44.0kJ·mol-1,N2(g)+O2(g)=2NO(g) ΔH=+180.5kJ·mol-1,则甲烷脱硝反应:CH4(g)+2NO(g)+O2(g)=CO2(g)+N2(g)+2H2O(g) ΔH=
(6)二氧化碳经催化氢化可转化成绿色能源乙醇(CH3CH2OH)。已知:
①2H2(g)+O2(g)=2H2O(g)
 = -483.6 kJ·mol-1
= -483.6 kJ·mol-1②CH3CH2OH(l)+3O2(g)=2CO2(g)+3H2O(l)
 =-1366.8kJ·mol-1
=-1366.8kJ·mol-1③H2O(l)=H2O(g)
 =+44.0kJ·mol-1
=+44.0kJ·mol-1则二氧化碳与氢气转化成CH3CH2OH(l)和液态水的热化学方程式为:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】主族元素A、B、C、D的原子序数都小于18,A与D同主族,B与C在同一周期,A、D原子的最外层电子数都是1,C原子最外层电子数比B原子少2个,且C最外层电子数是次外层电子数的2倍。A、B单质在常温下均为气体,它们在高温下以体积比2∶1完全反应,生成物在常温下是液体。此液体与D单质能激烈反应生成A的单质。所得溶液滴入酚酞显红色,同时溶液中含有与氖原子的电子层结构相同的阳离子。回答下列问题:
(1)写出元素符号A______ ,B______ ,C______ ,D______ 。
(2)写出B与C在高温下完全反应后生成物的化学式______ ,电子式______ ,结构式______ 。
(3)用电子式表示B、D在高温下形成的化合物的电子式______ ,判断其中的化学键的类型______ 。
(4)写出一种有A、B、C、D组成的化合物的化学式______ 。
(1)写出元素符号A
(2)写出B与C在高温下完全反应后生成物的化学式
(3)用电子式表示B、D在高温下形成的化合物的电子式
(4)写出一种有A、B、C、D组成的化合物的化学式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】价类二维图是学习元素及其化合物知识的重要模型。它是以元素化合价为纵坐标,物质类别为横坐标的二维平面图像。如图为氯元素的价类二维图。___________ ,写出③的化学式___________ ,①中含有的化学键类型为___________ ,请用电子式表示物质⑤___________ 。
(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式___________ ,在该反应中浓盐酸体现了___________ 性。若制备标准状况下5.6L的物质②,则被氧化的HCl的质量为___________ 克。
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,生成无色无味的气体,还有白烟生成,写出反应方程式___________ 。若有1mol气体生成,转移电子数为___________ 个。

(2)写出实验室用二氧化锰固体与浓盐酸制备物质②的离子方程式
(3)管道工人通常用浓氨水检查输送②的管道是否漏气,生成无色无味的气体,还有白烟生成,写出反应方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】硫氰化钾(KSCN)常用于合成树脂、杀虫杀菌剂等,某实验小组用如图所示装置制备硫氰化钾。已知: 是一种难溶于水的无色液体,密度为1.26g/cm3;
是一种难溶于水的无色液体,密度为1.26g/cm3; 难溶于
难溶于 。
。

回答下列问题:
(1)制备 溶液:三颈烧瓶内盛有
溶液:三颈烧瓶内盛有 、水和催化剂,实验开始时,打开K1(K2处于关闭状态),点燃装置A处酒精灯,加热装置D(水浴),使装置A中产生的氨气缓缓通入三颈烧瓶中,反应至
、水和催化剂,实验开始时,打开K1(K2处于关闭状态),点燃装置A处酒精灯,加热装置D(水浴),使装置A中产生的氨气缓缓通入三颈烧瓶中,反应至 消失,反应方程式为
消失,反应方程式为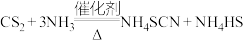 。
。
①装置A中发生反应的化学方程式为___________ ,装置A___________ (填“能”或“不能”)直接加热 固体制取氨气。
固体制取氨气。
②仪器B的名称是___________ ;装置C的作用是___________ 。
③三颈烧瓶左侧导管必须插入下层的 中,主要原因是
中,主要原因是___________ 。
④装置D中橡皮管的作用是___________ 。
(2)制备KSCN溶液:
①熄灭装置A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃, 完全分解后(反应方程式为
完全分解后(反应方程式为 ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为___________ 。
②装置E可用于尾气处理。已知酸性 溶液能将
溶液能将 氧化生成淡黄色沉淀,铬元素被还原为
氧化生成淡黄色沉淀,铬元素被还原为 ,写出其氧化
,写出其氧化 的离子方程式:
的离子方程式:___________ 。
 是一种难溶于水的无色液体,密度为1.26g/cm3;
是一种难溶于水的无色液体,密度为1.26g/cm3; 难溶于
难溶于 。
。
回答下列问题:
(1)制备
 溶液:三颈烧瓶内盛有
溶液:三颈烧瓶内盛有 、水和催化剂,实验开始时,打开K1(K2处于关闭状态),点燃装置A处酒精灯,加热装置D(水浴),使装置A中产生的氨气缓缓通入三颈烧瓶中,反应至
、水和催化剂,实验开始时,打开K1(K2处于关闭状态),点燃装置A处酒精灯,加热装置D(水浴),使装置A中产生的氨气缓缓通入三颈烧瓶中,反应至 消失,反应方程式为
消失,反应方程式为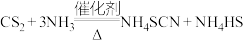 。
。①装置A中发生反应的化学方程式为
 固体制取氨气。
固体制取氨气。②仪器B的名称是
③三颈烧瓶左侧导管必须插入下层的
 中,主要原因是
中,主要原因是④装置D中橡皮管的作用是
(2)制备KSCN溶液:
①熄灭装置A处的酒精灯,关闭K1,移开水浴,将装置D继续加热至105℃,
 完全分解后(反应方程式为
完全分解后(反应方程式为 ),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为
),打开K2,继续保持溶液温度为105℃,缓缓滴入适量的KOH溶液,制得KSCN溶液。反应的化学方程式为②装置E可用于尾气处理。已知酸性
 溶液能将
溶液能将 氧化生成淡黄色沉淀,铬元素被还原为
氧化生成淡黄色沉淀,铬元素被还原为 ,写出其氧化
,写出其氧化 的离子方程式:
的离子方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】某研究小组为研究不同价态含硫物质的转化,设计实验如下,请回答有关问题。
[实验方案]按下图装置进行实验:

(1)A中发生反应的化学方程式______ 。
(2)B中品红溶液褪色,说明A中反应硫元素的价态由+6价转化为____ 价。
(3)C中出现淡黄色沉淀,反应中Na2S作_____ (填“氧化剂”或“还原剂”,下同),SO2作______ 。
(4)若D中有 生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有
生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有 生成的方法是
生成的方法是____ ,写出D中发生反应的离子方程式____ ,D中FeCl3试剂也可用____ (填序号)代替。
A.NaCl溶液 B.酸性KMnO4溶液 C.氯水 D.BaCl2溶液
(5)E的作用是_______ ,所发生反应的化学方程式为________ 。
[实验总结]硫元素“价类二维图”如下图:

(6)硫元素常见的化合价有−2、0、+4、+6,可以通过_______ (填反应类型,下同)反应实现不同价态含硫物质的相互转化;可以通过____ 反应实现同一价态不同类别含硫物质的相互转化。
[实验方案]按下图装置进行实验:

(1)A中发生反应的化学方程式
(2)B中品红溶液褪色,说明A中反应硫元素的价态由+6价转化为
(3)C中出现淡黄色沉淀,反应中Na2S作
(4)若D中有
 生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有
生成,则可说明硫元素的化合价由+4价转化为+6价,检验D中有 生成的方法是
生成的方法是A.NaCl溶液 B.酸性KMnO4溶液 C.氯水 D.BaCl2溶液
(5)E的作用是
[实验总结]硫元素“价类二维图”如下图:

(6)硫元素常见的化合价有−2、0、+4、+6,可以通过
您最近一年使用:0次
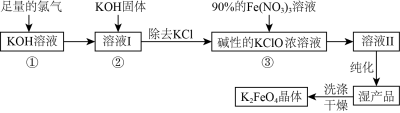
【推荐3】高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺流程如下:
(1)K2FeO4中铁元素在周期表中的位置第___________ 周期第___________ 列。
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
(3)“纯化”时需加入饱和的KOH溶液,其作用是___________ 。
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。每制得59.4 g K2FeO4,理论上消耗氧化剂的物质的量为___________ mol。
(5)工业上用异丙醇对湿产品进行洗涤,目的是___________ 。
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:___________ 。
(1)K2FeO4中铁元素在周期表中的位置第
(2)在溶液I中加入KOH固体的目的是___________(填字母)。
| A.为下一步反应提供碱性的环境 |
| B.使KClO3转化为KClO |
| C.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| D.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
(3)“纯化”时需加入饱和的KOH溶液,其作用是
(4)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为
(5)工业上用异丙醇对湿产品进行洗涤,目的是
(6)高铁酸钾(K2FeO4)作为水处理剂的一个优点是能与水反应生成胶体吸附杂质,写出该反应的离子方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】常温下由三种短周期元素形成的气体单质X、Y、Z,有下列转化关系(反应条件已略去):

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
化合物丙的电子式是___ ;化合物丙中存在的化学键为___ 、___ 。

已知:X分子中含共价键最多;甲分子中含10个电子,乙分子含有18个电子。
化合物丙的电子式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有A、B、C、D、E五种短周期元素,它们的原子序数依次增大,其中B是地壳中含量最多的元素;已知A、C及B、E分别是同主族元素,且B、E两元素原子核内质子数之和是A、C两元素原子核内质子数之和的2倍;处于同周期的C、D、E元素中,D是该周期金属元素中金属性最弱的元素。
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)__________________ >__________________ ;
(2)A、B、C形成的化合物的晶体类型为__________________ ;电子式为__________________ ;
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式__________________ ;
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式__________________ ;
(5)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的离子方程式__________________ .
(1)试比较C、D两元素最高价氧化物对应水化物碱性的强弱(填化学式)
(2)A、B、C形成的化合物的晶体类型为
(3)写出D单质与C元素最高价氧化物对应水化物反应的离子方程式
(4)写出两种均含A、B、C、E四种元素的化合物在溶液中相互反应、且生成气体的离子方程式
(5)通常条件下,C的最高价氧化物对应水化物2mol与E最高价氧化物对应水化物1mol的稀溶液间反应放出的热量为114.6kJ,试写出表示该热量变化的离子方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】已知X、Y、Z、W和T五种短周期主族元素,它们的原子序数依次增大。X原子中的电子只占据一个原子轨道。Y是地壳中含量最多的元素,T是海水中离子浓度最大的元素,W原子的最外层电子数是电子层数的2倍,Z原子的最外层s电子数比内层的s电子数少3个。根据以上信息填空:
(1)W元素的原子核外共有__ 种不同运动状态的电子;最外层电子排布式为__ ,T原子中电子云的形状有__ 种。
(2)由X、Y、T三种元素形成的化合物A具有漂白性。则A的电子式为__ 。
(3)Y、Z、W、T的简单离子的半径由大到小的顺序为(用离子符号表示)__ ;X2Y的沸点__ X2W的沸点(填“>”或“<”)。
(4)X、Y、W可形成两种带一个负电荷的双核阴离子,请写出两者之间发生反应的离子方程式为___ 。
(1)W元素的原子核外共有
(2)由X、Y、T三种元素形成的化合物A具有漂白性。则A的电子式为
(3)Y、Z、W、T的简单离子的半径由大到小的顺序为(用离子符号表示)
(4)X、Y、W可形成两种带一个负电荷的双核阴离子,请写出两者之间发生反应的离子方程式为
您最近一年使用:0次



