25 ℃、101 kPa下,1g甲醇燃烧生成CO2和液态水时放热22.69 kJ,下列热化学方程式正确的是
| A.CH3OH(l)+3/2O2(g)=CO2(g)+2H2O(l) ΔH=726kJ·mol-1 |
| B.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-1 452 kJ·mol-1 |
| C.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=-726 kJ·mol-1 |
| D.2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l) ΔH=1 452 kJ·mol-1 |
更新时间:2024-05-09 10:30:18
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】我国科研人员研究了不同含金催化剂催化乙烯加氢的反应历程如下图所示(已知反应:C2H4(g)+H2(g)=C2H6(g),△H=akJ·mol-1),下列说法错误的是
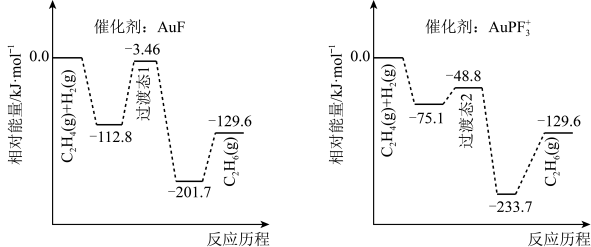

| A.1molC2H4(g)和1molH2(g)的键能之和比lmolC2H6(g)的键能大 |
| B.a=-129.6 |
| C.效果较好的催化剂是AuPF3+大 |
| D.稳定性:过渡态1<过渡态2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】如图是某条件下N2与H2反应过程中能量变化的曲线图.根据图象判断下列叙述中正确的是( )


A.该反应的热化学方程式为N2(g)+3H2(g) 2NH3(g) △H=+92kJ·mol﹣1 2NH3(g) △H=+92kJ·mol﹣1 |
| B.a曲线是加入催化剂时的能量变化曲线 |
| C.加入催化剂,该化学反应的反应热数值会减小 |
D.反应2NH3(g) N2(g)+3H2(g)△H=+92kJ·mol﹣1 N2(g)+3H2(g)△H=+92kJ·mol﹣1 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列方程式书写正确的是
A. 的电离方程式:Na2SO3 的电离方程式:Na2SO3 2Na++SO 2Na++SO |
B.NaHCO3水解的离子方程式:HCO +H2O +H2O CO CO + H3O+ + H3O+ |
C. 的电离方程式:H2S 的电离方程式:H2S H++HS-、HS- H++HS-、HS- H++S2- H++S2- |
D.热化学方程式: |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列有关中和热的说法正确的是
①表示中和热的热化学方程式为
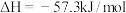
②准确测量中和热的整个实验过程中,至少测定2次温度
③测量中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
④ 的稀溶液和含
的稀溶液和含 的稀溶液反应的反应热
的稀溶液反应的反应热
⑤中和热测定:用 盐酸和
盐酸和 溶液进行实验,用量筒量取NaOH溶液时,仰视取液,测得的中和热数值偏小
溶液进行实验,用量筒量取NaOH溶液时,仰视取液,测得的中和热数值偏小
⑥中和热测定实验中为减少热量散失,NaOH溶液应分多次倒入量热计中
⑦用温度计测定盐酸溶液起始温度后未洗涤,直接测定氢氧化钠的温度会导致测得中和热的数值偏小
①表示中和热的热化学方程式为

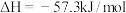
②准确测量中和热的整个实验过程中,至少测定2次温度
③测量中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小
④
 的稀溶液和含
的稀溶液和含 的稀溶液反应的反应热
的稀溶液反应的反应热
⑤中和热测定:用
 盐酸和
盐酸和 溶液进行实验,用量筒量取NaOH溶液时,仰视取液,测得的中和热数值偏小
溶液进行实验,用量筒量取NaOH溶液时,仰视取液,测得的中和热数值偏小⑥中和热测定实验中为减少热量散失,NaOH溶液应分多次倒入量热计中
⑦用温度计测定盐酸溶液起始温度后未洗涤,直接测定氢氧化钠的温度会导致测得中和热的数值偏小
| A.①③④⑥ | B.③④⑤⑦ | C.①③⑤⑦ | D.②③④⑥ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】已知1g氢气燃烧生成气态水放出 121 kJ的热量,下列热化学方程式正确的是
A.H2O(g)= H2(g)+  O2(g) △H = + 242kJ/mol O2(g) △H = + 242kJ/mol |
| B.2H2(g) + O2(g) = 2H2O(l) △H= —484 kJ/mol |
C.H2(g) +  O2(g) = H2O(g) △H= + 242 kJ/mol O2(g) = H2O(g) △H= + 242 kJ/mol |
| D.2H2(g) + O2(g) = 2H2O(g) △H= + 484 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用于汽车尾气净化的反应: ,在298K、100
,在298K、100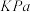 下,该反应的
下,该反应的 、
、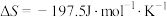 ,下列有关说法错误的是
,下列有关说法错误的是
 ,在298K、100
,在298K、100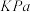 下,该反应的
下,该反应的 、
、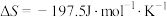 ,下列有关说法错误的是
,下列有关说法错误的是A.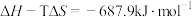 ,该反应在室温下能正向自发进行 ,该反应在室温下能正向自发进行 |
B.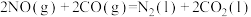  |
C.  |
D.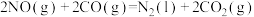  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关能量的叙述不正确的是( )
| A.活化能的大小对化学反应的能量变化不产生影响 |
| B.化学键的断裂和形成是化学反应中发生能量变化的主要原因 |
| C.HCl(aq)和NaOH(aq)反应的中和热为57.3kJ/mol,则CH3COOH(aq)和NaOH(aq)完全反应生成1molH2O(l)时,放出的热量为57.3kJ |
D.CO(g)的燃烧热是283.0kJ/mol,则反应2CO2(g)=2CO(g)+O2(g)的反应热 =+566.0kJ/mol =+566.0kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】有关能量的判断或表示方法正确的是
| A.由H+(aq)+OH-(aq)=H2O(l)△H=-57.3kJ/mol,可知:含1molCH3COOH的溶液与含1molNaOH的溶液混合,放出热量等于57.3kJ |
B.已知C2H6的燃烧热为1090kJ·mol-1,则C2H6燃烧的热化学方程式为:C2H6(g)+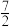 O2(g)=2CO2(g)+3H2O(l)ΔH=-1090kJ/mol O2(g)=2CO2(g)+3H2O(l)ΔH=-1090kJ/mol |
| C.2gH2完全燃烧生成液态水放出285.8kJ热量,则氢气燃烧的热化学方程式为:2H2(g)+O2(g)=2H2O(l)△H=-285.8kJ/mol |
| D.已知2CO(g)+O2(g)=2CO2(g)ΔH=-566kJ·mol-1,则CO的燃烧热ΔH=-283kJ |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】常温、常压下,4.8 g碳(石墨)在一定量的氧气中燃烧,反应完成后碳无剩余,共放出100 kJ的热量。【已知:碳的燃烧热∆H=-394 kJ/mol ;2C(石墨)+O2(g)═2CO(g)∆H=-221 kJ/mol】,则燃烧后的产物是
| A.CO2 | B.CO |
| C.CO2和CO | D.无法确定 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】甲烷和二氧化碳的催化重整是实现碳达峰、碳中和的重要研究项目。已知甲烷、一氧化碳、氢气的燃烧热分别是890.3 kJ/mol、283 kJ/mol、285.8 kJ/mol。则:CH4(g)+CO2(g)=2CO(g)+2H2(g) △H=
| A.-247.3 kJ/mol | B.+247.3 kJ/mol | C.-2027.9 kJ/mol | D.+2027.9 kJ/mol |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】2017年中国首次海域可燃冰(CH4·nH2O,密度ρ1 g·cm-3)试开采成功。若以辛烷代表汽油(密度ρ2 g·cm-3)的组成,下列说法不正确的是
① CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH1 = —a kJ·mol-1
② 2C8H18(l) + 25O2(g) =16CO2 (g) + 18H2O(l) ΔH 2 = —b kJ·mol-1
① CH4(g) + 2O2(g) =CO2(g) + 2H2O(l) ΔH1 = —a kJ·mol-1
② 2C8H18(l) + 25O2(g) =16CO2 (g) + 18H2O(l) ΔH 2 = —b kJ·mol-1
| A.可燃冰适宜保存在低温,高压的环境中 |
B.1 m3可燃冰可释放出标准状况下 m3的CH4 m3的CH4 |
| C.汽油的燃烧热约为0.5b kJ·mol-1 |
D.1m3可燃冰释放出的甲烷燃烧放出的热量约为等体积汽油的 倍 倍 |
您最近一年使用:0次


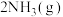
 。对于工业合成氨的反应,下列说法正确的是
。对于工业合成氨的反应,下列说法正确的是 液化分离有利于平衡正向移动
液化分离有利于平衡正向移动


