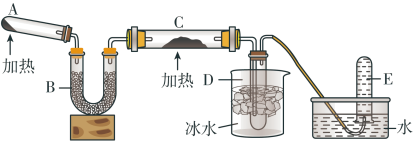
已知氨气具有还原性,可以与灼热的氧化铜反应生成两种单质和水,用下图中的装置可以实现该反应。
(1)A中加入的物质是两种固体,A中反应的化学方程式为______ 。
(2)仪器B中加入的物质是_______ (单选,填标号)。
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是_______ ,发生反应的化学方程式为________ 。
(4)D中收集到的物质是_______ (选填“液氨”或“氨水”);将酚酞溶液滴到该物质中,出现的现象是_______ ,用电离方程式解释出现该现象的原因________ 。
(5)金属镁在E中收集到的气体中燃烧的化学方程式为_______ 。
(1)A中加入的物质是两种固体,A中反应的化学方程式为
(2)仪器B中加入的物质是
a.碱石灰 b.无水氯化钙 c.无水硫酸铜 d.五氧化二磷
(3)实验时在C中观察到得现象是
(4)D中收集到的物质是
(5)金属镁在E中收集到的气体中燃烧的化学方程式为
更新时间:2024-05-12 22:06:30
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、X为中学化学常见物质,A、B、C含有相同的元素甲,已知甲元素是汽车尾气中含量最多的元素,它们可以发生如图转化(水未标出):
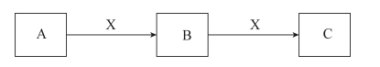
(1)若A为单质则其名称为_______ 。
(2)C物质的颜色为_______ 。
(3)若A为化合物,则A→B的化学方程式为_______ ,每生成1molB转移电子的物质的量为_______ 。
(4)C与水反应的化学方程式_______ 。

(1)若A为单质则其名称为
(2)C物质的颜色为
(3)若A为化合物,则A→B的化学方程式为
(4)C与水反应的化学方程式
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】如图是部分短周期元素的单质及其化合物的转化关系图(有关反应的条件及生成的H2O已略去).

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式_____________________ ;
(2)C的结构式__________________________ ;H为正盐,则H的化学式为____________________ ;
(3)L的溶液与化合物E反应的离子方程式:______________ ;
(4)化合物J的化学式____________________ .

已知:
(a)A、B、C、D是非金属单质,其中B、C、D在常温常压下是气体.
(b)反应①、②是化工生产中的重要反应.
(c)化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥.
(d)化合物L具有漂白性,可由Cl2与NaOH溶液反应而制得.
(e)化合物J由两种元素组成,其相对分子质量为32.
请按要求填空:
(1)反应③的化学方程式
(2)C的结构式
(3)L的溶液与化合物E反应的离子方程式:
(4)化合物J的化学式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】“空气中氧气体积分数的测定”有多种方法,请按要求回答下列问题:在燃烧匙内盛过量红磷,红磷必须过量的原因是______ ,点燃红磷后立即插入集气瓶内,塞紧橡皮塞红磷燃烧的现象是____________ ,其反应的化学方程式为____________________ 。待红磷火焰熄灭,集气瓶冷却至室温,打开止水夹,观察到的现象是______ ,该实验除了得出氧气在空气中的体积分数之外,还能得出氮气具有的性质是______ (任写一点);若测得空气中氧气的体积分数约为1/7,则可能的原因是______ 。


您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】某学习小组用氨催化氧化法(已知: )在实验室模拟制硝酸,设计如图2所示装置。
)在实验室模拟制硝酸,设计如图2所示装置。
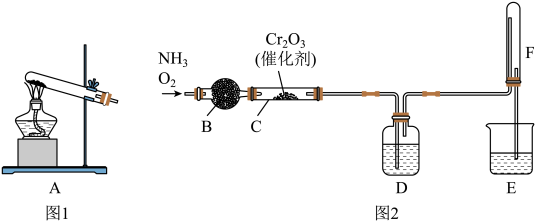
(1)写出实验室以图1装置A作发生装置制备氨气的化学方程式____________ 。
(2)仪器B的名称是____________ 。
(3)按图2所示连接好装置,首先____________ ,接着装好药品,按一定比例通入氧气、氨气,在催化剂、加热条件下反应一段时间,取少量E中溶液于试管中,滴加几滴紫色石蕊试液,观察到____________ 现象时,说明E中已制得硝酸。
(4)若没有装置D,可以观察到F中有白烟生成,则白烟成分是____________ (写化学式)。装置D盛放试剂是____________ (写名称),作用是____________ 。
(5)请指出图2模拟制备硝酸的装置可能存在的缺点是____________ 。
 )在实验室模拟制硝酸,设计如图2所示装置。
)在实验室模拟制硝酸,设计如图2所示装置。
(1)写出实验室以图1装置A作发生装置制备氨气的化学方程式
(2)仪器B的名称是
(3)按图2所示连接好装置,首先
(4)若没有装置D,可以观察到F中有白烟生成,则白烟成分是
(5)请指出图2模拟制备硝酸的装置可能存在的缺点是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】由一种短周期金属元素和一种短周期非金属元素组成的化合物X可与水发生复分解反应。某校兴趣小组用如图所示装置(夹持装置略去)对其进行探究实验。
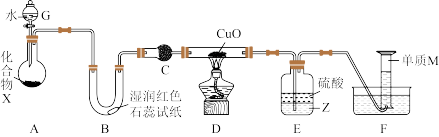
(1)仪器G的名称是_______ ,B中红色石蕊试纸变蓝,则单质M的电子式为_______ 。
(2)化合物X与水反应会生成一种白色沉淀,写出X与水反应的化学方程式:_______ 。
(3)C中的试剂名称为_______ 。
(4)实验时,装置D中硬质玻璃管内的现象为_______ 。
(5)装置E中试剂Z为_______ (填化学式),装置E的作用是_______ 。
(6)若装置A中固体样品含有杂质(杂质不参与反应),某同学通过测定F中单质M在标准状况下的体积和固体样品的质量,以确定固体样品中X的质量分数,判断该方案是否可行,并说明原因:_______ 。

(1)仪器G的名称是
(2)化合物X与水反应会生成一种白色沉淀,写出X与水反应的化学方程式:
(3)C中的试剂名称为
(4)实验时,装置D中硬质玻璃管内的现象为
(5)装置E中试剂Z为
(6)若装置A中固体样品含有杂质(杂质不参与反应),某同学通过测定F中单质M在标准状况下的体积和固体样品的质量,以确定固体样品中X的质量分数,判断该方案是否可行,并说明原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,其中A是单质,它们有如图所示转化关系。
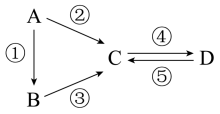
(1)若A是淡黄色固体,B为氢化物,常温下,D的浓溶液是一种无色黏稠油状液体。则反应③的化学方程式为_______ 。在加热条件下,D的浓溶液能与木炭发生反应生成C,D体现的性质为_______ 。
(2)若B是淡黄色固体,且②③的反应物中均有常温下为液态的一种物质。则反应③的化学反应方程式为_______ 。
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为_______ ;若C、D组成元素相同,且无其他元素参与相互转化,则C转化为D的离子方程式为_______ ;在D中滴入氢氧化钠溶液,一段时间内观察到的现象是_______ 。
(4)常温下,A、B、C、D均为气体;气体B溶于水显碱性;在雷雨天气,可发生反应②,则反应③的化学方程式为_______ ,D相对分子质量比C大16,则D为_______ (填化学式),在标准状况下将1.92 g铜粉投入一定量浓硝酸中,当铜粉完全溶解后共收集到标准况下1.12 L气体,则所得气体的化学式为_______ ,参加反应的硝酸为_______ mol。

(1)若A是淡黄色固体,B为氢化物,常温下,D的浓溶液是一种无色黏稠油状液体。则反应③的化学方程式为
(2)若B是淡黄色固体,且②③的反应物中均有常温下为液态的一种物质。则反应③的化学反应方程式为
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为
(4)常温下,A、B、C、D均为气体;气体B溶于水显碱性;在雷雨天气,可发生反应②,则反应③的化学方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】将二氧化碳转化为绿色液体燃料甲醇是实现碳中和的一个重要途径。甲醇的制备原理为: 。
。
(1)工业上利用低浓度氨水作为捕获剂,吸收烟气中过量 的离子方程式为
的离子方程式为_______ 。
(2)①甲醇的制备反应一般认为通过如下两步来实现:


根据盖斯定律,该反应的
_______  。
。
②按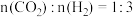 投料,不同催化剂作用下,反应
投料,不同催化剂作用下,反应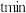 时,
时, 的产率随温度的变化如图所示,下列说法正确的是
的产率随温度的变化如图所示,下列说法正确的是_______ 。(填标号)

A. 的平衡常数K大于
的平衡常数K大于 的平衡常数K
的平衡常数K
B.使用催化剂I时,d点已达到平衡
C.若a点时, ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度
D.c点转化率比a点低的原因一定是催化剂活性降低
(3)已知反应 的
的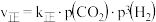 ,
,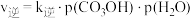 ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压
分别为正、逆反应速率常数,p为气体分压(分压 总压
总压 物质的量分数)。在
物质的量分数)。在 下,按初始投料比
下,按初始投料比 、
、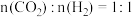 、
、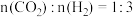 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:

①a、b、c各曲线所表示的投料比由大到小的顺序为_______ (用字母表示)。
②N点在b曲线上, 时的压强平衡常数
时的压强平衡常数
_______  (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。
③ 条件下,测得某时刻
条件下,测得某时刻 、
、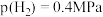 、
、 ,此时
,此时
_______ (保留两位小数)。
(4)我国科学家制备了一种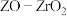 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(S)随温度的变化曲线如图。
选择性(S)随温度的变化曲线如图。
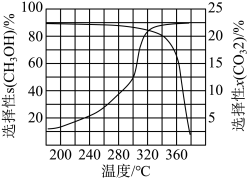
温度升高, 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:_______ 。
 。
。(1)工业上利用低浓度氨水作为捕获剂,吸收烟气中过量
 的离子方程式为
的离子方程式为(2)①甲醇的制备反应一般认为通过如下两步来实现:


根据盖斯定律,该反应的

 。
。②按
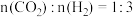 投料,不同催化剂作用下,反应
投料,不同催化剂作用下,反应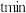 时,
时, 的产率随温度的变化如图所示,下列说法正确的是
的产率随温度的变化如图所示,下列说法正确的是
A.
 的平衡常数K大于
的平衡常数K大于 的平衡常数K
的平衡常数KB.使用催化剂I时,d点已达到平衡
C.若a点时,
 ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度D.c点转化率比a点低的原因一定是催化剂活性降低
(3)已知反应
 的
的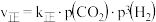 ,
,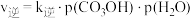 ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压
分别为正、逆反应速率常数,p为气体分压(分压 总压
总压 物质的量分数)。在
物质的量分数)。在 下,按初始投料比
下,按初始投料比 、
、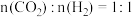 、
、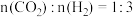 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
①a、b、c各曲线所表示的投料比由大到小的顺序为
②N点在b曲线上,
 时的压强平衡常数
时的压强平衡常数
 (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。③
 条件下,测得某时刻
条件下,测得某时刻 、
、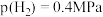 、
、 ,此时
,此时
(4)我国科学家制备了一种
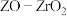 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(S)随温度的变化曲线如图。
选择性(S)随温度的变化曲线如图。
温度升高,
 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】有一瓶澄清的溶液,其中可能含有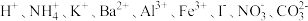 、
、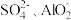 中的若干种。取该溶液进行以下实验:
中的若干种。取该溶液进行以下实验:
①用pH试纸检测,溶液呈强酸性;
②取溶液适量,加入少量 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;
③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性
b.溶液逐渐产生沉淀
c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝
④取适量③得到的碱性溶液,加入 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。
根据上述实验现象,回答下列问题:
(1)由①可以排除___________ 的存在。
(2)由②可以证明___________ 的存在;同时排除___________ 的存在。
(3)由③可以证明___________ 的存在;写出c、d所涉及的化学方程式,是离子反应的用离子方程式表示:c___________ ;d___________ 。
(4)由④可以排除___________ 的存在,同时证明___________ 的存在。
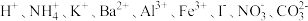 、
、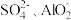 中的若干种。取该溶液进行以下实验:
中的若干种。取该溶液进行以下实验:①用pH试纸检测,溶液呈强酸性;
②取溶液适量,加入少量
 和数滴新制氯水,振荡,
和数滴新制氯水,振荡, 层呈紫红色;
层呈紫红色;③另取溶液适量,逐滴加入NaOH溶液;
a.溶液从酸性变为中性
b.溶液逐渐产生沉淀
c.沉淀完全溶解
d.最后加热溶液,有气体放出,该气体能使湿润的红色石蕊试纸变蓝
④取适量③得到的碱性溶液,加入
 溶液,有白色沉淀生成。
溶液,有白色沉淀生成。根据上述实验现象,回答下列问题:
(1)由①可以排除
(2)由②可以证明
(3)由③可以证明
(4)由④可以排除
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】研究氮的循环和转化对生产、生活有重要的价值。
I.(1)写出实验室制备氨气的化学方程式________ 。
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。
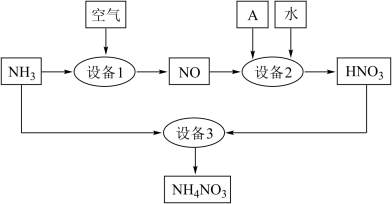
(2)设备1、3中发生反应的化学方程式分别是______ 、 ________ 。设备2中通入的物质A是________ 。
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在。某工厂处理氨氮废水的流程如下:

(3)过程①的目的是将NH4+转化为NH3,并通过鼓入大量空气将氨气吹出,写出NH4+转化为NH3的离子方程式________ 。
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为___ 、_______ 。
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序号)_________ 。
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出其中一个反应的离子方程式__________ 。
I.(1)写出实验室制备氨气的化学方程式
II.氨是重要的化工原料。某工厂用氨制硝酸和铵盐的流程如下图所示。

(2)设备1、3中发生反应的化学方程式分别是
III.氨氮废水的去除是当前科学研究的热点问题。氨氮废水中的氮元素多以NH4+和NH3•H2O的形式存在。某工厂处理氨氮废水的流程如下:

(3)过程①的目的是将NH4+转化为NH3,并通过鼓入大量空气将氨气吹出,写出NH4+转化为NH3的离子方程式
(4)过程②加入NaClO溶液可将氨氮转化为无毒物质,反应后含氮元素、氯元素的物质化学式分别为
(5)含余氯废水的主要成分是NaClO以及HClO,X可选用以下哪种溶液以达到去除余氯的目的(填序号)
a.KOH b.Na2SO3 c.KMnO4 d.NaCl
写出其中一个反应的离子方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】硫氰化钾(KSCN)俗称玫瑰红酸钾,是一种用途广泛的化学药品。实验室模拟工业制备硫氰氯化钾的实验装置如下图所示:

已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;
②三颈烧瓶内盛放:CS2、水和催化剂;
③ ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。
回答下列问题:
(1)装置A中反应的化学方程式是_______ 。
(2)装置C的作用是_______ 。
(3)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,水浴加热,保持三颈烧瓶内液温95℃一段时间,然后打开K2,继续保持液温95℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的化学方程式:_______ 。
(4)已知,酸性 可以把氨气氧化为无色无味的气体。装置
可以把氨气氧化为无色无味的气体。装置 的作用为吸收尾气,防止污染环境,写出吸收NH3时的离子方程式
的作用为吸收尾气,防止污染环境,写出吸收NH3时的离子方程式_______ 。
(5)测定晶体中KSCN的含量:称取 品配成
品配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 溶液作指示剂,用
溶液作指示剂,用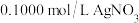 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 ,标准溶液
,标准溶液 。
。
已知:滴定时发生的反应: (白色)。
(白色)。
①晶体中KSCN的质量分数为_______ 。
②滴定达到终点后,发现滴定管尖嘴部分有悬滴,则KSCN的质量分数_______ 。(“偏大”、“偏小”或“无影响”)

已知:①NH3不溶于CS2,CS2密度比水大且不溶于水;
②三颈烧瓶内盛放:CS2、水和催化剂;
③
 ,该反应比较缓慢且
,该反应比较缓慢且 在高于170℃易分解。
在高于170℃易分解。回答下列问题:
(1)装置A中反应的化学方程式是
(2)装置C的作用是
(3)制备KSCN溶液:熄灭A处的酒精灯,关闭K1,水浴加热,保持三颈烧瓶内液温95℃一段时间,然后打开K2,继续保持液温95℃,缓缓滴入适量的KOH溶液,写出装置D中生成KSCN的化学方程式:
(4)已知,酸性
 可以把氨气氧化为无色无味的气体。装置
可以把氨气氧化为无色无味的气体。装置 的作用为吸收尾气,防止污染环境,写出吸收NH3时的离子方程式
的作用为吸收尾气,防止污染环境,写出吸收NH3时的离子方程式(5)测定晶体中KSCN的含量:称取
 品配成
品配成 溶液,量取
溶液,量取 溶液于锥形瓶中,加入适量稀硝酸,再加入几滴
溶液于锥形瓶中,加入适量稀硝酸,再加入几滴 溶液作指示剂,用
溶液作指示剂,用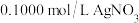 标准溶液滴定,达到滴定终点时消耗
标准溶液滴定,达到滴定终点时消耗 ,标准溶液
,标准溶液 。
。已知:滴定时发生的反应:
 (白色)。
(白色)。①晶体中KSCN的质量分数为
②滴定达到终点后,发现滴定管尖嘴部分有悬滴,则KSCN的质量分数
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】氯、氮、硫等及其化合物性质研究。如图是氮、硫元素的各种价态与物质类别的对应关系:
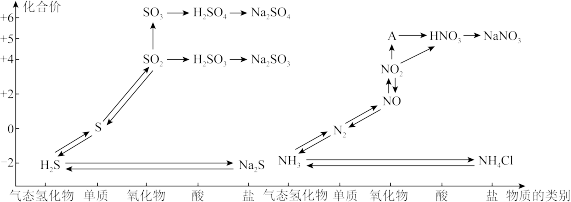
(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为____ 。
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式____ 。
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O 2HNO2
2HNO2
c.HClO+HNO2=HNO3+HCl
下列分析正确的是___ 。
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:
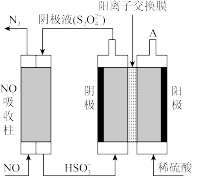
从A口中出来的物质的是____ 。写出电解池阴极的电极反应式____ 。
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
①上述实验中a=____ ,b=____ 。
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是____ (填实验编号)。
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质 NH3
NH3 HNO2
HNO2 HNO3
HNO3 N2
N2
请回答:
①过程Ⅲ发生反应的化学方程式为____ 。
②根据图1和图2,判断使用亚硝化菌的最佳条件为_______ 。
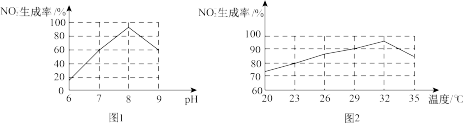
③利用微生物处理含氮废水的优点为_______ 。
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:_______ 。

(6)下图为制取氨气的装置和选用的试剂,其中错误的是_______ (填字母)。

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是_______ ,为了得到干燥的NH3,可用_______ 做干燥剂。若有5.35g氯化铵参加反应,则产生的气体在标准状况下的体积为_______ L。
(8)铵盐受热易分解,如图所示。
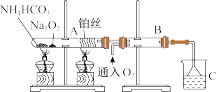
被加热的铂丝处发生反应的化学方程式为_______ 。

(1)工业上把海水先进行氧化,再吸收溴,达到富集溴的目的。吸收工艺常用的方法是先用热空气吹出Br2,再用SO2吸收Br2。写出SO2吸收Br2反应的离子方程式为
(2)氮氧化物的治理是当前生态环境保护中的重要课题之一。
①从原理上看,NH3可用于治理NO2,该反应在催化剂条件下可实现,其中有一种产物是空气的主要成分,写出化学方程式
②次氯酸盐也可用于脱除NO,主要过程如下:
a.NO+HClO=NO2+HCl
b. NO+NO2+H2O
 2HNO2
2HNO2 c.HClO+HNO2=HNO3+HCl
下列分析正确的是
A.NO2单独存在不能被次氯酸盐脱除
B.烟气中含有的少量的O2能提高NO的脱除率
C.脱除过程中,次氯酸盐溶液的酸性增强
③电解氧化吸收法:其原理如图所示:

从A口中出来的物质的是
(3)一种新型催化剂能使NO和CO发生反应2NO+2CO
 2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:
2CO2+N2。为验证温度和催化剂的比表面积对化学反应速率的影响规律,某同学设计了如表三组实验。回答下列问题:| 实验编号 | T(℃) | NO初始浓度(mol/L) | CO初始浓度(mol/L) | 催化剂的比表面积(m2/g) |
| I | 280 | 1.20×10-3 | 5.80×10-3 | 82 |
| II | 280 | 1.20×10-3 | b | 124 |
| III | 350 | a | 5.80×10-3 | 82 |
②上述实验中,能验证温度对化学反应速率影响规律的一组实验是
(4)氮及其化合物是重要的化工原料。含氮废水会加速藻类和其他浮游生物的大量繁殖,使水质恶化。利用微生物对含氮废水进行处理的流程如下:
蛋白质
 NH3
NH3 HNO2
HNO2 HNO3
HNO3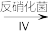 N2
N2请回答:
①过程Ⅲ发生反应的化学方程式为
②根据图1和图2,判断使用亚硝化菌的最佳条件为
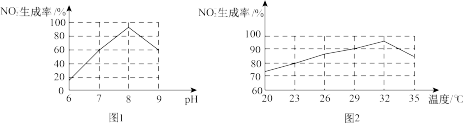
③利用微生物处理含氮废水的优点为
(5)肼(N2H4)暴露在空气中容易爆炸,但利用其制作的燃料电池是一种理想的电池,具有容量大、能量转化率高、产物无污染等优点,其工作原理如图所示,写出该电池的正极反应式:

(6)下图为制取氨气的装置和选用的试剂,其中错误的是

A. ①② B. ②③ C. ③④ D. ①③
(7)实验室制备氨气的化学反应方程式是
(8)铵盐受热易分解,如图所示。
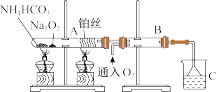
被加热的铂丝处发生反应的化学方程式为
您最近一年使用:0次



