将二氧化碳转化为绿色液体燃料甲醇是实现碳中和的一个重要途径。甲醇的制备原理为: 。
。
(1)工业上利用低浓度氨水作为捕获剂,吸收烟气中过量 的离子方程式为
的离子方程式为_______ 。
(2)①甲醇的制备反应一般认为通过如下两步来实现:


根据盖斯定律,该反应的
_______  。
。
②按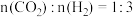 投料,不同催化剂作用下,反应
投料,不同催化剂作用下,反应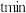 时,
时, 的产率随温度的变化如图所示,下列说法正确的是
的产率随温度的变化如图所示,下列说法正确的是_______ 。(填标号)

A. 的平衡常数K大于
的平衡常数K大于 的平衡常数K
的平衡常数K
B.使用催化剂I时,d点已达到平衡
C.若a点时, ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度
D.c点转化率比a点低的原因一定是催化剂活性降低
(3)已知反应 的
的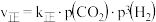 ,
,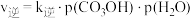 ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压
分别为正、逆反应速率常数,p为气体分压(分压 总压
总压 物质的量分数)。在
物质的量分数)。在 下,按初始投料比
下,按初始投料比 、
、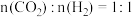 、
、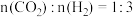 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:

①a、b、c各曲线所表示的投料比由大到小的顺序为_______ (用字母表示)。
②N点在b曲线上, 时的压强平衡常数
时的压强平衡常数
_______  (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。
③ 条件下,测得某时刻
条件下,测得某时刻 、
、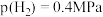 、
、 ,此时
,此时
_______ (保留两位小数)。
(4)我国科学家制备了一种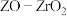 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(S)随温度的变化曲线如图。
选择性(S)随温度的变化曲线如图。
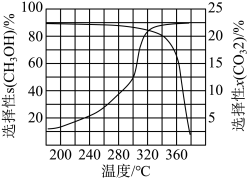
温度升高, 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:_______ 。
 。
。(1)工业上利用低浓度氨水作为捕获剂,吸收烟气中过量
 的离子方程式为
的离子方程式为(2)①甲醇的制备反应一般认为通过如下两步来实现:


根据盖斯定律,该反应的

 。
。②按
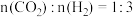 投料,不同催化剂作用下,反应
投料,不同催化剂作用下,反应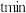 时,
时, 的产率随温度的变化如图所示,下列说法正确的是
的产率随温度的变化如图所示,下列说法正确的是
A.
 的平衡常数K大于
的平衡常数K大于 的平衡常数K
的平衡常数KB.使用催化剂I时,d点已达到平衡
C.若a点时,
 ,则此条件下反应已达到最大限度
,则此条件下反应已达到最大限度D.c点转化率比a点低的原因一定是催化剂活性降低
(3)已知反应
 的
的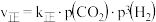 ,
,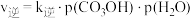 ,其中
,其中 、
、 分别为正、逆反应速率常数,p为气体分压(分压
分别为正、逆反应速率常数,p为气体分压(分压 总压
总压 物质的量分数)。在
物质的量分数)。在 下,按初始投料比
下,按初始投料比 、
、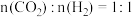 、
、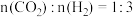 ,得到不同压强条件下
,得到不同压强条件下 的平衡转化率关系图:
的平衡转化率关系图:
①a、b、c各曲线所表示的投料比由大到小的顺序为
②N点在b曲线上,
 时的压强平衡常数
时的压强平衡常数
 (用平衡分压代替平衡浓度计算)。
(用平衡分压代替平衡浓度计算)。③
 条件下,测得某时刻
条件下,测得某时刻 、
、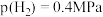 、
、 ,此时
,此时
(4)我国科学家制备了一种
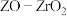 催化剂,实现
催化剂,实现 高选择性合成
高选择性合成 。气相催化合成过程中,
。气相催化合成过程中, 转化率(x)及
转化率(x)及 选择性(S)随温度的变化曲线如图。
选择性(S)随温度的变化曲线如图。
温度升高,
 转化率升高,但产物
转化率升高,但产物 含量降低的原因:
含量降低的原因:
更新时间:2023-04-26 15:40:42
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】已知氨气极易溶解于水:在加热条件下氨气可与灼热的氧化铜反应,产物为氮气、水和金属铜。用如图的装置可以实现该反应(加持装置已略去)。回答下列问题:

(1)写出实验室制取氨气的化学方程式_______ 。
(2)B中加入的物质的名称是______ ,其作用是______ 。
(3)实验结束后在D中收集到的物质为______ (填“酸性”、“中性”,“碱性”),E中收集到气体的电子式为______ 。

(1)写出实验室制取氨气的化学方程式
(2)B中加入的物质的名称是
(3)实验结束后在D中收集到的物质为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】氨气广泛应用于化工、轻工、化肥、制药、合成纤维等领域。同学们利用下图装置探究氨气的制备和性质。回答以下问题:
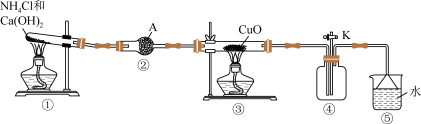
(1)装置①中反应化学方程式为_______ 。
(2)装置②中的A药品是_______ ;装置⑤的作用是吸收尾气,用倒扣水面上的漏斗代替直接插入水中的导管,其目的是_______ 。
(3)先加热装置①中的酒精灯,检验氨气已经充满整个装置的方法是:用玻璃棒蘸取漏斗口附近的溶液少许,_______ (补充完实验)。
(4)然后用酒精灯加热装置③,观察到黑色固体逐渐变红,预测固体产物有哪些可能?_______ 。装置④中气体仍为无色,利用装置设计实验证明没有产生NO,操作与现象是_______ 。据此分析,该实验的目的是检验NH3的_______ 性。

(1)装置①中反应化学方程式为
(2)装置②中的A药品是
(3)先加热装置①中的酒精灯,检验氨气已经充满整个装置的方法是:用玻璃棒蘸取漏斗口附近的溶液少许,
(4)然后用酒精灯加热装置③,观察到黑色固体逐渐变红,预测固体产物有哪些可能?
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】煤燃烧产生的粉煤灰(主要含有SiO2、Fe2O3、Al2O3等)是火电厂产生的废渣,若不加处理会污染环境。为综合利用,研究人员对其进行如下处理:

(1)滤渣主要成分是________________ ;滤液①中的阳离子为_____________________ 。
(2)滤液①中还加入还原剂原因是________________ ;若加入的还原剂为铁粉,反应的离子方程式为_____________________________________ 。
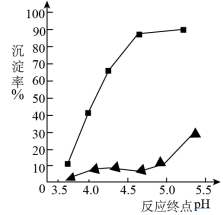
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为_________________ ;反应终点的pH对铝和铁分离效果的影响如右图。根据实验结果,为达到好的分离效果,反应过程中控制pH的范围是__________ ,选择该范围的理由是_________ 。
(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是_____________ 。
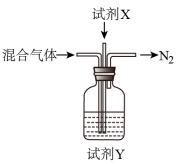
②煅烧NH4Al(SO4) 2时发生4NH4Al(SO4)2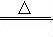 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是___________ (填化学式);试剂Y是_________ (填名称),其中溶质的物质的量为_____________ 。

(1)滤渣主要成分是
(2)滤液①中还加入还原剂原因是
(3)加入氨水是为了调节pH使铝离子沉淀,其离子方程式为

(4)NH4HSO4和H2SO4按物质的量比1:1混合溶于水配制成浸取液,220℃时可将高铝粉煤灰中Al2O3转化为硫酸铝铵[NH4Al(SO4) 2],然后分离、煅烧获得纯Al2O3。
查阅资料知硫酸铝铵:①溶解度:0℃时,S=5.2g;100℃时,S=421.9g 。②280℃时分解。
①依据资料可知,将硫酸铝铵与其他溶质分离的方法是
②煅烧NH4Al(SO4) 2时发生4NH4Al(SO4)2
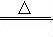 2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
2Al2O3+5SO3↑+3SO2↑+2NH3↑+N2↑+5H2O↑,得到混合气体(NH3、N2、SO2、SO3、H2O )。若16mol混合气体按如下装置被完全吸收制得浸取液。则右下图中,试剂X是
您最近一年使用:0次
【推荐1】石油裂解产生的乙烯含有0.5%~3%乙炔,乙炔在Ziegler-Natta催化剂中会使乙烯聚合失活。乙炔选择性加氢已经被证明是提纯乙烯最有效的技术之一。回答下列问题:
(1)已知25℃、101kPa下,相关物质的燃烧热数据如下表:
乙炔半氢化反应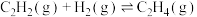 的
的 =
=_____________ 。
(2)在其他条件相同时,在不同的Pd基催化剂作用下,乙炔的转化率及乙烯的选择性随反应温度的变化如图a、b所示。已知:乙烯的选择性=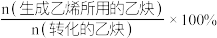 。
。______________ 。
②为保证该转化过程,需要过量的氢气,缺点是________________ 。
③某温度下,在刚性容器中发生乙炔半氢化反应,已知 与
与 的初始投料比[
的初始投料比[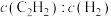 ]为1∶10,
]为1∶10, 的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为
的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为 ;则平衡时体系的压强=
;则平衡时体系的压强=___________ (用 列出计算式即可,下同);该反应的平衡常数
列出计算式即可,下同);该反应的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)
④制备基于MOFs(金属有机框架)薄膜材料为 /
/ 混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将
混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将 “固定”,能高效选择性吸附
“固定”,能高效选择性吸附 ,原理示意如图。
,原理示意如图。 最接近的是
最接近的是__________ 。(填标号)
A.利用 萃取碘水
萃取碘水
B.利用“杯酚”分离 和
和
C.利用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
(3)在工业领域也可用N,N-二甲基甲酰胺(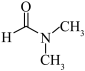 )粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
)粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是__________________________ 。
(1)已知25℃、101kPa下,相关物质的燃烧热数据如下表:
物质 |
|
|
|
燃烧热(△H)/ | -1299.6 | -285.8 | -1411.0 |
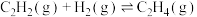 的
的 =
=(2)在其他条件相同时,在不同的Pd基催化剂作用下,乙炔的转化率及乙烯的选择性随反应温度的变化如图a、b所示。已知:乙烯的选择性=
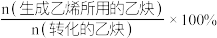 。
。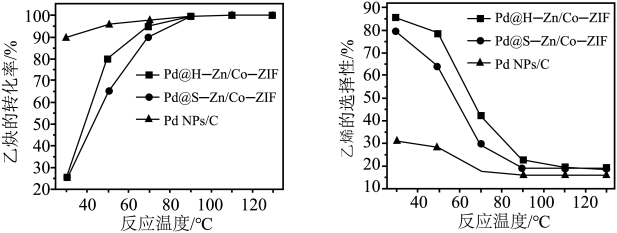
图a 图b
①若在实际生产中,选择Pd@H-Zn/Co-ZIF催化剂、50~60℃的反应条件,其依据是:②为保证该转化过程,需要过量的氢气,缺点是
③某温度下,在刚性容器中发生乙炔半氢化反应,已知
 与
与 的初始投料比[
的初始投料比[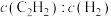 ]为1∶10,
]为1∶10, 的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为
的平衡转化率为90%(忽略其他副反应的发生)。若初始的总压强为 ;则平衡时体系的压强=
;则平衡时体系的压强= 列出计算式即可,下同);该反应的平衡常数
列出计算式即可,下同);该反应的平衡常数
④制备基于MOFs(金属有机框架)薄膜材料为
 /
/ 混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将
混合气体分离提供了一种经济高效的技术。该材料孔径大小和形状恰好将 “固定”,能高效选择性吸附
“固定”,能高效选择性吸附 ,原理示意如图。
,原理示意如图。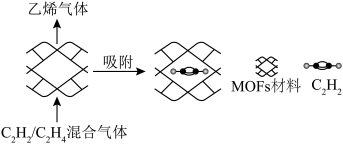
 最接近的是
最接近的是A.利用
 萃取碘水
萃取碘水B.利用“杯酚”分离
 和
和
C.利用饱和碳酸钠溶液除去乙酸乙酯中的少量乙酸
(3)在工业领域也可用N,N-二甲基甲酰胺(
 )粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
)粗乙烯中回收乙炔。N,N-二甲基甲酰胺是极性亲水性溶剂,其可与水任意比互溶的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题
(1)已知:①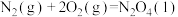
 kJ⋅mol
kJ⋅mol
②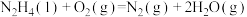
 kJ⋅mol
kJ⋅mol ;
;
写出液态肼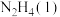 和
和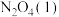 反应生成
反应生成 和水蒸气的热化学方程式:
和水蒸气的热化学方程式:__________________ 。
(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
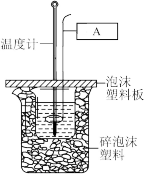
①中和热的测定装置如图所示。图中A的仪器名称:____________ 。
②用相同浓度和体积的氨水( )代替NaOH溶液进行上述实验,测得的中和热的数值会
)代替NaOH溶液进行上述实验,测得的中和热的数值会______ (填“偏大”、“偏小”、“无影响”)。
(3)CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol的CO和0.3 mol的 ,在催化剂存在和800℃的条件下加热,发生如下反应:
,在催化剂存在和800℃的条件下加热,发生如下反应: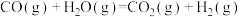
 ,反应中
,反应中 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:
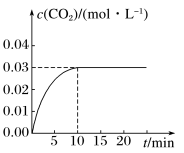
①根据图上数据,该温度(800℃)下的平衡常数
______ 。
②在催化剂存在和800℃的条件下,在某一时刻测得 mol⋅L
mol⋅L ;
;
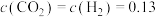 mol⋅L
mol⋅L ,则此时正、逆反应速率的大小:
,则此时正、逆反应速率的大小:
______  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
Ⅱ.还原法炼铅,包含反应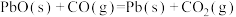
 ,该反应的平衡常数的对数值与温度的关系如表:
,该反应的平衡常数的对数值与温度的关系如表:
③当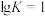 ,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为______ (保留两位有效数字);若向容器中充入一定量的CO气体后,平衡发生移动,再次达到平衡时,CO的百分含量______ (填“增大”“减小”或“不变”)。
(1)已知:①
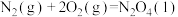
 kJ⋅mol
kJ⋅mol
②
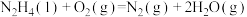
 kJ⋅mol
kJ⋅mol ;
;写出液态肼
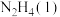 和
和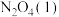 反应生成
反应生成 和水蒸气的热化学方程式:
和水蒸气的热化学方程式:(2)用50 mL 0.50 mol/L盐酸与50 mL 0.55 mol/L NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:

①中和热的测定装置如图所示。图中A的仪器名称:
②用相同浓度和体积的氨水(
 )代替NaOH溶液进行上述实验,测得的中和热的数值会
)代替NaOH溶液进行上述实验,测得的中和热的数值会(3)CO用途广泛,工业应用时离不开平衡思想的指导:
Ⅰ.在某一容积为5 L的体积不变的密闭容器内,加入0.3 mol的CO和0.3 mol的
 ,在催化剂存在和800℃的条件下加热,发生如下反应:
,在催化剂存在和800℃的条件下加热,发生如下反应: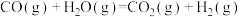
 ,反应中
,反应中 的浓度随时间变化情况如图:
的浓度随时间变化情况如图:
①根据图上数据,该温度(800℃)下的平衡常数

②在催化剂存在和800℃的条件下,在某一时刻测得
 mol⋅L
mol⋅L ;
;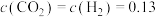 mol⋅L
mol⋅L ,则此时正、逆反应速率的大小:
,则此时正、逆反应速率的大小:
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。Ⅱ.还原法炼铅,包含反应
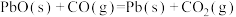
 ,该反应的平衡常数的对数值与温度的关系如表:
,该反应的平衡常数的对数值与温度的关系如表:| 温度/℃ | 300 | 727 | 1227 |
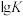 | 6.17 | 2.87 | 1.24 |
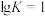 ,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
,在恒容密闭容器中放入PbO并通入CO,达平衡时,混合气体中CO的体积分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】习近平主席在《中央城镇化工作会议》发出号召:“让居民望得见山、看得见水、记得住乡愁” 。消除含氮、硫、氯等化合物对大气和水体的污染对建设美丽家乡,打造宜居环境具有重要意义。
(1)以HCl为原料,用O2氧化制取Cl2,可提高效益,减少污染。反应为:4HCl(g) + O2(g)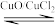 2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
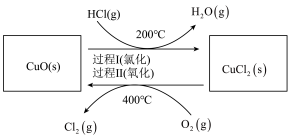
过程I的反应为:2HCl(g) + CuO (s) CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程Ⅱ反应的热化学方程式为
CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程Ⅱ反应的热化学方程式为___________ 。
(2)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g) ⇌N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。
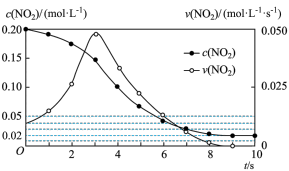
①0~3s内,甲容器中NO2的反应速率增大的原因是______________________ 。
②甲达平衡时,温度若为T℃,此温度下的平衡常数K=____________________ 。
③平衡时,K甲_____ K乙,P甲_____ P乙(填“>”、“<”或“=”)。
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①可用次氯酸钠除去氨氮,同时产生一种大气组成的气体。写出总反应化学方程式:___________ 。
②EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图所示。则阴极附近Fe2+参与反应的离子方程式为______ 。

(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1 mol· L −1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为_________________ 。(已知25℃时:H2SO3的电离常数Ka1=1.3×10−2,Ka2=6.2×10−8)
(1)以HCl为原料,用O2氧化制取Cl2,可提高效益,减少污染。反应为:4HCl(g) + O2(g)
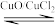 2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
2Cl2(g) + 2H2O(g) ∆H = −115.4 kJ·mol−1,通过控制合适条件,分两步循环进行,可使HCl转化率接近100%。原理如图所示:
过程I的反应为:2HCl(g) + CuO (s)
 CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程Ⅱ反应的热化学方程式为
CuCl2(s) + H2O(g) ∆H1 = −120.4 kJ·mol−1,过程Ⅱ反应的热化学方程式为(2)容积均为1L的甲、乙两个容器,其中甲为绝热容器,乙为恒温容器.相同温度下,分别充入0.2mol的NO2,发生反应:2NO2(g) ⇌N2O4(g) ∆H<0,甲中NO2的相关量随时间变化如图所示。

①0~3s内,甲容器中NO2的反应速率增大的原因是
②甲达平衡时,温度若为T℃,此温度下的平衡常数K=
③平衡时,K甲
(3)水体中过量氨氮(以NH3表示)会导致水体富营养化。
①可用次氯酸钠除去氨氮,同时产生一种大气组成的气体。写出总反应化学方程式:
②EFH2O2FeOx法可用于水体中有机污染物降解,其反应机理如图所示。则阴极附近Fe2+参与反应的离子方程式为

(4)工业上可用Na2SO3溶液吸收法处理SO2,25℃时用1 mol· L −1的Na2SO3溶液吸收SO2,当溶液pH=7时,溶液中各离子浓度的大小关系为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】氢气是工业上重要的原料。
(1)氢气用于工业合成氨 N2(g) + 3H2(g) 2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。
① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5﹑t7时刻所对应的实验条件改变分别是t4_________ 、t5__________ 、t7______ 。

②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后,测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为____________ 。
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g) H2(g) + CO(g) △H= +131.3 kJ/mol
H2(g) + CO(g) △H= +131.3 kJ/mol
①该反应在低温下不能自发进行的原因是__________________________________ 。
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度( ) 。
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol碘化氢及bmol碘化氢(a>b)待反应:2HI(g) H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A_______ c(I2)B ;平衡时HI的分解率αA______ αB ;平衡时H2在混合气体中的体积分数A______ B (填写“>”“<”“=”)。
(1)氢气用于工业合成氨 N2(g) + 3H2(g)
 2NH3(g);ΔH = -92.2 kJ·mol-1。
2NH3(g);ΔH = -92.2 kJ·mol-1。① 一定温度下,在容积恒定的密闭容器中,一定量的N2和H2反应达到平衡后,改变某一外界条件,反应速率与时间的关系如下图所示,其中t4 ﹑t5﹑t7时刻所对应的实验条件改变分别是t4

②温度为T℃时,将2amolH2和amolN2放入0.5L密闭容器中,充分反应后,测得N2的转化率为50﹪,此时放出热量46.1 kJ。则该温度下反应的平衡常数为
(2)工业上大量的氢气来源于焦炭与水蒸气高温下的反应:
C(s) + H2O(g)
 H2(g) + CO(g) △H= +131.3 kJ/mol
H2(g) + CO(g) △H= +131.3 kJ/mol①该反应在低温下不能自发进行的原因是
②恒温,在容积可变的密闭容器中,进行如上可逆反应。一段时间后,下列物理量不发生变化时,能表明该反应已达到平衡状态的有:Ⅰ混合气体的密度;Ⅱ容器内气体的压强;Ⅲ混合气体的总物质的量; ⅣCO物质的量浓度
A.只有Ⅳ B.只有Ⅰ和Ⅳ C.只有Ⅱ和Ⅲ
D.Ⅰ、Ⅲ和Ⅳ E.都可以
(3)在容积相同的两密闭容器A和B中,保持温度为423K,同时向A、B中分别加入amol碘化氢及bmol碘化氢(a>b)待反应:2HI(g)
 H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A
H2(g)+I2(g) 达到平衡后,平衡时I2的浓度c(I2)A
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g) 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。

①图中A点时,SO2的转化率为___________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正___________ v(A)逆(填“>”“<”或 “=”)。
③图中B点的压强平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用___________ 法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为___________ 。
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:___________ 。
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为___________
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)
 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正
③图中B点的压强平衡常数Kp=
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】平衡,可逆反应的宿命,可逆反应永恒的话题。
(1)在一体积为10L的容器中,通入一定量的CO和H2O,在一定温度时发生反应,4s后达到平衡状态。CO+H2O(g)⇌CO2+H2;△H<0
①CO和H2O的浓度变化如下图所示,则在0~4s时正反应的平均反应速率为v(CO2)=_______ mol·L-1·min-1
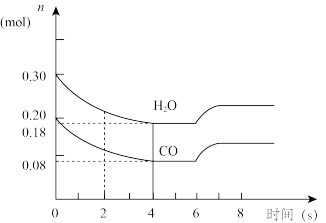
②图中6~7s之间反应向_______ (填左、右或不)移动,原因可能是_______ (填字母代号)
A.只充入水蒸气 B.只降低温度 C.只使用催化剂
D.只充入惰性气体 E.增大压强 F.只充入CO2
(2)在25℃下,将amol·L-1的醋酸与0.01mol·L-1的NaOH等体积混合,反应平衡时溶液中c(Na+)=c(CH3COO-),则溶液显_______ 性(填“酸”“碱”或“中”);用含a的代数式表示CH3COOH的电离常数Ka=_______ 。
(3)氨气的水溶液称为氨水,它的主要存在微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol/L
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O
则CH3COONH4溶液呈_______ 性(填“酸”、“碱”或“中”),NH4HCO3溶液呈_______ 性(填“酸”、“碱”或“中”),NH4HCO3溶液中浓度最大的离子是_______ (填离子的名称)
(4)已知常温下Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=1.0×10-38。现有0.1mol·L-1的CuCl2溶液中含有Fe3+,调节pH=3.0使Fe3+沉淀完全[即当c(Fe3+)<10-5mol·L-1时认为沉淀完全]此时Cu2+是否开始沉淀_______ (填“是”或“否”)。
(1)在一体积为10L的容器中,通入一定量的CO和H2O,在一定温度时发生反应,4s后达到平衡状态。CO+H2O(g)⇌CO2+H2;△H<0
①CO和H2O的浓度变化如下图所示,则在0~4s时正反应的平均反应速率为v(CO2)=

②图中6~7s之间反应向
A.只充入水蒸气 B.只降低温度 C.只使用催化剂
D.只充入惰性气体 E.增大压强 F.只充入CO2
(2)在25℃下,将amol·L-1的醋酸与0.01mol·L-1的NaOH等体积混合,反应平衡时溶液中c(Na+)=c(CH3COO-),则溶液显
(3)氨气的水溶液称为氨水,它的主要存在微粒是NH3·H2O。
已知:a.常温下,醋酸和NH3·H2O的电离平衡常数均为1.74×10-5mol/L
b.CH3COOH+NaHCO3=CH3COONa+CO2↑+H2O
则CH3COONH4溶液呈
(4)已知常温下Ksp[Cu(OH)2]=2.2×10-20,Ksp[Fe(OH)3]=1.0×10-38。现有0.1mol·L-1的CuCl2溶液中含有Fe3+,调节pH=3.0使Fe3+沉淀完全[即当c(Fe3+)<10-5mol·L-1时认为沉淀完全]此时Cu2+是否开始沉淀
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),
CO(g)+H2O(g),
其化学平衡常数K和温度T的关系如下表, 回答下列问题:
(1)该反应的化学平衡常数表达式为K =_________________________________ 。
(2)该反应为____________ 反应(选填吸热、放热)。
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为_____ K。
 CO(g)+H2O(g),
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如下表, 回答下列问题:
| T (K) | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K =
(2)该反应为
(3)某温度下,平衡浓度符合下式:c(CO2)·c(H2)=c(CO)·c(H2O),试判断此时的温度为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】根据下表所示化学反应与数据关系:
(1)反应①是__________  填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。
(2)写出反应③的平衡常数 的表达式
的表达式 __________ 。
(3)根据反应①与②可推导出 、
、 与
与 之间的关系,则
之间的关系,则
__________  用
用 、
、 表示
表示 。
。
(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有__________  填写字母序号
填写字母序号 。
。
A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO浓度
(5)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在 、
、 、
、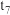 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断
时都改变了一种条件,试判断 时改变的是
时改变的是___
②若 时降压,
时降压,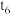 时增大反应物的浓度,请在图中画出
时增大反应物的浓度,请在图中画出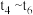 时逆反应速率与时间的关系曲线
时逆反应速率与时间的关系曲线___ 。
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
①Fe(s)+CO2(g) FeO(s)+CO(s) FeO(s)+CO(s) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g)  FeO(s)+H2(g) FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g)  CO2(g)+H2(g) CO2(g)+H2(g) | K3 | ? | ? |
(1)反应①是
 填“吸热”或“放热”
填“吸热”或“放热” 反应。
反应。(2)写出反应③的平衡常数
 的表达式
的表达式 (3)根据反应①与②可推导出
 、
、 与
与 之间的关系,则
之间的关系,则
 用
用 、
、 表示
表示 。
。(4)要使反应③在一定条件下建立的平衡向逆反应方向移动,可采取的措施有
 填写字母序号
填写字母序号 。
。A.缩小反应容器的容积
B.扩大反应容器的容积
C.升高温度
D.使用合适的催化剂
E.设法减小平衡体系中的CO浓度
(5)若反应③的逆反应速率与时间的关系如图所示:

①可见反应在
 、
、 、
、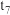 时都达到了平衡,而
时都达到了平衡,而 、
、 时都改变了一种条件,试判断
时都改变了一种条件,试判断 时改变的是
时改变的是②若
 时降压,
时降压,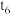 时增大反应物的浓度,请在图中画出
时增大反应物的浓度,请在图中画出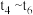 时逆反应速率与时间的关系曲线
时逆反应速率与时间的关系曲线
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐3】FeCl3是重要的化工原料,无水氯化铁在300℃以上升华,遇潮湿空气极易潮解
(1)制备无水氯化铁
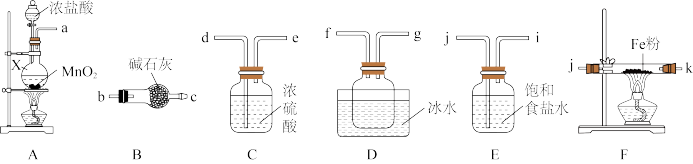
①仪器X的名称为_______ 。
②装置A中发生反应的化学方程式为_______
③装置的连接顺序为a→_______ →j,k→_______ (按气流方向,用小写字母表示)。
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i)Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii)Fe3+与SO2发生氧化还原反应,其离子方程式为①_______
④实验结论:反应(i)、(ii)的活化能大小关系是:E(i)_______ E(ii)(填“>”、“<”或“=”,下同),平衡常数大小关系是:K(i)_______ K(ii)。
⑤另取5mLlmol⋅L−1FeCl3溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是_______ 。
(1)制备无水氯化铁

①仪器X的名称为
②装置A中发生反应的化学方程式为
③装置的连接顺序为a→
(2)探究FeCl3与SO2的反应
已知反应体系中存在下列两种化学变化:
(i)Fe3+与SO2发生络合反应生成Fe(SO2)62+(红棕色);
(ii)Fe3+与SO2发生氧化还原反应,其离子方程式为①
| 步骤 | 现象 | 结论 |
| I.取5mL1mol⋅L−1FeCl3溶液于试管中,通入SO2至饱和 | 溶液很快由黄色变为红棕色 | |
| II.用激光笔照射步骤I中的红棕色溶液 | 溶液中无明显光路 | ②红棕色物质不是 |
| III.将步骤I中的溶液静置 | 1小时后,溶液逐渐变为浅绿色 | |
| IV.向步骤III中溶液加入2滴K3[Fe(CN)6]溶液 | ③ | 溶液中含有Fe2+ |
⑤另取5mLlmol⋅L−1FeCl3溶液,先滴加2滴浓盐酸,再通入SO2至饱和。几分钟后,溶液由黄色变为浅绿色,由此可知:促使氧化还原反应(ii)快速发生可采取的措施是
您最近一年使用:0次



