氮氧化物的转化和综合利用既有利于节约资源,又有利于保护环境。
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g) 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。

①图中A点时,SO2的转化率为___________ 。
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正___________ v(A)逆(填“>”“<”或 “=”)。
③图中B点的压强平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用___________ 法提高脱氮效率。
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为___________ 。
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:___________ 。
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为___________
(1)SO2经过净化后与空气混合进行催化氧化可制取硫酸,其中SO2发生催化氧化的反应为: 2SO2(g)+O2(g)
 2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
2SO3(g)。若在T1℃、0.1MPa条件下,往一密闭容器通入SO2和O2[其中n(SO2)∶n(O2)=2∶1],测得容器内总压强与反应时间的关系如图所示。
①图中A点时,SO2的转化率为
②在其他条件不变的情况下,测得T2℃时压强的变化曲线如图所示,则C点的正反应速率v(C)正与A点的逆反应速率v(A)逆的大小关系为v(C)正
③图中B点的压强平衡常数Kp=
(2)利用脱氮菌可净化低浓度NO废气。当废气在塔内停留时间均为90 s的情况下,测得不同条件下NO的脱氮率如图Ⅰ、Ⅱ所示。

①由图Ⅰ知,当废气中的NO含量增加时,宜选用
②图Ⅱ中,循环吸收液加入Fe2+、Mn2+提高了脱氮的效率,其可能原因为
(3)研究表明:NaClO2/H2O2酸性复合吸收剂可同时有效脱硫、脱硝。图Ⅲ所示为复合吸收剂组成一定时,温度对脱硫脱硝的影响。

①写出废气中的SO2与NaClO2反应的离子方程式:
②温度高于60 ℃后,NO去除率随温度升高而下降的原因为
更新时间:2022-03-01 22:21:50
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】化学反应速率在生产生活中有重要作用。
(1)氨的合成为氮肥的生产工业奠定了基础,其原理 。
。
①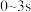 ,
, 的浓度增加了
的浓度增加了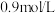 ,用
,用 表示其平均反应速率为
表示其平均反应速率为_______ 。
②下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是_______ (填字母)。
A.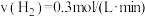 B.
B.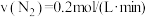
C.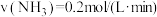 D.
D.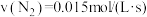
(2)研究反应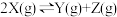 的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。
的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。

①对比实验Ⅰ、Ⅱ可得出:_______ ,化学反应速率加快。
②对比实验Ⅱ、Ⅳ可得出:_______ ,化学反应速率加快。
③实验Ⅲ与实验Ⅱ相比,实验Ⅲ平衡时间短的原因是_______ 。
(1)氨的合成为氮肥的生产工业奠定了基础,其原理
 。
。①
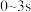 ,
, 的浓度增加了
的浓度增加了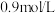 ,用
,用 表示其平均反应速率为
表示其平均反应速率为②下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是
A.
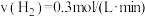 B.
B.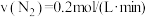
C.
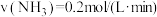 D.
D.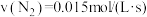
(2)研究反应
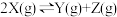 的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。
的速率影响因素,在不同条件下进行4组实验,Y、Z起始浓度为0,反应物X的浓度随反应时间的变化情况如图所示。
①对比实验Ⅰ、Ⅱ可得出:
②对比实验Ⅱ、Ⅳ可得出:
③实验Ⅲ与实验Ⅱ相比,实验Ⅲ平衡时间短的原因是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】硒元素不仅被科学家称为人体微量元素中的“抗癌之王”,还广泛应用于冶金、玻璃、陶瓷、电子、太阳能等众多领域。以铜阳极泥(主要成分为Ag2Se、Cu2Se和银、金、铂等)为原料制备纯硒的工艺流程如图所示:

回答下列问题:
(1)焙烧。此时硫酸最好选择________ (填“浓硫酸”“50%硫酸”或“20%硫酸”)。“焙烧”过程中Ag2Se参与反应的化学方程式为________________________ 。
(2)水吸收。水吸收反应过程中的还原产物是_____________________ 。
(3)过滤。“过滤”所得粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:
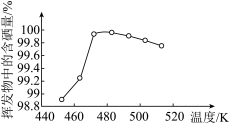
蒸馏操作中控制的最佳温度是________ (填序号)。
A.455℃ B.462℃ C.475℃ D.515℃
(4)水浸出步骤中,为加快浸出速率,可采取哪些措施?_________________ (写2条),“浸渣”中含有的金属单质是___________ 。
(5)浸出液。若“浸出液”中c(Ag+)=3.0×10-2 mol./L,则溶液中c( )最大为
)最大为__________ 。[已知:Ksp(Ag2SO4)=1.20×10-5,计算结果保留两位有效数字]

回答下列问题:
(1)焙烧。此时硫酸最好选择
(2)水吸收。水吸收反应过程中的还原产物是
(3)过滤。“过滤”所得粗硒可采用真空蒸馏的方法进行提纯,获得纯硒。真空蒸馏的挥发物中硒含量与温度的关系如图所示:

蒸馏操作中控制的最佳温度是
A.455℃ B.462℃ C.475℃ D.515℃
(4)水浸出步骤中,为加快浸出速率,可采取哪些措施?
(5)浸出液。若“浸出液”中c(Ag+)=3.0×10-2 mol./L,则溶液中c(
 )最大为
)最大为
您最近一年使用:0次
【推荐3】氮及其化合物是科学家们一直在探究的问题,它们在工农业生产和生命活动中起着重要的作用。回答下列问题:
(1)查阅资料: 标准摩尔生成焓是指在 25℃和101kPa时,由元素最稳定的单质生成 1mol纯化合物时的焓变,符号为 。已知以下物质的标准摩尔生成焓如下表所示。
。已知以下物质的标准摩尔生成焓如下表所示。
由此可得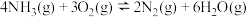
 =
=___________  。
。
(2)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、Ⅱ。
反应I:

反应Ⅱ: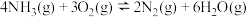

为分析某催化剂对该反应的选择性,将 1mol NH3和2mol O2充入1 L密闭容器中,在不同温度相同时间下,测得有关物质的量关系如图。
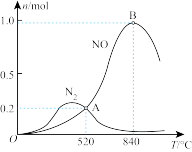
①该催化剂在低温时对反应___________ (填“Ⅰ”或“Ⅱ”)的选择性更好。
②520℃时,容器中为 c(NH3)=___________ mol/L,该温度下反应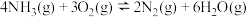 的平衡常数K=
的平衡常数K=___________ (不要求得出计算结果,只需列出有具体数字的计算式)。
③高于840℃时,NO 的产率降低的可能原因是___________ (填选项字母)。
A. NH3溶于水 B. 反应活化能增大
C.反应I的平衡常数变小 D. 催化剂活性降低
(3)NH3也是造成水体富营养化的重要原因之一,用 NaClO 溶液氧化可除去氨氮。其反应机理如图1所示(其中H2O 和 NaCl 略去)。
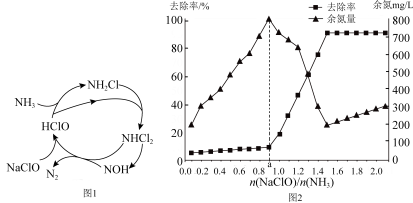
①NaClO 氧化 NH3的总反应的化学方程式为___________ 。
②改变 对溶液中NaClO去除氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图2 所示,则除氨氮过程中最佳的
对溶液中NaClO去除氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图2 所示,则除氨氮过程中最佳的 值约为
值约为___________ 。
③为了提高氨氮的去除率,在实际工艺过程中温度控制在 15℃~30℃时,其可能的原因是:___________ 。
(1)查阅资料: 标准摩尔生成焓是指在 25℃和101kPa时,由元素最稳定的单质生成 1mol纯化合物时的焓变,符号为
 。已知以下物质的标准摩尔生成焓如下表所示。
。已知以下物质的标准摩尔生成焓如下表所示。| 物质 |  |  |
 | -46 | -242 |
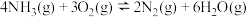
 =
= 。
。(2)氨气的催化氧化是工业制取硝酸的重要步骤,假设只会发生以下两个竞争反应Ⅰ、Ⅱ。
反应I:


反应Ⅱ:
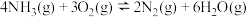

为分析某催化剂对该反应的选择性,将 1mol NH3和2mol O2充入1 L密闭容器中,在不同温度相同时间下,测得有关物质的量关系如图。

①该催化剂在低温时对反应
②520℃时,容器中为 c(NH3)=
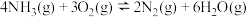 的平衡常数K=
的平衡常数K=③高于840℃时,NO 的产率降低的可能原因是
A. NH3溶于水 B. 反应活化能增大
C.反应I的平衡常数变小 D. 催化剂活性降低
(3)NH3也是造成水体富营养化的重要原因之一,用 NaClO 溶液氧化可除去氨氮。其反应机理如图1所示(其中H2O 和 NaCl 略去)。

①NaClO 氧化 NH3的总反应的化学方程式为
②改变
 对溶液中NaClO去除氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图2 所示,则除氨氮过程中最佳的
对溶液中NaClO去除氨氮效果与余氯(溶液中+1价氯元素的含量)的影响如图2 所示,则除氨氮过程中最佳的 值约为
值约为③为了提高氨氮的去除率,在实际工艺过程中温度控制在 15℃~30℃时,其可能的原因是:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐1】合成氨是人类科学技术上的一项重大突破,其反应原理为:N2(g)+3H2(g)⇌2NH3(g) △H=-92.4kJ⋅mol-1
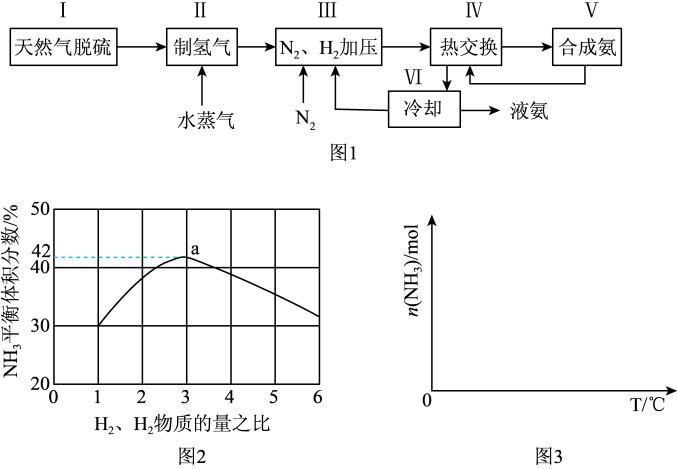
一种工业合成氨的简易流程图如图:
(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:___ 。
(2)步骤II中制氯气原理如下:
①CH4(g)+H2O(g)=CO2(g)+3H2(g) △H=+206.4kJ⋅mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.2kJ⋅mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是___ 。
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为___ 。
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:___ 。
(4)依据温度对合成氨反应的影响,在图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图___ 。
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是___ (填序号),简述本流程中提高合成氨原料总转化率的方法:___ 。
一种工业合成氨的简易流程图如图:

(1)天然气中的H2S杂质常用常用氨水吸收,产物为NH4HS。一定条件下向NH4HS溶液中通入空气,得到单质硫并使吸收液再生,写出再生反应的化学方程式:
(2)步骤II中制氯气原理如下:
①CH4(g)+H2O(g)=CO2(g)+3H2(g) △H=+206.4kJ⋅mol-1
②CO(g)+H2O(g)=CO2(g)+H2(g) △H=-41.2kJ⋅mol-1
对于反应①,一定可以提高平衡体系中H2百分含量,又能加快反应速率的是
a.升高温度 b.增大水蒸气浓度 c.加入催化剂 d.降低压强
利用反应②,将CO进一步转化,可提高H2产量。若1molCO和H2的混合气体(CO的体积分数为20%)与H2O反应,得到1.18molCO、CO2和H2的混合气体,则CO转化率为
(3)图2表示500℃、60.0MPa条件下,原料气投料比与平衡时NH3体积分数的关系。根据图中a点数据计算N2的平衡体积分数:
(4)依据温度对合成氨反应的影响,在图3坐标系中,画出一定条件下的密闭容器内,从通入原料气开始,随温度不断升高,NH3物质的量变化的曲线示意图
(5)上述流程图中,使合成氨放出的热量得到充分利用的主要步骤是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】 是一种重要的化工原料。工业上可以利用硫(
是一种重要的化工原料。工业上可以利用硫( )与
)与 为原料制备
为原料制备 ,
, 受热分解成气态
受热分解成气态 ,发生反应
,发生反应 ,回答下列问题:
,回答下列问题:
(1) 的电子式为
的电子式为_______ , 分子的空间构型为
分子的空间构型为_______ 。
(2)上述反应中属于极性分子的有_______ , 原子电子云有
原子电子云有_______ 种不同的形状。
(3)某温度下,若 完全分解成气态
完全分解成气态 。在恒温密闭容器中,
。在恒温密闭容器中, 与
与 物质的量比为
物质的量比为 时开始反应。
时开始反应。
①当 的体积分数为
的体积分数为 时,
时, 的转化率为
的转化率为_______ 。
②当以下数值不变时,能说明该反应达到平衡的是_______ (填序号)
a. 气体密度 b. 气体总压 c. 与
与 体积比 d.
体积比 d.  的体积分数
的体积分数
(4)一定条件下, 与
与 反应中
反应中 的平衡转化率、
的平衡转化率、 分解产生
分解产生 的体积分数随温度的变化曲线如图所示。据图分析,生成
的体积分数随温度的变化曲线如图所示。据图分析,生成 的反应为
的反应为_______ (填“放热”或“吸热”)反应。工业上通常采用在 的条件下进行此反应,不采用低于
的条件下进行此反应,不采用低于 原因是
原因是_______ 。

(5)用燃煤废气(含 、
、 、
、 、
、 、
、 、
、 等)使尾气中的
等)使尾气中的 转化为单后硫
转化为单后硫 ,可实现废物利用,保护环境,写出其中一个反应的化学方程式
,可实现废物利用,保护环境,写出其中一个反应的化学方程式_______ 。
 是一种重要的化工原料。工业上可以利用硫(
是一种重要的化工原料。工业上可以利用硫( )与
)与 为原料制备
为原料制备 ,
, 受热分解成气态
受热分解成气态 ,发生反应
,发生反应 ,回答下列问题:
,回答下列问题:(1)
 的电子式为
的电子式为 分子的空间构型为
分子的空间构型为(2)上述反应中属于极性分子的有
 原子电子云有
原子电子云有(3)某温度下,若
 完全分解成气态
完全分解成气态 。在恒温密闭容器中,
。在恒温密闭容器中, 与
与 物质的量比为
物质的量比为 时开始反应。
时开始反应。①当
 的体积分数为
的体积分数为 时,
时, 的转化率为
的转化率为②当以下数值不变时,能说明该反应达到平衡的是
a. 气体密度 b. 气体总压 c.
 与
与 体积比 d.
体积比 d.  的体积分数
的体积分数(4)一定条件下,
 与
与 反应中
反应中 的平衡转化率、
的平衡转化率、 分解产生
分解产生 的体积分数随温度的变化曲线如图所示。据图分析,生成
的体积分数随温度的变化曲线如图所示。据图分析,生成 的反应为
的反应为 的条件下进行此反应,不采用低于
的条件下进行此反应,不采用低于 原因是
原因是
(5)用燃煤废气(含
 、
、 、
、 、
、 、
、 、
、 等)使尾气中的
等)使尾气中的 转化为单后硫
转化为单后硫 ,可实现废物利用,保护环境,写出其中一个反应的化学方程式
,可实现废物利用,保护环境,写出其中一个反应的化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】
(1)已知:下列两个热化学方程式: Fe(s) + 1/2O2(g) =FeO(s) =-272.0KJ/mol,2Al(s) + 3/2O2(g) =Al2O3(s)
=-272.0KJ/mol,2Al(s) + 3/2O2(g) =Al2O3(s)  =-1675.7KJ/mol 则Al(s)的单质和FeO(s)反应的热化学方程式是
=-1675.7KJ/mol 则Al(s)的单质和FeO(s)反应的热化学方程式是____________________________ 。
(2)对于下列反应:2SO2 + O2 2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为
2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为_____________ 。如果开始时SO2浓度为4mol/L,2min后反应达平衡,若这段时间内v(O2)为0.5mol/(L· min),那么2min时SO2的浓度为_______________ 。
(3)如图表示在密闭容器中反应:2SO2+O2 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是________ ;bc过程中改变的条件可能是____________________ ;
(4)若增大压强时,将反应速度变化情况画在c—d处_______________ 。

(1)已知:下列两个热化学方程式: Fe(s) + 1/2O2(g) =FeO(s)
 =-272.0KJ/mol,2Al(s) + 3/2O2(g) =Al2O3(s)
=-272.0KJ/mol,2Al(s) + 3/2O2(g) =Al2O3(s)  =-1675.7KJ/mol 则Al(s)的单质和FeO(s)反应的热化学方程式是
=-1675.7KJ/mol 则Al(s)的单质和FeO(s)反应的热化学方程式是(2)对于下列反应:2SO2 + O2
 2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为
2SO3, 如果2min内SO2的浓度由6 mol/L下降为2 mol/L,那么,用O2浓度变化来表示的反应速率为(3)如图表示在密闭容器中反应:2SO2+O2
 2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是
2SO3+Q达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是(4)若增大压强时,将反应速度变化情况画在c—d处

您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】回答下列问题:
(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液 的关系如图所示,
的关系如图所示, 一般选择5左右,理由是
一般选择5左右,理由是_______ 。

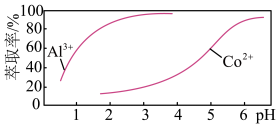
(2)萃取剂对 、
、 萃取率与
萃取率与 的关系如图所示。
的关系如图所示。
萃取分离钴、铝的实验操作:向萃取分液后的有机相中加稀硫酸调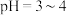 ,分液可得
,分液可得 溶液;
溶液;_______ ,可得 溶液。
溶液。
(3)已知萃取剂A、B中 对钴离子、锰离子萃取率的影响如图所示,为了除去
对钴离子、锰离子萃取率的影响如图所示,为了除去 ,应选择萃取剂
,应选择萃取剂_______ (填“A”或“B”)。

(1)“萃取分离”溶液中钴、锂的萃取率与平衡时溶液
 的关系如图所示,
的关系如图所示, 一般选择5左右,理由是
一般选择5左右,理由是
(2)萃取剂对
 、
、 萃取率与
萃取率与 的关系如图所示。
的关系如图所示。
萃取分离钴、铝的实验操作:向萃取分液后的有机相中加稀硫酸调
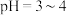 ,分液可得
,分液可得 溶液;
溶液; 溶液。
溶液。(3)已知萃取剂A、B中
 对钴离子、锰离子萃取率的影响如图所示,为了除去
对钴离子、锰离子萃取率的影响如图所示,为了除去 ,应选择萃取剂
,应选择萃取剂
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】氨在国防、工农业生产领域发挥着重要作用。
(1)工业以甲烷为原料生产氨气的过程如下:甲烷 氢气
氢气 氨气。
氨气。
①过程Ⅰ中,有关化学反应的能量变化如图所示

反应①为__________反应(填“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是__________。
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g) ⇌[Cu(NH3)2]CH2COO•CO(1),
①N元素在周期表中的位置为__________,NH3的电子式为__________。
②所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是__________(选填字母)。
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
(3)合成NH3的反应为放热反应,如果该反应平衡时,只改变一个条件,再次达到新平衡时,平衡常数K值变大。关于该反应的说法正确的是__________(填字母序号)。
(4)400℃,28MPa时,将1molN2和3mol H2混合充入体积可变的密闭容器中,加入催化剂,10分钟后反应达到平衡平衡时N2转化率为60%。
①下列图象能正确表示该过程中相关量的变化的是__________(填字母序号)。

②平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)恒温恒容时,若原料气投料比n(H2):n(N2)=1:1,平衡时、NH3的体积分数为30%。容器内的压强与起始压强之比为__________。
(1)工业以甲烷为原料生产氨气的过程如下:甲烷
 氢气
氢气 氨气。
氨气。①过程Ⅰ中,有关化学反应的能量变化如图所示

反应①为__________反应(填“吸热”或“放热”),CH4(g)与H2O(g)反应生成CO(g)和H2(g)的热化学方程式是__________。
(2)CO可降低过程Ⅱ所用催化剂的催化效率,常用乙酸二氨合铜(Ⅰ)溶液吸收,其反应原理为:[Cu(NH3)2CH3COO](aq)+CO(g)+NH3(g) ⇌[Cu(NH3)2]CH2COO•CO(1),
①N元素在周期表中的位置为__________,NH3的电子式为__________。
②所得溶液经处理的又可再生,恢复其吸收CO能力,再生的适宜条件是__________(选填字母)。
a.高温、高压 b.高温、低压 c.低温、低压 d.低温、高压
(3)合成NH3的反应为放热反应,如果该反应平衡时,只改变一个条件,再次达到新平衡时,平衡常数K值变大。关于该反应的说法正确的是__________(填字母序号)。
| A.一定向正反应方向移动 | B.在平衡移动时正反应速率先增大再减小 |
| C.一定向逆反应方向移动 | D.在平衡移动时逆反应速率先减小再增大 |
①下列图象能正确表示该过程中相关量的变化的是__________(填字母序号)。

②平衡常数Kp=__________(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(5)恒温恒容时,若原料气投料比n(H2):n(N2)=1:1,平衡时、NH3的体积分数为30%。容器内的压强与起始压强之比为__________。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】利用黄铁矿(主要成分为 )与软锰矿(主要成分为
)与软锰矿(主要成分为 )制备
)制备 并回收单质硫的部分工艺流程如下:
并回收单质硫的部分工艺流程如下:
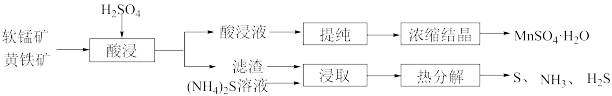
已知:酸浸液主要含有 、
、 、
、 等金属阳离子。
等金属阳离子。
(1)当温度为90℃时,酸浸过程中硫酸浓度c对Mn浸取率的影响如图1所示。

①基态 的价电子排布式为
的价电子排布式为___________ 。
②酸浸时反应生成 和S的离子方程式为
和S的离子方程式为___________ 。
③100min后,Mn浸取率随硫酸浓度增大而呈下降趋势,可能的原因是___________ 。
④酸浸液中还含有 等重金属阳离子,请结合数据说明能否用MnS除去
等重金属阳离子,请结合数据说明能否用MnS除去
___________ 。[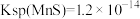 ,
,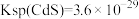 ]
]
(2) 溶液浸取滤渣时的反应为
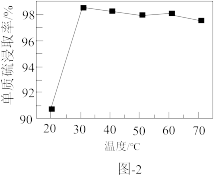
溶液浸取滤渣时的反应为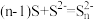 ,单质硫浸取率随温度变化曲线如图2所示。温度高于30℃,单质硫浸取率下降的可能原因是
,单质硫浸取率随温度变化曲线如图2所示。温度高于30℃,单质硫浸取率下降的可能原因是___________ 。
(3)制备得到的 产品中含有少量
产品中含有少量 和
和 杂质,进行以下实验测定产品中
杂质,进行以下实验测定产品中 含量:取10.00g产品溶于水,配成100mL溶液;取10.00mL所配溶液用
含量:取10.00g产品溶于水,配成100mL溶液;取10.00mL所配溶液用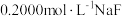 溶液滴定,消耗10.00mL;另取10.00mL所配溶液用
溶液滴定,消耗10.00mL;另取10.00mL所配溶液用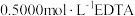 溶液滴定,消耗13.00mL。(已知:
溶液滴定,消耗13.00mL。(已知: 和
和 难溶于水;
难溶于水; 、
、 和
和 与EDTA按物质的量之比1∶1反应。),计算产品中
与EDTA按物质的量之比1∶1反应。),计算产品中 的质量分数
的质量分数___________ 。(写出计算过程)
 )与软锰矿(主要成分为
)与软锰矿(主要成分为 )制备
)制备 并回收单质硫的部分工艺流程如下:
并回收单质硫的部分工艺流程如下:
已知:酸浸液主要含有
 、
、 、
、 等金属阳离子。
等金属阳离子。(1)当温度为90℃时,酸浸过程中硫酸浓度c对Mn浸取率的影响如图1所示。

①基态
 的价电子排布式为
的价电子排布式为②酸浸时反应生成
 和S的离子方程式为
和S的离子方程式为③100min后,Mn浸取率随硫酸浓度增大而呈下降趋势,可能的原因是
④酸浸液中还含有
 等重金属阳离子,请结合数据说明能否用MnS除去
等重金属阳离子,请结合数据说明能否用MnS除去
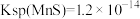 ,
,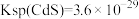 ]
](2)
 溶液浸取滤渣时的反应为
溶液浸取滤渣时的反应为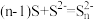 ,单质硫浸取率随温度变化曲线如图2所示。温度高于30℃,单质硫浸取率下降的可能原因是
,单质硫浸取率随温度变化曲线如图2所示。温度高于30℃,单质硫浸取率下降的可能原因是
(3)制备得到的
 产品中含有少量
产品中含有少量 和
和 杂质,进行以下实验测定产品中
杂质,进行以下实验测定产品中 含量:取10.00g产品溶于水,配成100mL溶液;取10.00mL所配溶液用
含量:取10.00g产品溶于水,配成100mL溶液;取10.00mL所配溶液用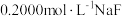 溶液滴定,消耗10.00mL;另取10.00mL所配溶液用
溶液滴定,消耗10.00mL;另取10.00mL所配溶液用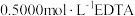 溶液滴定,消耗13.00mL。(已知:
溶液滴定,消耗13.00mL。(已知: 和
和 难溶于水;
难溶于水; 、
、 和
和 与EDTA按物质的量之比1∶1反应。),计算产品中
与EDTA按物质的量之比1∶1反应。),计算产品中 的质量分数
的质量分数
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】丙烯是重要的化工原料,可用于生产丙醇、卤代烃和塑料。
(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理如下:
I.
Ⅱ.
___________ 
Ⅲ. 。
。
(2)某研究小组向密闭容器中充入一定量的 和
和 ,分别在A、B两种不同催化剂作用下发生反应I,
,分别在A、B两种不同催化剂作用下发生反应I,一段时间后 测得 的产率与温度的关系如图所示。
的产率与温度的关系如图所示。___________ (填序号)。
A.使用催化剂B的最佳温度约为250℃
B.相同条件下,改变压强会影响 的产率
的产率
C.催化剂不仅能改变反应速率,还能改变平衡时的产率
D.两种催化剂均能降低反应的活化能,但不能改变 的数值
的数值
②在催化剂A作用下,温度低于200°C时, 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是___________ 。
(3)反应 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。___________ (填“丙烷”或“丙烯”),
___________ (填“大于”“小于”或“等于”) 。
。
②起始时充入一定量丙烷,在恒压 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为___________ (用分数表示),该反应的平衡常数 =
=___________  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(4)丙烷氧化脱氢法制备丙烯的反应为
 ,过程中还生成
,过程中还生成 、
、 等副产物。相同时间内,
等副产物。相同时间内, 的转化率和
的转化率和 的产率随温度变化的关系如图所示。
的产率随温度变化的关系如图所示。 的选择性为
的选择性为___________ %( 的选择性=
的选择性= ,计算结果精确到0.1)。
,计算结果精确到0.1)。
②基于上述研究结果,能提高 的选择性的措施是
的选择性的措施是___________ 。
(1)工业上用丙烯加成法制备1,2-二氯丙烷,主要副产物为3-氯丙烯。反应原理如下:
I.

Ⅱ.


Ⅲ.
 。
。(2)某研究小组向密闭容器中充入一定量的
 和
和 ,分别在A、B两种不同催化剂作用下发生反应I,
,分别在A、B两种不同催化剂作用下发生反应I, 的产率与温度的关系如图所示。
的产率与温度的关系如图所示。
A.使用催化剂B的最佳温度约为250℃
B.相同条件下,改变压强会影响
 的产率
的产率C.催化剂不仅能改变反应速率,还能改变平衡时的产率
D.两种催化剂均能降低反应的活化能,但不能改变
 的数值
的数值②在催化剂A作用下,温度低于200°C时,
 的产率随温度升高变化不大,主要原因是
的产率随温度升高变化不大,主要原因是(3)反应
 在不同温度下达到平衡,在总压强分别为
在不同温度下达到平衡,在总压强分别为 和
和 时,测得丙烷及丙烯的物质的量分数如图所示。
时,测得丙烷及丙烯的物质的量分数如图所示。

 。
。②起始时充入一定量丙烷,在恒压
 条件下发生反应,Q点对应温度下丙烷的转化率为
条件下发生反应,Q点对应温度下丙烷的转化率为 =
= (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。(4)丙烷氧化脱氢法制备丙烯的反应为

 ,过程中还生成
,过程中还生成 、
、 等副产物。相同时间内,
等副产物。相同时间内, 的转化率和
的转化率和 的产率随温度变化的关系如图所示。
的产率随温度变化的关系如图所示。
 的选择性为
的选择性为 的选择性=
的选择性= ,计算结果精确到0.1)。
,计算结果精确到0.1)。②基于上述研究结果,能提高
 的选择性的措施是
的选择性的措施是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】天然气的主要成分为CH4,还含有C2H6等烃类,是重要的燃料和化工原料。
(1)乙烷在一定条件可发生如下反应:C2H6(g) C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
①ΔH=___________ kJ•mol-1。
②提高该反应平衡转化率的方法有___________ 、___________ 。
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g) C2H4(g)+H2(g)。
C2H4(g)+H2(g)。
①可判断该反应达平衡的标志为___________ (填选项字母)。
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=___________ (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)高温下,甲烷生成乙烷的反应如下:2CH4 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=___________ r1。
(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:___________ 。
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为___________ 。
(1)乙烷在一定条件可发生如下反应:C2H6(g)
 C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:
C2H4(g)+H2(g)ΔH,相关物质的燃烧热数据如下表所示:| 物质 | C2H6(g) | C2H4(g) | H2(g) |
| 燃烧热ΔH/(kJ•mol-1) | —1560 | —1411 | —286 |
②提高该反应平衡转化率的方法有
(2)密闭容器中通入等物质的量的乙烷和氢气,在等温等压下(p)发生上述反应C2H6(g)
 C2H4(g)+H2(g)。
C2H4(g)+H2(g)。①可判断该反应达平衡的标志为
A.容器内混合气体的密度恒定
B.容器内混合气体的压强恒定
C.容器内乙烷和氢气的物质的量之比恒定
D.生成乙烯的速率和乙烷消耗的速率相等
②如果乙烷的平衡转化率为α,反应的平衡常数Kp=
(3)高温下,甲烷生成乙烷的反应如下:2CH4
 C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=
C2H6+H2,反应在初期阶段的速率方程为:r=kc(CH4),其中k为反应速率常数,设反应开始时的反应速率为r1,甲烷的转化率为α时的反应速率为r2,则r2=(4)CH4和CO2都是比较稳定的分子,科学家利用电化学装置实现两种分子的耦合转化,其原理如下图所示:
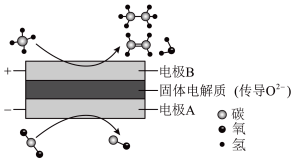
②若生成的乙烯和乙烷的体积比为2∶1,则消耗的CH4和CO2体积比为
您最近一年使用:0次
【推荐3】甲烷和水蒸气催化制氢主要存在如下两个反应:
①CH4(g)+ H2O (g) CO(g)+3H2(g) △H= +206kJ•mol-1
CO(g)+3H2(g) △H= +206kJ•mol-1
②CO(g)+ H2O (g) CO2 (g)+H2(g) △H=-41kJ•mol-1
CO2 (g)+H2(g) △H=-41kJ•mol-1
恒定压强为P0时,将n(CH4):n(H2O)=1
:3的混合气体投入反应器中,平衡时各组分的物质的量分数与温度的关系如图所示。回答下列问题:
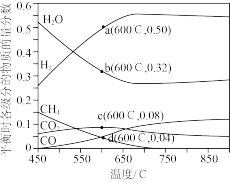
(1)写出CH4与CO2生成H2和CO的热化学方程式:___________ 。
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________ (填字母)。
(3)恒定压强为P0,投料比n(CH4): n(H2O)=1 :3时,从提高氢气产率角度考虑反应温度应控制在___________ ℃左右。
(4)600°C时,CH4的平衡转化率为___________ (保留2位有效数字),反应①的平衡常数的计算式为Kp=___________ (Kp是以分压表示的平衡常数,分压=总压×物质的量分数)。
①CH4(g)+ H2O (g)
 CO(g)+3H2(g) △H= +206kJ•mol-1
CO(g)+3H2(g) △H= +206kJ•mol-1②CO(g)+ H2O (g)
 CO2 (g)+H2(g) △H=-41kJ•mol-1
CO2 (g)+H2(g) △H=-41kJ•mol-1恒定压强为P0时,将n(CH4):n(H2O)=1
:3的混合气体投入反应器中,平衡时各组分的物质的量分数与温度的关系如图所示。回答下列问题:

(1)写出CH4与CO2生成H2和CO的热化学方程式:
(2)关于甲烷和水蒸气催化制氢反应,下列叙述正确的是___________ (填字母)。
| A.恒温、恒容条件下,加入惰性气体,压强增大,反应速率加快 |
| B.恒温、恒容条件下,加入水蒸气,活化分子百分数增大,反应速率加快 |
| C.升高温度,活化分子百分数增大,有效碰撞频率增大,反应速率加快 |
| D.加入合适的催化剂,同时降低反应温度,相同时间内的转化率可能不变 |
(4)600°C时,CH4的平衡转化率为
您最近一年使用:0次



