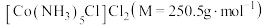 是一种易溶于热水,难溶于乙醇的紫红色晶体。
是一种易溶于热水,难溶于乙醇的紫红色晶体。(1)制备步骤:将适量氯化铵溶于浓氨水中,边搅拌边分批次加入
 研细的
研细的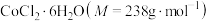 ,得到
,得到 沉淀。边搅拌边慢慢滴入足量
沉淀。边搅拌边慢慢滴入足量 溶液,得到
溶液,得到 溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到
溶液。慢慢注入适量浓盐酸,得到沉淀,水浴加热,冷却至室温,得到紫红色晶体,减压过滤,洗涤,烘干,得到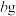 产品。
产品。(2)钴的测定:取
 样品于锥形瓶中,加入
样品于锥形瓶中,加入 溶液并加热使钴(Ⅲ)完全沉淀,后加入
溶液并加热使钴(Ⅲ)完全沉淀,后加入 和
和 将其还原为钴(Ⅱ),再加入
将其还原为钴(Ⅱ),再加入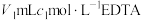 ,用
,用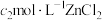 标准溶液滴定过量的
标准溶液滴定过量的 ,消耗
,消耗 溶液平均体积为
溶液平均体积为 与金属阳离子
与金属阳离子 反应)。
反应)。对于上述实验,下列说法错误的是
| A.本实验应在通风橱中进行 |
B.分批次加入研细的 ,目的是防止反应过快 ,目的是防止反应过快 |
C.温度过高不利于 的生成 的生成 |
D.还原性: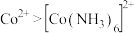 |
更新时间:2024-05-16 07:01:56
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】探究铁及其化合物的性质,下列方案设计、现象和结论不完全正确的是
实验方案 | 现象 | 结论 | |
A | 往 溶液中加入Zn片 溶液中加入Zn片 | 溶液浅绿色逐渐褪去 |  的氧化能力比 的氧化能力比 强 强 |
B | 往 溶液中滴加KSCN溶液,再加入少量 溶液中滴加KSCN溶液,再加入少量 固体 固体 | 溶液先变成血红色后无明显变化 |  对反应无影响 对反应无影响 |
C | 将食品脱氧剂样品中的还原铁粉溶于盐酸,滴加KSCN溶液 | 溶液呈浅绿色 | 食品脱氧剂样品中没有+3价铁 |
D | 向沸水中逐滴加5~6滴饱和 溶液,持续煮沸 溶液,持续煮沸 | 溶液先变成红褐色再析出沉淀 |  先水解得 先水解得 再聚集成 再聚集成 沉淀 沉淀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
【推荐2】ClO2因具有杀菌能力强,对人体、动物没有危害以及对环境不造成二次污染等特点,各受人们的青睐。图是一种制ClO2的微观示意图。下列有关说法正确的是

(其中: 表示钠原子,
表示钠原子, 表示氯原子,
表示氯原子, 表示氧原子)
表示氧原子)

(其中:
 表示钠原子,
表示钠原子, 表示氯原子,
表示氯原子, 表示氧原子)
表示氧原子)| A.该反应为置换反应 |
| B.该反应中,NaClO2作氧化剂 |
| C.该条件下,氧化性:Cl2>ClO2 |
| D.制取135 g ClO2,有4 mol Cl2失去电子 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】通常状况下, 是一种油状液体,可用于漂白,其分子空间构型与氨分子的相似。下列关于
是一种油状液体,可用于漂白,其分子空间构型与氨分子的相似。下列关于 的叙述正确的是
的叙述正确的是
 是一种油状液体,可用于漂白,其分子空间构型与氨分子的相似。下列关于
是一种油状液体,可用于漂白,其分子空间构型与氨分子的相似。下列关于 的叙述正确的是
的叙述正确的是A. 分子中所有原子共面 分子中所有原子共面 |
B. 能与 能与 以配位键生成 以配位键生成 |
C.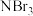 比 比 易挥发 易挥发 |
D. 水解生成 水解生成 和 和 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】向硫酸铜溶液中依次加入氨水和乙醇,关于此实验下列现象预测和分析错误的是
| 选项 | 现象预测 | 分析 |
| A | CuSO4溶液呈天蓝色 | 溶液中含有[Cu(H2O)]2+ |
| B | 加入少量氨水时产生白色沉淀 | 氨水呈碱性,可与Cu2+形成难溶的Cu(OH)2 |
| C | 继续加入过量氨水,沉淀溶解,得到深蓝色透明溶液 | NH3中N配位能力较强,与Cu2+形成[Cu(NH3)4]2+,促进Cu(OH)2溶解,平衡向溶解方向移动 |
| D | 继续加入乙醇并用玻璃棒摩擦试管壁,析出深蓝色晶体 | 乙醇极性较小,析出的深蓝色晶体是[Cu(NH3)4]SO4•H2O |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】能正确表示下列变化的离子方程式是
A.乙醇与KMnO4酸性溶液反应:5CH3CH2OH+4 + 12H+→5CH3COO-+5H++4Mn2++11H2O + 12H+→5CH3COO-+5H++4Mn2++11H2O |
B.0.1mol ·L-1 AgNO3溶液中加入过量浓氨水:Ag++3NH3·H2O=Ag(NH3)2OH+2H2O+ |
| C.少量Mg(OH)2溶于FeCl3 溶液:3Mg(OH)2(s)+2Fe3+(aq) =2Fe(OH)3(s)+3Mg2+(aq) |
| D.H2l8O 中投入Na2O2固体:2H218O+2Na2O2=4Na++4OH-+18O2↑ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】根据下列实验操作,观察到的现象和得出的结论均正确的是
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 将SO2气体通入Ba(NO3)2溶液 | 有白色沉淀生成 | SO2中混有SO3 |
| B | 向试管底部有少量铜的Cu(NO3)2溶液中加入稀硫酸 | 铜片不溶解 | 铜不能与稀硫酸反应 |
| C | 乙醇和浓硫酸170℃共热,产生的气体直接通入酸性KMnO4溶液 | 溶液紫红色褪去 | 生成气体可能是乙烯 |
| D | 将蘸有浓氨水的玻璃棒靠近试剂瓶瓶口 | 瓶口有白烟生成 | 该试剂瓶中盛有的一定是浓盐酸 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列实验操作规范且能达到实验目的的是
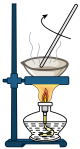 | 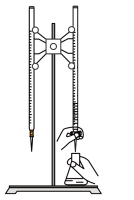 | 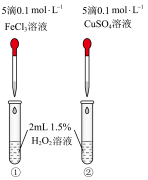 | 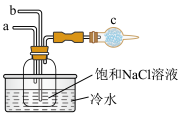 |
蒸干 溶液可制得无水 溶液可制得无水 固体 固体 | 用标准 溶液滴定雉形瓶中的盐酸 溶液滴定雉形瓶中的盐酸 | 反应速率①>②,可以验证 的催化效果比 的催化效果比 好 好 | 先从 通 通 ,然后从 ,然后从 通入 通入 ,可制得少量 ,可制得少量 固体 固体 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】利用石墨电极电解1mol/L氯化钠溶液,并收集阳极气体检验其成分。已知:O2能使酸性的淀粉KI溶液变蓝,不能使中性的淀粉KI溶液变蓝。
实验:①将气体通入中性的淀粉KI溶液中,溶液变蓝。②用足量NaOH溶液充分洗气,气体体积减少,将剩余气体通入中性的淀粉KI溶液中,溶液颜色不变,再向溶液中滴加2滴H2SO4溶液,溶液变蓝。③向酸性的淀粉KI溶液中通入空气,溶液颜色不变。
下列对实验现象的解释或推测不合理 的是
实验:①将气体通入中性的淀粉KI溶液中,溶液变蓝。②用足量NaOH溶液充分洗气,气体体积减少,将剩余气体通入中性的淀粉KI溶液中,溶液颜色不变,再向溶液中滴加2滴H2SO4溶液,溶液变蓝。③向酸性的淀粉KI溶液中通入空气,溶液颜色不变。
下列对实验现象的解释或推测
A.根据实验现象可以判断电解时阳极的电极反应式为:2Cl-—2e- Cl2↑ Cl2↑ |
| B.根据实验可以得出反应物的浓度和溶液的pH会影响物质的氧化性 |
| C.根据实验可以得出中性条件下,氧化性Cl2>O2 |
D.NaOH溶液洗气时发生反应的离子方程式为:2OH-+Cl2 Cl-+ClO-+H2O Cl-+ClO-+H2O |
您最近一年使用:0次



