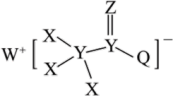常用作吸附剂和催化剂,将铝铵矾
常用作吸附剂和催化剂,将铝铵矾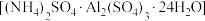 加热到723K,会生成
加热到723K,会生成 。下列说法错误的是
。下列说法错误的是A.第一电离能: | B.碱性: |
C.离子半径: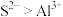 | D.电负性: |
更新时间:2024-05-24 16:47:57
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列关于元素周期表和元素周期律的说法正确的是
| A.从氟到碘,其氢化物的稳定性逐渐增强 |
| B.氧与硫为同主族元素,氧比硫的原子半径小,氧比硫的非金属性强 |
| C.第三周期从钠到氯,氧化物的水化物碱性逐渐减弱,酸性逐渐增强 |
| D.铝原子比钠原子失去电子数目多,还原性:Al>Na |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】某温度时,ⅥA元素单质A2、B、D与H2反应生成气态H2X的热化学方程式如下:
 A2(g)+H2(g)=H2A(g)
A2(g)+H2(g)=H2A(g) 
B(g)+H2(g)=H2B(g)
D(g)+H2(g) H2D(g)
H2D(g) 
下列说法正确的是
 A2(g)+H2(g)=H2A(g)
A2(g)+H2(g)=H2A(g) 
B(g)+H2(g)=H2B(g)

D(g)+H2(g)
 H2D(g)
H2D(g) 
下列说法正确的是
| A.稳定性:H2A<H2B<H2D |
| B.降温有利于D与H2反应生成H2D |
| C.A2(g)+2H2B(g)=2H2A(g)+2B(g) ΔH=-444kJ·mol-1 |
| D.与H2的化合反应由易到难的顺序为:D>B>A2 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】已知X、Y、Z为短周期主族元素,在周期表中的相应位置如图所示,下列说法不正确的是( )


| A.若X为金属元素,则其与氧元素形成的化合物中阴阳离子个数比可能是1∶2 |
| B.若Z、Y能形成气态氢化物,则稳定性一定是ZHn>YHn |
| C.若Y是金属元素,则其氢氧化物既能和强酸反应又能和强碱反应 |
| D.三种元素的原子半径:r(X)>r(Y)>r(Z) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列微粒半径的比较中,正确的是( )
| A.r(Na+)> r(Na) | B.r(Cl―)> r(Cl) |
| C.r(Ca2+)> r(Cl―) | D.r(Mg)> r(Na) |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】如图是部分短周期元素化合价与原子序数的关系图,下列说法不正确的是


A. 与 与 形成的两种化合物中阳、阴离子的个数比均为 形成的两种化合物中阳、阴离子的个数比均为 |
B. 、 、 、 、 、 、 、 、 五种元素的原子中半径最大的是 五种元素的原子中半径最大的是 |
C. 和 和 的最高价氧化物对应的水化物能相互反应 的最高价氧化物对应的水化物能相互反应 |
D.氧化物 可做消毒剂 可做消毒剂 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】下列五种短周期元素的某些性质如表所示(其中只有W、Y、Z为同周期元素)。
下列叙述错误的是
| 元素 | X | W | Y | Z | R |
| 原子半径(pm) | 37 | 64 | 66 | 70 | 154 |
| 主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
| A.第一电离能大小顺序为:W>Z>Y |
| B.X、Y、Z三种元素形成的化合物,其晶体一定是分子晶体 |
| C.电负性的大小顺序为:W>Y>Z |
| D.Y与R、Y与X均可形成含有非极性共价键的化合物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列说法正确的是
| A.电子层数越多,原子半径越大 |
| B.第一电离能越小,元素金属性越强 |
| C.极性共价键越多,分子极性越强 |
| D.电负性越大,元素非金属性越强 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】物质M(结构如下图)常作为锂离子电池、锂离子电容器等的非水电解液添加剂。X、Y、Z、W为原子序数依次增大的短周期主族元素,基态W原子中有3个未成对电子。

| A.电负性:W>Z | B.最简单氢化物的沸点:Y>X |
| C.最高价含氧酸的酸性:X>W | D.第一电离能:X>Y |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大。
下列说法正确的是
| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有一个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
A.TY2是一种常用的溶剂,是极性分子,分子中存在2个 键 键 |
| B.W的氢化物形成的水溶液是强酸,可以刻蚀玻璃 |
C.在 、101kPa下,已知 、101kPa下,已知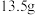 的X固体单质在 的X固体单质在 中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 中完全燃烧后恢复至原状态,放热419kJ,该反应的热化学方程式为 |
| D.Z的单质能在冷的Y的最高价氧化物水化物中钝化 |
您最近一年使用:0次