生物质气(主要成分为CO、 、
、 等)与
等)与 混合,在铜基催化剂
混合,在铜基催化剂 的作用下可合成甲醇。下列说法错误的是
的作用下可合成甲醇。下列说法错误的是
 、
、 等)与
等)与 混合,在铜基催化剂
混合,在铜基催化剂 的作用下可合成甲醇。下列说法错误的是
的作用下可合成甲醇。下列说法错误的是A. 是直线形分子 是直线形分子 |
B.第一电离能: |
C. 的空间结构为平面三角形 的空间结构为平面三角形 |
| D.基态Zn原子核外电子的空间运动状态有30种 |
更新时间:2024-05-24 10:54:46
|
相似题推荐
单选题
|
较易
(0.85)
【推荐1】下列说法正确的是
| A.1s22s22p63s13p1表示的是基态原子的电子排布 |
| B.电子仅在激发态跃迁到基态时才会产生原子光谱 |
| C.第三周期元素的原子半径从左到右逐渐减小,第一电离能依次增大 |
| D.日常生活中的许多可见光,如霓虹灯光、节日焰火等,都与原子核外电子发生跃迁释放能量有关 |
您最近一年使用:0次
【推荐2】下列事实与解释不对应 的是
| 选项 | 事实 | 解释 |
| A | 第一电离能: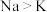 |  与K位于同一主族,原子半径: 与K位于同一主族,原子半径: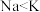 ,原子核对外层电子的吸引能力: ,原子核对外层电子的吸引能力: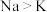 |
| B | 晶体中每个分子紧邻的分子数: 硫化氢晶体(12个)  冰(4个) 冰(4个) | 冰中水分子间主要以氢键结合,硫化氢晶体中硫化氢分子间主要以范德华力结合 |
| C | 分子的极性: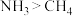 |  键的极性大于 键的极性大于 键的极性 键的极性 |
| D | 熔点: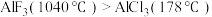 |  属于离子晶体, 属于离子晶体, 属于分子晶体 属于分子晶体 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
解题方法
【推荐1】价电子对互斥模型( 模型)可有效解释和预测分子的空间构型,下列解释均正确的是
模型)可有效解释和预测分子的空间构型,下列解释均正确的是
 模型)可有效解释和预测分子的空间构型,下列解释均正确的是
模型)可有效解释和预测分子的空间构型,下列解释均正确的是| 选项 | 分子 | 中心原子上价层电子对数 | 杂化轨道类型 | 分子的空间结构 |
| A |  | 4 |  | 平面正三角形 |
| B |  | 4 |  | 正四面体形 |
| C |  | 2 |  | 直线形 |
| D |  | 3 |  | 三角锥形 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较易
(0.85)
名校
【推荐2】下列叙述正确的是
| A.SO32-中硫原子的杂化方式为sp2 | B.C2H2分子中含有3个σ键和2个π键 |
| C.H2O分子中氧原子的杂化方式为sp2 | D.BF3分子空间构型呈三角锥形 |
您最近一年使用:0次

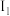 、
、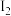 …表示,单位为
…表示,单位为 ),下列关于元素R的判断一定正确的是
),下列关于元素R的判断一定正确的是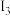
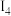

 键
键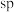 杂化轨道形成的化合物分子中一定含有
杂化轨道形成的化合物分子中一定含有 键
键

