海水中富含氯、溴、碘等卤族元素。
Ⅰ.碘是人体必须的微量元素之一,海洋植物如海带、海藻中含有丰富的碘元素。
在实验室中,从海藻里提取碘的流程如下:______ ,步骤ⅲ:______ 。
(2)步骤ⅱ中可使用 ,是因为
,是因为 的氧化性强于
的氧化性强于 ,请从原子结构角度说明理由
,请从原子结构角度说明理由____________ 。
(3)当使用 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。 时
时 转化率几乎为0,结合离子方程式从物质性质的角度解释原因:
转化率几乎为0,结合离子方程式从物质性质的角度解释原因:____________ 。
Ⅱ.不同卤素原子之间以共价键相结合形成的化合物成为卤素互化物,例如IBr、ICl等,它们的性质与卤素单质类似。
(4)①ICl中I元素的化合价是______ 。
②ICl与稀NaOH溶液可以发生非氧化还原反应,请写出该反应的离子方程式____________ 。
Ⅰ.碘是人体必须的微量元素之一,海洋植物如海带、海藻中含有丰富的碘元素。
在实验室中,从海藻里提取碘的流程如下:
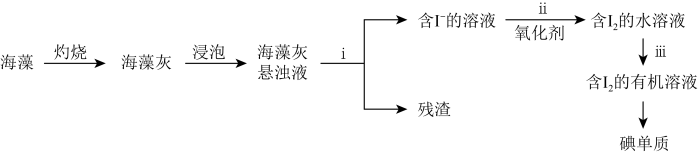
(2)步骤ⅱ中可使用
 ,是因为
,是因为 的氧化性强于
的氧化性强于 ,请从原子结构角度说明理由
,请从原子结构角度说明理由(3)当使用
 做氧化剂时,
做氧化剂时, 的转化率受外界因素的影响如下图所示。
的转化率受外界因素的影响如下图所示。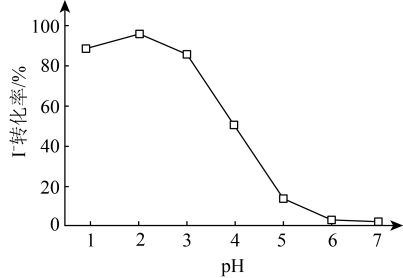
 时
时 转化率几乎为0,结合离子方程式从物质性质的角度解释原因:
转化率几乎为0,结合离子方程式从物质性质的角度解释原因:Ⅱ.不同卤素原子之间以共价键相结合形成的化合物成为卤素互化物,例如IBr、ICl等,它们的性质与卤素单质类似。
(4)①ICl中I元素的化合价是
②ICl与稀NaOH溶液可以发生非氧化还原反应,请写出该反应的离子方程式
更新时间:2024-05-26 16:32:52
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】1875年,法国化学家布瓦博德朗发现了门捷列夫预言的“类铝”,即新元素镓。金属镓有“电子工业脊梁”的美誉,镓及其化合物应用广泛。某学校化学兴趣小组在实验室利用如图装置模拟制备三氯化镓,并用该装置验证卤素单质氧化性的相对强弱。
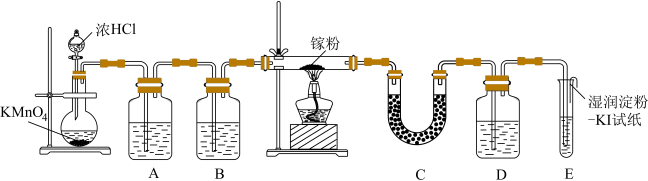
已知:①三氯化镓( )具有很强的吸湿性,在空气中吸收湿气而冒烟。
)具有很强的吸湿性,在空气中吸收湿气而冒烟。
②在氯气流中加热镓可制备 ,反应方程式
,反应方程式 。
。
(1)写出
 与浓盐酸反应制取氯气的离子方程式:
与浓盐酸反应制取氯气的离子方程式:(2)装置B中的试剂为
(3)D中装有NaBr溶液,反应开始后能通过D证明卤素单质氧化性相对强弱的现象是
(4)请推测写
 与NaOH反应的化学方程式
与NaOH反应的化学方程式
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐2】从硒鼓废料中回收硒的工艺流程如图。
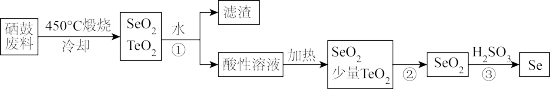
已知:
ⅰ.硒(34Se)、碲(52Te)与氧同主族;
ⅱ.硒鼓废料中主要成分为硒(含少量碲、碳、铜等)。煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2;
ⅲ.部分物质的物理性质。
(1)Te元素在元素周期表的位置是___________ ,稳定性:H2Se___________ H2S(填“>”、“<”或“=”)。
(2)过程①所得滤渣的主要成分是___________ 。
(3)根据表中数据,过程②最适宜的分离方法是___________ 。
(4)过程③发生反应的化学方程式是___________ 。
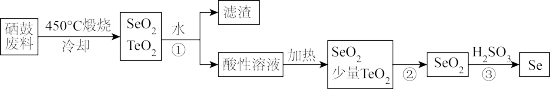
已知:
ⅰ.硒(34Se)、碲(52Te)与氧同主族;
ⅱ.硒鼓废料中主要成分为硒(含少量碲、碳、铜等)。煅烧过程中,回收料中的硒、碲被氧化成SeO2和TeO2;
ⅲ.部分物质的物理性质。
| 物质 | 熔点 | 沸点 | 溶解度 |
| SeO2 | 340℃(315℃升华) | 684℃ | 易溶于水 |
| TeO2 | 733℃(450℃升华) | 1260℃ | 微溶于水 |
(1)Te元素在元素周期表的位置是
(2)过程①所得滤渣的主要成分是
(3)根据表中数据,过程②最适宜的分离方法是
(4)过程③发生反应的化学方程式是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】W、X、Y、Z 是原子序数依次增大的四种短周期元素。W 的气态氢化物能使紫色石蕊溶液变蓝,W、X和Y三种元素的最高价氧化物的水化物两两之间可以发生反应,W、X、Y、Z 的最外层电子数之和为 16。回答下列问题:
(1)Z 单质的电子式是__ 。W的气态氢化物能使紫色石蕊溶液变蓝的原因__ (用化学方程式表示)。
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是____ (用离子符号表示)。
(3)不能能证明Z的非金属性比W强的实验事实是____ (填字母)。
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式_ 。
(5) Y和Z两元素形成化合物中化学键的类型为____ 。
(6)用电子式表示X2O的形成过程____ 。
(7)砷(As)与W位于同一主族,下列推断正确的是_____ (填序号)。
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
(1)Z 单质的电子式是
(2)X、Y、Z 三种元素的简单离子的离子半径由大到小的顺序是
(3)不能能证明Z的非金属性比W强的实验事实是
A.HZ的稳定性比WH3的稳定性性强
B.Z2与H2化合比W2与H2化合容易
C.HZ的水溶液酸性比WH3的水溶液酸性强
D.Z的最高价氧化物对应水化物的酸性比W强
(4)Z和氧元素、硫元素组成的SOZ2是一种液态化合物,沸点为77℃,遇水能剧烈水解,有白雾和带有刺激性气味的气体逸出,该气体可使滴有品红试液的滤纸褪色。请写出SOZ2和水反应的化学方程式
(5) Y和Z两元素形成化合物中化学键的类型为
(6)用电子式表示X2O的形成过程
(7)砷(As)与W位于同一主族,下列推断正确的是
①砷元素的最低负化合价为−3价
②砷的最高价氧化物对应的水化物属于酸
③热稳定性:AsH3>NH3
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐1】如图是部分元素周期表,序号代表某一元素请用化学用语回答下列问题。
(1)①~⑩中,最活泼的金属元素是______ (写元素符号);稀有气体元素名称是______ ;②的简单气态氢化物电子式是______ 。
(2)①、④、⑤原子半径由大到小的顺序是______ 。
(3)⑧、⑨的气态氢化物,更稳定的是______ (填化学式);结构式为______ 。
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是______ (填化学式);碱性最强的物质的电子式为______ ,它与⑥的最高价氧化物的水化物反应的离子方程式为______ 。
族 周期 | IA | 0 | ||||||
| 1 | IIA | IIIA | IVA | VA | VIA | VIIA | ||
| 2 | ① | ② | ③ | ④ | ||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ | ||
(2)①、④、⑤原子半径由大到小的顺序是
(3)⑧、⑨的气态氢化物,更稳定的是
(4)①~⑨的最高价氧化物的水化物中:酸性最强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐2】四种短周期元素在周期表中的相对位置如下所示,其中Z元素原子核外电子总数是其最外层电子数的3倍。
请回答下列问题:
(1)元素Z位于周期表中的第_________ 周期,_________ 族;
(2)这些元素的氢化物中,水溶液碱性最强的是_______________ (写化学式);
(3)XW2的电子式为_______________ ;
(4)Y的最高价氧化物的化学式为________________ ;
(5)W和Y形成的一种二元化合物具有色温效应,相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为_________________ 。
| X | Y | |
| Z | W |
请回答下列问题:
(1)元素Z位于周期表中的第
(2)这些元素的氢化物中,水溶液碱性最强的是
(3)XW2的电子式为
(4)Y的最高价氧化物的化学式为
(5)W和Y形成的一种二元化合物具有色温效应,相对分子质量在170~190之间,且W的质量分数约为70%。该化合物的化学式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐3】五种短周期元素A、B、C、D、E的原子序数依次增大,A和C同族,B和D同族,C的简单离子和B的简单离子具有相同的电子层结构;A和B、D、E均能形成共价型化合物;A和B形成的化合物在水中呈碱性,C和E形成的化合物中阴阳离子的个数比为1:1,根据判断出的元素及相应化学式回答问题:
(1)五种元素中,金属性最强的是_______ (填元素名称),非金属性最强的元素是_____ (填元素名称)。
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是_________ (用化学式表示)。
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为________ ,其中存在的化学键类型为_______________ 。
(4)E离子的结构示意图是__________ ,单质E与水反应的离子方程式为_________ 。
(1)五种元素中,金属性最强的是
(2)由元素A分别和元素B、D、E所形成的共价型化合物中,热稳定性最差的是
(3)元素A和E形成的化合物与元素A和B形成的化合物反应,产物的电子式为
(4)E离子的结构示意图是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐1】海洋是巨大的资源宝库,孕育着丰富的矿产。海水资源的综合利用对人类的生产生活有重要意义。回答下列问题:
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器________ (填“蒸发皿”“坩埚”或“烧杯”)内进行。
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有_________ (填一种即可);
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
(4)欲证明水溶液中含有I2,实验方法为________________ 。
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为___________ 。
(6)步骤②说明溴单质具有_________ 性,步骤③④的目的是______________ 。
(7)步骤③的还原剂若为 溶液,则其离子方程式为
溶液,则其离子方程式为____________ 。
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
| A.稀硝酸 | B.酸性 | C.浓硫酸 | D.稀硫酸、 |
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为
(6)步骤②说明溴单质具有
(7)步骤③的还原剂若为
 溶液,则其离子方程式为
溶液,则其离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐2】下表为元素周期表的一部分,请参照元素①—⑨在表中的位置,回答下列问题:
(1)第三周期中元素非金属性最强的元素的原子结构示意图为___________ 。
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)___________
(3)下列可以判断⑤和⑥金属性强弱的是___________ 。
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式___________ 。用⑥与赤铁矿冶炼金属铁的化学方程式___________ 。
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:
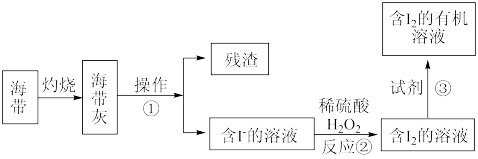
操作①的名称是___________ ;反应②的离子方程式是___________ 。
| 族 周期 | ⅠA | 0 | ||||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | ② | ③ | ④ | |||||
| 3 | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | |||
(2)②③⑨最高价氧化物对应水化物酸性强弱顺序为(填化学式)
(3)下列可以判断⑤和⑥金属性强弱的是
a.⑤单质的熔点比⑥单质低 b.⑤的化合价比⑥低
c.⑤单质与水反应比单质⑥剧烈 d.⑤最高价氧化物的水化物的碱性比⑥强
(4)工业制备⑥单质的化学方程式
(5)海水化学资源的开发利用具有重要的意义和作用,下图是海带中提取碘的示意图:

操作①的名称是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】海洋植物如海带、海藻中含有丰富的碘元素,主要以碘化物形式存在。有一化学课外小组用海带为原料制取少量碘单质,他们将海带灼烧成灰,用水浸泡一段时间(碘化物充分溶解在水中),得到海带灰悬浊液,然后按以下实验流程提取单质碘:(已知:2I-+Cl2=2Cl-+I2)
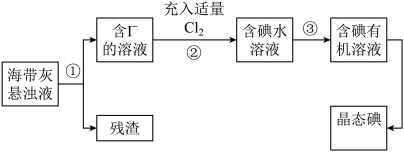
(1)指出提取碘的过程中有关的实验操作名称:①______ ,③ _____ 。
(2)过程②中充入适量Cl2的目的是(用方程式解释)_________________ ,把溶液中的I-转化成I2。
(3)操作③中所用的有机试剂可以是______________ (只填一种)。
(4)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
过程③正确操作步骤的顺序是:(填编号字母)_______ →________ →________ →A→H→________ →E→F。

(1)指出提取碘的过程中有关的实验操作名称:①
(2)过程②中充入适量Cl2的目的是(用方程式解释)
(3)操作③中所用的有机试剂可以是
(4)操作过程③可以分解为如下几步:
A.把盛有溶液的分液漏斗放在铁架台的铁圈中;
B.把50mL碘水和15mL有机溶剂加入分液漏斗中,并盖好玻璃塞;
C.检验分液漏斗活塞和上口的玻璃塞是否漏液;
D.倒转漏斗用力振荡,并不时旋开活塞放气,最后关闭活塞,把分液漏斗放正;
E.旋开活塞,用烧杯接收溶液;
F.从分液漏斗上口倒出上层液体;
G.将漏斗上口的玻璃塞打开或使塞上的凹槽与漏斗上口的小孔对准;
H.静置、分层。
过程③正确操作步骤的顺序是:(填编号字母)
您最近一年使用:0次



