A + B → X + Y + H2O(未配平,反应条件略去)是中学常见反应的化学方程式,请回答:
(1)若Y为黄绿色气体:
①当A、B的物质的量之比为1∶4且A为黑色固体时,该反应的离子方程式是_______ ;
②当A、B的物质的量之比为1∶6时,写出该反应的化学方程式,并用双线桥表示反应过程中的电子转移:_______ 。
③实验室处理尾气Y时常用NaOH而不用NaHSO3溶液,其原因是(用离子反应方程式表示)_______ 。
(2)若A为单质,B为无色油状黏稠液体,当 A、B的物质的量之比为1∶2时,则A可能为_______ ,检查其中刺激性气体产物X的方法是_______ 。
(3)常温下A在B的浓溶液中会“钝化”,且A可溶于X溶液中,若A为金属单质,A和B以物质的量之比1∶4反应。
①过量的A和100mL2mol/L的B溶液充分反应后将溶液稀释至500mL后溶液中阴离子的物质的量浓度为_______ 。
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量之比为1∶2时,则被还原的X是_______ mol。
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为_______ 。
(5)若A、B、X、Y均为化合物。X为极易溶于水的气体,则盐A是_______ 盐,X极易溶于水的原因是:_______ 。
(1)若Y为黄绿色气体:
①当A、B的物质的量之比为1∶4且A为黑色固体时,该反应的离子方程式是
②当A、B的物质的量之比为1∶6时,写出该反应的化学方程式,并用双线桥表示反应过程中的电子转移:
③实验室处理尾气Y时常用NaOH而不用NaHSO3溶液,其原因是(用离子反应方程式表示)
(2)若A为单质,B为无色油状黏稠液体,当 A、B的物质的量之比为1∶2时,则A可能为
(3)常温下A在B的浓溶液中会“钝化”,且A可溶于X溶液中,若A为金属单质,A和B以物质的量之比1∶4反应。
①过量的A和100mL2mol/L的B溶液充分反应后将溶液稀释至500mL后溶液中阴离子的物质的量浓度为
②含 a mol X的溶液溶解了一定量A后,若溶液中两种金属阳离子的物质的量之比为1∶2时,则被还原的X是
(4)若A、B、X、Y均为化合物。向A溶液中加入硝酸酸化的AgNO3溶液,产生白色沉淀;B的焰色为黄色。则A与B按物质的量之比1:4反应后,溶液中溶质的化学式为
(5)若A、B、X、Y均为化合物。X为极易溶于水的气体,则盐A是
更新时间:2016-12-08 22:58:42
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】“常见无机物”,主要是指的铝、铁、硫、氯四种元素的单质及化合物。完成下列填空:
(1)四种元素原子的半径大小Fe >______ >______ >______
(2)铝原子核外电子排布式_________________________ ,有_________ 种不同能量级的电子;铝热剂的成分是铝粉与氧化铁的混合物;写出铝热反应的化学方程式____________________
(3)工业上用氯气和__________ 制取漂粉精;吸收多余氯气的试剂是______________ 。
(4)硫磺粉末与铁粉混合加热,写出该反应的化学反应方程式并标出电子转移的方向和数目______________________________________________________ 。
(5)硫的非金属性________ 于氯(选填“强”、“弱”),用一个事实证明______________________ ,
再从原子结构的知识加以解释________________________________________________ 。
(1)四种元素原子的半径大小Fe >
(2)铝原子核外电子排布式
(3)工业上用氯气和
(4)硫磺粉末与铁粉混合加热,写出该反应的化学反应方程式并标出电子转移的方向和数目
(5)硫的非金属性
再从原子结构的知识加以解释
您最近一年使用:0次
【推荐2】利用氧化还原反应原理配平以下化学方程式,并:
FeSO4+ KNO3+ H2SO4 == K2SO4+ Fe2(SO4)3+ NO↑+ H2O
(1)标出电子转移的方向和数目____________________________ 。
(2)当电子转移了0.3mol时,有_________ g氧化剂参加反应。
FeSO4+ KNO3+ H2SO4 == K2SO4+ Fe2(SO4)3+ NO↑+ H2O
(1)标出电子转移的方向和数目
(2)当电子转移了0.3mol时,有
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】化学与人类生活密切相关。请按要求,回答下列问题:
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是_____ ,当反应中有1mol K2FeO4生成时,消耗Cl2在标况下的体积为_________ L,转移电子的数目为_____ 。
(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:_____________________________________________ 。
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:___________ 。
(4)工业上制漂白粉的化学方程式为_______________________________ ,新制氯水在阳光照射下产生无色气体,该反应的化学方程式是______ 。
(5)KA1(SO4)2•12H2O因其溶于水生成_____ (化学式)可以吸附杂质,从而达到净水作用。
(6)硅钢具有很高的_____ ,主要用作变压器的铁芯;硅酸钠水溶液的俗名为______ ,可作为木材________________ 的原料。
(7)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:________________________________ 。若向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,下列结果不可能出现的是________ 。
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
(1)K2FeO4是一种重要的净水剂,可用下列方法制得:2Fe(OH)3+3Cl2+10KOH
 2K2FeO4+6KCl+8H2O。在该反应中,还原剂是
2K2FeO4+6KCl+8H2O。在该反应中,还原剂是(2)宇航员常用过氧化钠作供氧剂,写出过氧化钠与二氧化碳反应的化学方程式并用双线桥法表示电子转移的方向和数目:
(3)厨房里小苏打常作面包和糕点的发泡剂,写出小苏打溶于水的电离方程式:
(4)工业上制漂白粉的化学方程式为
(5)KA1(SO4)2•12H2O因其溶于水生成
(6)硅钢具有很高的
(7)电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔来制造印刷电路板。写出FeCl3溶液与铜发生反应的离子方程式:
A.有铜无铁 B.有铁无铜 C.铁、铜都有 D.铁、铜都无
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】与硫同族的元素Te,最高价氧化物的水化物碲酸(H6TeO6)的酸性比H2SO4____ (选填“强”或“弱”),其氧化性比硫酸强。向碲酸中通入SO2气体,若反应中生成的TeO2与Te的物质的量之比为2:1,写出该反应的化学方程式______________ 。当6mol碲酸与一定量SO2恰好完全反应,所得溶液体积为20L,则所得溶液的pH为____________ 。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】乙二酸俗名草酸,下面是化学学习小组的同学对草酸晶体(H2C2O4·xH2O)进行的探究性学习的过程,请你参与并协助他们完成相关学习任务。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。
通过查阅资料和网络查询得知草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定,学习小组的同学设计了滴定的方法测定x值。
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4;
③用浓度为0.1000mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00mL。
(1)滴定时,将酸性KMnO4标准液装在如图中的_____ (填“甲”或“乙”)滴定管中。

(2)滴定时发生的离子反应是_______ 。
(3)本实验滴定达到终点的标志是________ 。
(4)通过上述数据,求得x=______ 。
讨论:
①若滴定终点时俯视滴定管刻度,则由此测得的x值会______ (填“偏大”“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会______ 。
该组同学的研究课题是:探究测定草酸晶体(H2C2O4·xH2O)中的x值。
通过查阅资料和网络查询得知草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定,学习小组的同学设计了滴定的方法测定x值。
①称取1.260g纯草酸晶体,将其制成100.00mL水溶液为待测液;
②取25.00mL待测液放入锥形瓶中,再加入适量的稀H2SO4;
③用浓度为0.1000mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00mL。
(1)滴定时,将酸性KMnO4标准液装在如图中的

(2)滴定时发生的离子反应是
(3)本实验滴定达到终点的标志是
(4)通过上述数据,求得x=
讨论:
①若滴定终点时俯视滴定管刻度,则由此测得的x值会
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】锑白(Sb2O3)在工业中有着广泛的作用。用辉锑矿(主要成分为Sb2S3,还含有少量 SiO2)制备锑白的工艺流程如下图:

已知:
①Sb3+与Fe2+的氧化性强弱相当。
②Sb2S3不溶于水;Sb2O3为白色粉末,不溶于水,溶于酸和强碱。
③水解时保持溶液的c(H+) =0.1~0.3mol/L。
(1) “浸出”是将辉锑矿溶于FeCl3溶液,为提高浸出速率可采取的措施是_________ (任写一种)。请写出其中发生的氧化还原反应离子方程式: _________ 。滤渣的成分为S单质和_________ 。
(2) 水解是利用SbCl3的水解反应制取Sb2O3(SbCl3的水解分为多步),其反应可以简单表示为:SbCl3 +3H2O Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):
Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):_________ 。
(3) 简述检验沉淀是否洗净的实验方法:_________ ,若未出现浑浊则证明沉淀已洗干净,反之则没有。

已知:
①Sb3+与Fe2+的氧化性强弱相当。
②Sb2S3不溶于水;Sb2O3为白色粉末,不溶于水,溶于酸和强碱。
③水解时保持溶液的c(H+) =0.1~0.3mol/L。
(1) “浸出”是将辉锑矿溶于FeCl3溶液,为提高浸出速率可采取的措施是
(2) 水解是利用SbCl3的水解反应制取Sb2O3(SbCl3的水解分为多步),其反应可以简单表示为:SbCl3 +3H2O
 Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):
Sb(OH)3 +3HCl,2Sb(OH)3 =Sb2O3 +3H2O。为了促进水解趋于完全,可采取的措施(填两点):(3) 简述检验沉淀是否洗净的实验方法:
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】下图中,A、C是工业上用途很广的两种重要化工原料,B为日常生活中常见的金属,H、G是正四面体结构的非极性分子,H是一种重要的能源,J是一种耐高温材料,K是由两种常见元素组成的化合物(图中部分反应物或生成物没有列出)。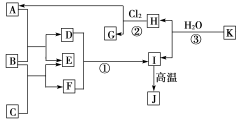
请按要求回答:
(1)写出B的化学式____________________ ,G的电子式________________ 。
(2)反应①的离子方程式为___________________________ 。
(3)反应②进行的条件是____________ 、____________________ 。
(4)反应③的化学方程式为_______________________ 。

请按要求回答:
(1)写出B的化学式
(2)反应①的离子方程式为
(3)反应②进行的条件是
(4)反应③的化学方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】某非金属单质A经下图所示的过程转化为含氧酸D,已知D为强酸,请回答下列问题:

(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式) D:____________ 。
②写出B→C反应的化学方程式:___________________________________________
(2)若A在常温下为气体,C是红棕色气体。
①A的化学式______________
②写出B→C反应的化学方程式:______________________________
③D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:______________________________ 。

(1)若A常温下为淡黄色固体,B是有刺激性气味的无色气体。
①若A、D的水溶液均能使湿润的蓝色石蕊试纸变红,且D为强酸,则A、D分别为(填写化学式) D:
②写出B→C反应的化学方程式:
(2)若A在常温下为气体,C是红棕色气体。
①A的化学式
②写出B→C反应的化学方程式:
③D的浓溶液在常温下可与铜反应并生成C气体,该反应的化学方程式为:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】利用“价类二维图”研究物质的性质是化学研究的重要手段。如图是氯元素的化合价与部分物质类别的对应关系。
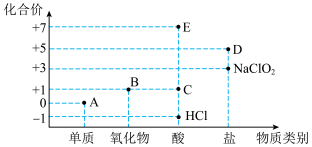
(1)物质E的化学式为___________
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是___________ (填化学式)
(3)A与水反应的离子方程式为___________
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为___________
(5)已知A与氢氧化钠溶液反应生成 和
和 的混合物,若
的混合物,若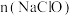 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为___________
(6)已知二氧化氯( )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为___________ ,电子数目之比为___________ 。
(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式___________ 。

(1)物质E的化学式为
(2)A、B、C、D(钾盐)四种物质中,属于电解质的是
(3)A与水反应的离子方程式为
(4)B为酸性氧化物,则B与氢氧化钠溶液反应的化学方程式为
(5)已知A与氢氧化钠溶液反应生成
 和
和 的混合物,若
的混合物,若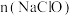 与
与 之比为2:3,则氧化剂与还原剂的物质的量之比为
之比为2:3,则氧化剂与还原剂的物质的量之比为(6)已知二氧化氯(
 )为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的
)为高效无毒的消毒剂,实际消毒效果比物质A要好。在室温及标准大气压的条件下,等物质的量的 和物质A比较,所含的原子总数之比为
和物质A比较,所含的原子总数之比为(7)氯碱工业指的是工业上用电解饱和食盐水的方法,制取氯气和烧碱等主要产品,在国民经济和国防建设中占有重要地位。请写出氯化钠溶液在通电条件下,发生反应的离子方程式
您最近一年使用:0次



