(1)甲醇可作为燃料电池的原料。以CH4和H2O为原料,通过下列反应来制备甲醇。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206.0kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g)ΔH=-129.0 kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为_______ 。
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+ 氧化成Co3+,然后以Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:
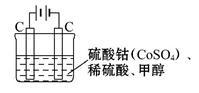
①写出阳极电极反应式_______ 。
②写出Co3+除去甲醇的离子方程式_______ 。
Ⅰ:CH4(g)+H2O(g)=CO(g)+3H2(g)ΔH=+206.0kJ·mol-1
Ⅱ:CO(g)+2H2(g)=CH3OH(g)ΔH=-129.0 kJ·mol-1
CH4(g)与H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为
(2)甲醇对水质会造成一定的污染,有一种电化学法可消除这种污染,其原理是:通电后,将Co2+ 氧化成Co3+,然后以Co3+ 作氧化剂把水中的甲醇氧化成CO2而净化。实验室用如图装置模拟上述过程:

①写出阳极电极反应式
②写出Co3+除去甲醇的离子方程式
更新时间:2016/12/08 23:03:20
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】 、
、 、
、 等含硫物质均是重要的化学原料。回答下列问题:
等含硫物质均是重要的化学原料。回答下列问题:
(1)已知
 ;
;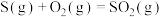
 ,
,
___________ (填“>”“=”或“<”) 。
。
(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。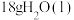 吸收热量为
吸收热量为___________ kJ;根据系统(II)可知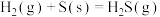 的
的
___________  。
。
(3)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:
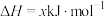 。
。
已知:碳的燃烧热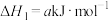

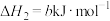


则x为___________ (用含a、b、c的代数式表示)。
(4)实验室用 与
与 在一定条件下进行下列反应:
在一定条件下进行下列反应:
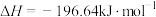 ,当放出314.624kJ热量时,
,当放出314.624kJ热量时, 的转化率为
的转化率为___________ 。
(5)如图是硫酸生产过程中钒催化剂参与反应的能量变化,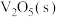 与
与 反应生成
反应生成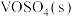 和
和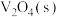 的热化学方程式为
的热化学方程式为___________ 。
 、
、 、
、 等含硫物质均是重要的化学原料。回答下列问题:
等含硫物质均是重要的化学原料。回答下列问题:(1)已知

 ;
;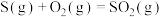
 ,
,
 。
。(2)下图是通过热化学循环在较低温度下由水或硫化氢分解制备氢气的反应系统原理。

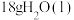 吸收热量为
吸收热量为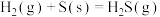 的
的
 。
。(3)黑火药是中国古代的四大发明之一,其爆炸的热化学方程式为:

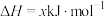 。
。已知:碳的燃烧热
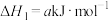

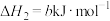


则x为
(4)实验室用
 与
与 在一定条件下进行下列反应:
在一定条件下进行下列反应:
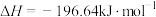 ,当放出314.624kJ热量时,
,当放出314.624kJ热量时, 的转化率为
的转化率为(5)如图是硫酸生产过程中钒催化剂参与反应的能量变化,
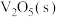 与
与 反应生成
反应生成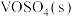 和
和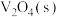 的热化学方程式为
的热化学方程式为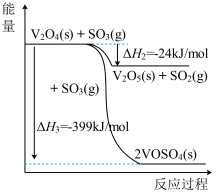
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)离子化合物 的化学式为
的化学式为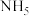 ,它所有原子的最外层都符合相应的稀有气体原子的最外层结构。有人认为
,它所有原子的最外层都符合相应的稀有气体原子的最外层结构。有人认为 是铵盐,这种想法是否正确
是铵盐,这种想法是否正确_______ 说明你的理由_______ 。
(2)火箭发射可以用肼( ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。
已知: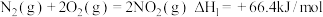
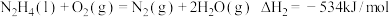
请写出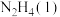 与
与 反应的热化学方程式
反应的热化学方程式_______
(3)相同条件下 酸性比
酸性比 强,请用一个化学方程式说明
强,请用一个化学方程式说明_______
(4)土壤中的铁循环( )可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮
)可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮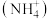 的原理:
的原理:_______ 。
(1)离子化合物
 的化学式为
的化学式为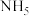 ,它所有原子的最外层都符合相应的稀有气体原子的最外层结构。有人认为
,它所有原子的最外层都符合相应的稀有气体原子的最外层结构。有人认为 是铵盐,这种想法是否正确
是铵盐,这种想法是否正确(2)火箭发射可以用肼(
 ,液态)作燃料,
,液态)作燃料, 作氧化剂,两者反应生成
作氧化剂,两者反应生成 和水蒸气。
和水蒸气。已知:
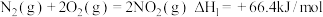
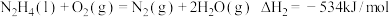
请写出
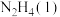 与
与 反应的热化学方程式
反应的热化学方程式(3)相同条件下
 酸性比
酸性比 强,请用一个化学方程式说明
强,请用一个化学方程式说明(4)土壤中的铁循环(
 )可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮
)可用于水体脱氮(脱氮是指将氮元素从水体中除去),用离子方程式分别说明利用土壤中的铁循环脱除水体中氨态氮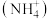 的原理:
的原理:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】甲醇作为燃料,在化石能源和可再生能源时期均有广泛的应用前景。
I. 甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为______ 。
(2)已知:25℃、101 kPa时,CH3OH(l) + 3/2 O2(g) ==== CO2 (g) + 2H2O(l) Δ H=-726.5 kJ/mol。相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是______ 。
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如右所示。
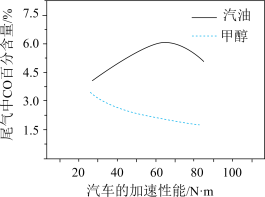
根据图信息分析,与汽油相比,甲醇作为燃料的优点是______ 。
II. 甲醇的合成
(4)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。
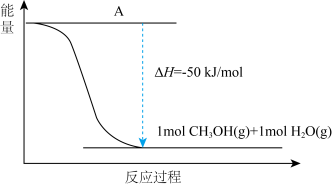
① 补全上图:图中A处应填入______ 。
② 该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH______ (填“变大”“变小”或“不变”)。
(5)已知: CO(g)+1/2 O2(g) ==== CO2(g) ΔH1=-283 kJ/mol
H2(g)+1/2 O2(g) ==== H2O(g) ΔH2=-242 kJ/mol
CH3OH(g) + 3/2 O2(g) ==== CO2 (g) + 2H2O(g) ΔH3=-676 kJ/mol
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g) + 2H2(g) ==== CH3OH(g) 。该反应的ΔH为_____ kJ/mol。
I. 甲醇可以替代汽油和柴油作为内燃机燃料。
(1)汽油的主要成分之一是辛烷[C8H18(l)]。已知:25℃、101 kPa时,1 mol C8H18(l)完全燃烧生成气态二氧化碳和液态水,放出5518 kJ热量。该反应的热化学方程式为
(2)已知:25℃、101 kPa时,CH3OH(l) + 3/2 O2(g) ==== CO2 (g) + 2H2O(l) Δ H=-726.5 kJ/mol。相同质量的甲醇和辛烷分别完全燃烧时,放出热量较多的是
(3)某研究者分别以甲醇和汽油做燃料,实验测得在发动机高负荷工作情况下,汽车尾气中CO的百分含量与汽车的加速性能的关系如右所示。

根据图信息分析,与汽油相比,甲醇作为燃料的优点是
II. 甲醇的合成
(4)以CO2(g)和H2(g)为原料合成甲醇,反应的能量变化如下图所示。

① 补全上图:图中A处应填入
② 该反应需要加入铜-锌基催化剂。加入催化剂后,该反应的ΔH
(5)已知: CO(g)+1/2 O2(g) ==== CO2(g) ΔH1=-283 kJ/mol
H2(g)+1/2 O2(g) ==== H2O(g) ΔH2=-242 kJ/mol
CH3OH(g) + 3/2 O2(g) ==== CO2 (g) + 2H2O(g) ΔH3=-676 kJ/mol
以CO(g)和H2(g)为原料合成甲醇的反应为CO(g) + 2H2(g) ==== CH3OH(g) 。该反应的ΔH为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】我国硒含量居世界首位,硒广泛用于冶金、陶瓷、电子、太阳能等领域。工业上常将含硒废料处理得到亚硒酸(H2SeO3)进而制备单质硒。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为___________ 。
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应___________ 。
(3)基态Se原子电子占据最高能级的电子云轮廓图为___________ 形。 号的空间结构为
号的空间结构为___________ 形。
(4)关于硒单质及其化合物说法正确的是___________ (填标号)。
a.硒单质在常温下呈固态 b. 既有氧化性又有还原性
既有氧化性又有还原性
c.键角: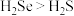 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下, 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:

 的
的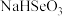 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为___________ ,计算反应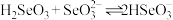 的平衡常数K=
的平衡常数K=___________ 。
(1)工业上在103℃的条件下,用甲酸(HCOOH)还原含亚硒酸(H2SeO3)的工业废液提取硒,此反应的化学方程式为
(2)研究表明,电解亚硒酸钠(Na2SeO3)、聚乙二醇和盐酸混合液也可直接制得单质硒,写出电解时阴极上发生的电极反应
(3)基态Se原子电子占据最高能级的电子云轮廓图为
 号的空间结构为
号的空间结构为(4)关于硒单质及其化合物说法正确的是
a.硒单质在常温下呈固态 b.
 既有氧化性又有还原性
既有氧化性又有还原性c.键角:
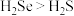 d.
d. 的最高价氧化物对应水化物的化学式为
的最高价氧化物对应水化物的化学式为
(5)室温下,
 电离平衡体系中含
电离平衡体系中含 微粒的物质的量分数与溶液
微粒的物质的量分数与溶液 的关系如图所示,回答下列问题:
的关系如图所示,回答下列问题:
 的
的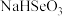 溶液中离子浓度由大到小的顺序为
溶液中离子浓度由大到小的顺序为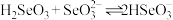 的平衡常数K=
的平衡常数K=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】某课外小组分别用如图所示装置对原电池和电解原理进行实验探究。
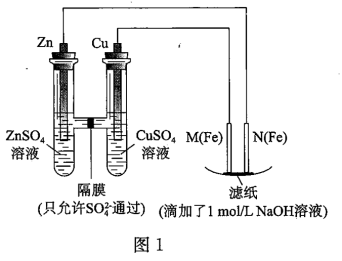
请回答:
Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是___________ (填字母序号)。
A.铝 B.石墨 C.银 D.铂
(2)M极发生反应的电极反应式为___________ ;
(3)实验过程中,SO
___________ (填“从左向右”、“从右向左”或“不”)移动;滤纸上能观察到的现象有___________ ,写出产生此现象的反应方程式:___________ ;
Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO )在溶液中呈紫红色。
)在溶液中呈紫红色。
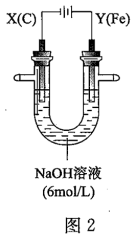
(4)电解过程中,X极区溶液的pH___________ (填“增大”、“减小”或“不变”);
(5)电解过程中,Y极发生的电极反应为___________ 和4OH--4e-=2H2O+O2↑,若在X极收集到672mL气体,在Y极收集到168mL气体(均已折算为标准状况时气体体积),则Y电极(铁电极)质量减少___________ g。
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为___________ 。

请回答:
Ⅰ.用如图1所示装置进行第一组实验。
(1)在保证电极反应不变的情况下,不能替代Cu做电极的是
A.铝 B.石墨 C.银 D.铂
(2)M极发生反应的电极反应式为
(3)实验过程中,SO

Ⅱ.用如图2所示装置进行第二组实验。实验过程中,两极均有气体产生,Y极区溶液逐渐变成紫红色;停止实验,铁电极明显变细,电解液仍然澄清。查阅资料发现,高铁酸根(FeO
 )在溶液中呈紫红色。
)在溶液中呈紫红色。
(4)电解过程中,X极区溶液的pH
(5)电解过程中,Y极发生的电极反应为
(6)在碱性锌电池中,用高铁酸钾作为正极材料,电池总反应为:2K2FeO4+3Zn=Fe2O3+ZnO+2K2ZnO2该电池正极的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲烷燃料电池采用铂为电极材料,两个电级上分别通入CH4和O2,电解质溶液为 KOH溶液。某研究小组将上述两个甲烷燃料电池串联后作为电源,进行电解饱和NaCl溶液的实验。如[图1所示]
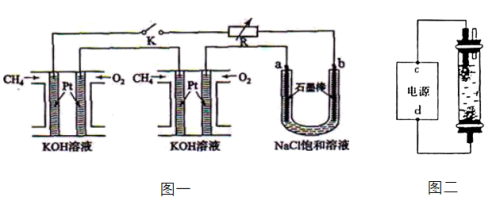
回答下列问题:
(1)甲烷燃料电池工作时,其电极反应分别为:正极___________ ,负极___________ 。
(2)闭合K开关后,a、b电极上均有气体产生,其中a电极上得到的是___________ ,电解 NaCl溶液的总反应方程式为___________
(3)若将饱和NaCl溶液改为CuCl2溶液,闭合K开关后,电解CuCl2溶液的化学方程式为:_____ 。若电解池中电极增重3.2 g,则通过电解池的电子的物质的量为______ mol。
(4)某学生制作一种家用环保型消毒液发生器,用石墨作电极电解饱和NaCl溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的“84”消毒液,设计了如图2的装置,电源d电极名称为___________ (填“正极”或“负极"),“84”消毒液的有效成分为___________ (填化学式)。

回答下列问题:
(1)甲烷燃料电池工作时,其电极反应分别为:正极
(2)闭合K开关后,a、b电极上均有气体产生,其中a电极上得到的是
(3)若将饱和NaCl溶液改为CuCl2溶液,闭合K开关后,电解CuCl2溶液的化学方程式为:
(4)某学生制作一种家用环保型消毒液发生器,用石墨作电极电解饱和NaCl溶液,通电时,为使Cl2被完全吸收,制得有较强杀菌能力的“84”消毒液,设计了如图2的装置,电源d电极名称为
您最近一年使用:0次



