准确称取12 g铝土矿样品(含Al2O3、Fe2O3、SiO2)放入盛有100 mL某浓度硫酸溶液的烧杯中,充分反应后过滤,向滤液中加入10 mol·L-1的NaOH溶液,产生的沉淀质量m与加入的NaOH溶液的体积V的关系如图所示:

请填空回答:
(1)H2SO4溶液的物质的量浓度为_________________ 。
(2)若a=4.6,用于沉淀Fe3+消耗NaOH的体积是____________ mL,铝土矿中各成分的质量分数:Al2O3为______________ , SiO2为______________ 。

请填空回答:
(1)H2SO4溶液的物质的量浓度为
(2)若a=4.6,用于沉淀Fe3+消耗NaOH的体积是
更新时间:2016-12-09 07:06:25
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】(1)0.3mol NH3分子中所含原子数与__________________ 个H2O分子中所含原子数相等。
(2)在9.5g某二价金属的氯化物中含有0.2mol Cl-,该金属元素的相对原子质量为_______ 。
(3)在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合物中C和O原子个数比是_______ 。
(2)在9.5g某二价金属的氯化物中含有0.2mol Cl-,该金属元素的相对原子质量为
(3)在标准状况下,由CO和CO2组成的混合气体为6.72L,质量为12g,此混合物中C和O原子个数比是
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐2】一定质量的镁、铝混合物投到2mol·L-1的盐酸中,待金属完全溶解后,再向溶液中逐滴加入2mol·L-1的氢氧化钠溶液,生成沉淀的质量与加入氢氧化钠溶液的体积关系如图所示。
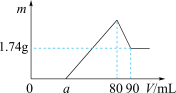
则:
(1)0~amL、a~80mL、80~90mL对应反应的离子方程式分别为:
①0~amL:___ ;
②amL~80mL:__ 、__ ;
③80mL~90ml:___ 。
(2)金属铝的质量为___ 。
(3)盐酸的体积是__ mL。
(4)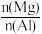 =
=__ 。
(5)a=__ 。

则:
(1)0~amL、a~80mL、80~90mL对应反应的离子方程式分别为:
①0~amL:
②amL~80mL:
③80mL~90ml:
(2)金属铝的质量为
(3)盐酸的体积是
(4)
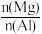 =
=(5)a=

您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】回答下列问题:
(1)在提炼核废料铀时,用过量的Ca2+处理3.52g氟化铀样品,生成2.34gCaF2沉淀,则氟化铀化学式为____ 。
(2)48gCH4和O2的混合气体在标准状况下的体积为44.8L,则混合气体中CH4与O2的物质的量之比为____ 。
(3)在标准状况下,142g氯气与氢气完全化合,将生成的气体配制成1L溶液,后取出10mL加蒸馏水制成200mL溶液,此稀释后溶液中溶质的物质的量浓度是____ mol•L-1。
(4)在一定条件下,某化合物X受热分解:2X A↑+2B↑+4C↑,测得反应后生成的混合气体的平均摩尔质量为22.86g•mol-1。则X的相对分子质量为
A↑+2B↑+4C↑,测得反应后生成的混合气体的平均摩尔质量为22.86g•mol-1。则X的相对分子质量为____ 。
(1)在提炼核废料铀时,用过量的Ca2+处理3.52g氟化铀样品,生成2.34gCaF2沉淀,则氟化铀化学式为
(2)48gCH4和O2的混合气体在标准状况下的体积为44.8L,则混合气体中CH4与O2的物质的量之比为
(3)在标准状况下,142g氯气与氢气完全化合,将生成的气体配制成1L溶液,后取出10mL加蒸馏水制成200mL溶液,此稀释后溶液中溶质的物质的量浓度是
(4)在一定条件下,某化合物X受热分解:2X
 A↑+2B↑+4C↑,测得反应后生成的混合气体的平均摩尔质量为22.86g•mol-1。则X的相对分子质量为
A↑+2B↑+4C↑,测得反应后生成的混合气体的平均摩尔质量为22.86g•mol-1。则X的相对分子质量为
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】
(1)将117 g NaCl溶于水配制成1 L溶液,该溶液中NaCl的物质的量浓度为___________ 。
(2)在标准状况下,将V L A气体(摩尔质量为M)溶于0.1 L水中,所得溶液的密度为ρ,则此溶液的物质的量浓度为_____________ 。
(3)某硫酸溶液的物质的量浓度为c1,密度为ρ1;另一种硫酸溶液的物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为______________ 。
(1)将117 g NaCl溶于水配制成1 L溶液,该溶液中NaCl的物质的量浓度为
(2)在标准状况下,将V L A气体(摩尔质量为M)溶于0.1 L水中,所得溶液的密度为ρ,则此溶液的物质的量浓度为
(3)某硫酸溶液的物质的量浓度为c1,密度为ρ1;另一种硫酸溶液的物质的量浓度为c2,密度为ρ2,将它们等体积混合后,所得溶液的密度为ρ3,则混合后硫酸的物质的量浓度为
A.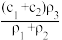 | B.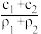 | C.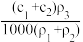 | D. |
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
【推荐3】将25℃ 101KPa条件下的氯化氢(HCl)气体49.6L,通入492mL水中,(已知水的密度为:1.00g/mL),得到密度为1.13g/mL的盐酸(即氯化氢的水溶液)。注:25℃101KPa条件下气体摩尔体积为24.8L/mol。
(1)此盐酸的质量分数为_________ (计算结果至0.1%)
(2)此盐酸的物质的量浓度为_____________ (计算结果保留一位小数)
(3)0.100 mol/L的稀盐酸500mL中含有的Cl-的数目为_____ (代入NA的近似值计算,结果保留三位有效数字)。
(1)此盐酸的质量分数为
(2)此盐酸的物质的量浓度为
(3)0.100 mol/L的稀盐酸500mL中含有的Cl-的数目为
您最近半年使用:0次
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】铝、氧化铝的性质与其他常见金属及氧化物相比,有一定的特殊性。
(1)可用NaOH溶液除去铁粉中的铝粉,反应原理是(用离子方程式表示)___________ ,将2.7gAl分别置于足量的NaOH溶液、稀硫酸中,生成H2的体积之比(同温同压)为___________ 。
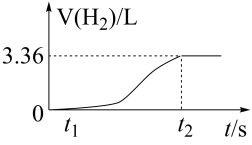
(2)证明Al2O3是两性氧化物的常用试剂是___________ (填名称),将ag废铝片置于100mL盐酸中,测得反应过程中生成氢气体积(标准状况)与时间的关系如图所示:0~t1时间段无气体生成的原因是___________ ,若反应后所得溶液中n(Al3+)=0.102mol且盐酸恰好完全反应,则原溶液中c(HCl)=___________ 。
(1)可用NaOH溶液除去铁粉中的铝粉,反应原理是(用离子方程式表示)
(2)证明Al2O3是两性氧化物的常用试剂是

您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐1】某天然碱可以看作是CO2和NaOH反应后的产物组成的一种物质。为了测定该物质的成分,进行如下实验:⑴称取3.32g天然碱样品,加入30mL过量稀盐酸,产生672mL CO2气体(标准状况);⑵另称取3.32g天然碱样品,在300℃下加热至分解完全,产生CO2 112mL(标准状况)和0.45g水。试通过计算,确定天然碱的化学式。
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐2】取表面部分氧化的镁条8.00g溶于250mL4.00mol·L-1的稀盐酸中,向所得溶液中滴加未知浓度的NaOH溶液,产生沉淀的质量与NaOH溶液的体积关系如图所示:
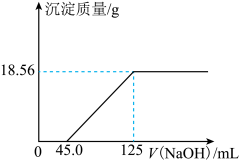
请计算:
(1)NaOH溶液的物质的量浓度___ mol·L-1。
(2)样品中镁元素的质量___ g。

请计算:
(1)NaOH溶液的物质的量浓度
(2)样品中镁元素的质量
您最近半年使用:0次
计算题
|
适中
(0.65)
【推荐3】某学习小组为探究一包铝热剂(铝与铁的氧化物)的组成,先取一部分铝热剂在高温下使之充分反应,将得到的固体经某种试剂只溶去其中的氧化物,再经过洗涤、干燥得到试样X(金属单质的损失忽略不计),试样X是铁和铝的混合物,然后将一定量的试样X分别投入浓度相同、体积均为100mL的稀盐酸中。
试回答下列问题:
(1)铝热剂所发生的反应称为铝热反应,铝热反应体现出铝的化学性质是______ 。指出铝热反应在工业生产中的一个用途:_____ 。
(2)盐酸的物质的量浓度为___ mol·L-1。
(3)根据表中第___ 组数据可以计算出试样X中Al、Fe的物质的量之比为__ 。
| ① | ② | ③ | |
| V(盐酸)/mL | 100 | 100 | 100 |
| m(X)/g | 2.22 | 4.44 | 6.66 |
| V(H2)/L(标准状况) | 1.344 | 2.24 | 2.24 |
试回答下列问题:
(1)铝热剂所发生的反应称为铝热反应,铝热反应体现出铝的化学性质是
(2)盐酸的物质的量浓度为
(3)根据表中第
您最近半年使用:0次

 溶液制得
溶液制得 ,反应方程式为:
,反应方程式为: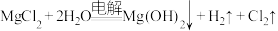 。现将
。现将 溶质质量分数为
溶质质量分数为 的
的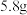 和若干滤液。试计算:
和若干滤液。试计算: 和
和 的质量比为
的质量比为 )
) 。应在滤液中加入一定量水和
。应在滤液中加入一定量水和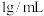 )
)

