甲醇是主要的化学工业基础原料和清洁液体燃料。工业上可以用CO或CO2来生产燃料甲醇。已知甲醇制备的有关化学反应以及在不同温度下的化学反应平衡常数如下表所示:

(1)反应②的反应热△H2_______ 0(填“>”、“<”或“=”);
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示。则平衡状态由A变到B时,平衡常数K(A)______ K(B)(填“>”、“<”或“=”);
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=___________ (用K1、K2表示)。500℃时测得反应③在某时刻H2(g)、CO2(g) 、CH3OH(g)、H2O(g)的浓度(mol/L)分别为0.8、0.1、0.3、0.15,则此时v(正)______ v(逆) (填“>”、“<”或“=”);
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是___________ ;当曲线Ⅰ变为曲线Ⅲ时,改变的条件是______________________________________ ;
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中乙酸的电离常数为_________________________ 。
| 化学反应及平衡常数 | 温度/℃ | ||
| 500 | 800 | ||
①2H2(g)+CO(g)  CH3OH(g) △H1 CH3OH(g) △H1 | K1 | 2.5 | 0.15 |
②H2(g)+CO2(g)  CO(g) +H2O(g) △H2 CO(g) +H2O(g) △H2 | K2 | 1.0 | 2.50 |
③3H2(g)+CO2(g)  CH3OH(g)+H2O(g) △H3 CH3OH(g)+H2O(g) △H3 | K3 | ||

(1)反应②的反应热△H2
(2)某温度下反应①中H2的平衡转化率(a)与体系总压强(P)的关系如图1所示。则平衡状态由A变到B时,平衡常数K(A)
(3)根据反应①与②可推导出K1、K2与K3之间的关系,则K3=
(4)在3L容积可变的密闭容器中发生反应②,已知c(CO)与反应时间t变化曲线Ⅰ如图2所示,若在t0时刻分别改变一个条件,曲线Ⅰ变为曲线Ⅱ和曲线Ⅲ。当曲线Ⅰ变为曲线Ⅱ时,改变的条件是
(5)一定条件下甲醇与一氧化碳反应可以合成乙酸。通常状况下,将amol/L的乙酸与bmol/LBa(OH)2溶液等体积混合,反应平衡时,2c(Ba2+)=c(CH3COO-),用含a和b的代数式表示该混合溶液中乙酸的电离常数为
更新时间:2016-12-09 07:10:21
|
相似题推荐
【推荐1】习总书记在十九大报告中明确指出:“宁要绿水青山,不要金山银山,而且绿水青山就是金山银山。”保护环境是我们的迫切需要。请回答下列问题:
(1) 会带来温室效应。目前,工业上采用氢气还原
会带来温室效应。目前,工业上采用氢气还原 制备乙醇的方法已经实现:
制备乙醇的方法已经实现: 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入
 和
和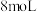
 ,在一定温度下反应,测得混合气体中
,在一定温度下反应,测得混合气体中 与时间的关系如图所示。
与时间的关系如图所示。

① 内,
内,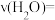
______  ;
;
②反应达到平衡时,
______ mol;
③在该温度下,该反应的化学平衡常数K______ (保留两位小数)。
(2)在恒容密闭容器中发生反应: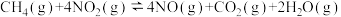
①下列说法能作为判断该反应达到化学平衡状态标志的是______ ;
A.容器内混合气体的密度保持不变
B.v正(NO2)=4v逆(CO2)
C.容器内压强保持不变
D.单位时间内,消耗nmol NO2的同时生成nmol NO
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为______ 反应(填“放热”或“吸热”)。
(3)在恒容密闭容器中,由CO可合成甲醇: ,回答问题:
,回答问题:
①该反应的化学平衡常数的表达式为______ ;
②若升高温度,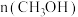 减少,则该反应为
减少,则该反应为______ 反应(填“放热”或“吸热”),若将体系温度升高,达到平衡时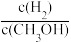
______ (填“增大”、“减小”或“不变”) 。
(1)
 会带来温室效应。目前,工业上采用氢气还原
会带来温室效应。目前,工业上采用氢气还原 制备乙醇的方法已经实现:
制备乙醇的方法已经实现: 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入
 和
和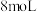
 ,在一定温度下反应,测得混合气体中
,在一定温度下反应,测得混合气体中 与时间的关系如图所示。
与时间的关系如图所示。
①
 内,
内,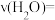
 ;
;②反应达到平衡时,

③在该温度下,该反应的化学平衡常数K
(2)在恒容密闭容器中发生反应:
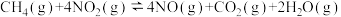
①下列说法能作为判断该反应达到化学平衡状态标志的是
A.容器内混合气体的密度保持不变
B.v正(NO2)=4v逆(CO2)
C.容器内压强保持不变
D.单位时间内,消耗nmol NO2的同时生成nmol NO
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为
(3)在恒容密闭容器中,由CO可合成甲醇:
 ,回答问题:
,回答问题:①该反应的化学平衡常数的表达式为
②若升高温度,
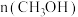 减少,则该反应为
减少,则该反应为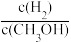
您最近一年使用:0次
填空题
|
适中
(0.64)
【推荐2】(1)在一定条件,可逆反应:mA+nB pC达到平衡状态。
pC达到平衡状态。
①若A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡向______ (填“正”或“逆”)反应方向移动。
②若A、B、C均为气体,且m+n<p,加热后,可使混合气体平均摩尔质量增加,则正反应是______ (填“吸热”或“放热”)反应。
③若在反应过程中,C的物质的量n(C)随时间的变化关系如右图所示(从t1时间开始对反应体系升高温度)。则a、b两点的正反应速率:v(a)______ v(b)(填“>”、“<”或“=”);

(2)Na2CO3溶液呈碱性,其原因是(用离子方程式表示)___________________ ;由同浓度的Na2CO3和NaHCO3组成的混合溶液中离子浓度由大到小的顺序为____________________ ;
(3)某温度下,纯水的c(H+)=3×10-7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH-)的比值为_________________ ;
(4)下列事实一定能说明HF是弱酸的是__________ ;
①常温下NaF溶液的pH大于7 ②常温下0.1mol/L的HF溶液pH=2.3
③HF能与Na2CO3溶液反应,产生CO2气体 ④1mol/L的HF水溶液能使紫色石蕊试液变红
 pC达到平衡状态。
pC达到平衡状态。①若A、C是气体,而且m+n=p,增大压强可使平衡发生移动,则平衡向
②若A、B、C均为气体,且m+n<p,加热后,可使混合气体平均摩尔质量增加,则正反应是
③若在反应过程中,C的物质的量n(C)随时间的变化关系如右图所示(从t1时间开始对反应体系升高温度)。则a、b两点的正反应速率:v(a)

(2)Na2CO3溶液呈碱性,其原因是(用离子方程式表示)
(3)某温度下,纯水的c(H+)=3×10-7mol/L,Na2S和NaOH两溶液的pH均为12,则两溶液中由水电离出的c(OH-)的比值为
(4)下列事实一定能说明HF是弱酸的是
①常温下NaF溶液的pH大于7 ②常温下0.1mol/L的HF溶液pH=2.3
③HF能与Na2CO3溶液反应,产生CO2气体 ④1mol/L的HF水溶液能使紫色石蕊试液变红
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】对于可逆反应CO+H2O(g) CO2+H2,回答下列问题:
CO2+H2,回答下列问题:
(1)830K时,若起始时c(CO)=2mol·L-1,c(H2O)=3 mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为________ ;平衡常数K的值为________ 。
(2)830 K,若只将起始时c(H2O)改为6 mol·L-1,则水蒸气的转化率为____ 。
(3)若830 K时,起始浓度c(CO)=a mol·L-1,c(H2O)=b mol·L-1,H2的平衡浓度c(H2)=c mol·L-1,则:
①a、b、c之间的关系式是________ ;
②当a=b时,a=________ c。
 CO2+H2,回答下列问题:
CO2+H2,回答下列问题:(1)830K时,若起始时c(CO)=2mol·L-1,c(H2O)=3 mol·L-1,平衡时CO的转化率为60%,水蒸气的转化率为
(2)830 K,若只将起始时c(H2O)改为6 mol·L-1,则水蒸气的转化率为
(3)若830 K时,起始浓度c(CO)=a mol·L-1,c(H2O)=b mol·L-1,H2的平衡浓度c(H2)=c mol·L-1,则:
①a、b、c之间的关系式是
②当a=b时,a=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】某小组以盐酸、醋酸为例探究其酸性的强弱。按要求回答下列问题。
(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知: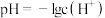
③此温度下,CH3COOH的电离平衡常数Ka=___________ (填计算式,不化简)。
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=___________ mol;充分反应后,剩余的n(Mg)=___________ mol。
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。___________

(1)取相同体积、相同浓度的盐酸和醋酸,分别测其pH和导电能力,对比分析,在下表填写空白。已知:
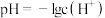
| 酸 | 0.1mol/L盐酸 | 0.1mol/L醋酸 | |
| pH(25℃) | 1 | 3 | |
| 导电能力 | 强 | 弱 | |
| 分析与结论 | ①微观解释(写出溶质在溶液中的存在形式,填粒子的化学式) | ||
| ②电离方程式 | |||
(2)在上述醋酸溶液中加入如下表所示物质,分析其中粒子的变化等,填写空白。
| 加入少量的物质 | 醋酸电离平衡移动方向 填“→”“←”或“不移动” | c(H⁺)/c(CH3COOH)比值变化 填“变大”“变小”或“不变” |
| ①CH3COONa(s) | ||
| ②水 |
(3)向两个锥形瓶中各加入0.06g镁条,塞紧橡胶塞,然后用注射器分别注入2mL 2mol/L盐酸、2mol/L醋酸。
①反应前n(Mg)=
②两锥形瓶内气体n随时间变化,对比分析后,在如下坐标中将示意曲线补充完整。

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】电离平衡常数是衡量弱电解质电离程度大小的量,已知部分物质的电离常数如表所示,请回答下列有关问题。
(1)向一定浓度的 溶液滴入酚酞的现象为
溶液滴入酚酞的现象为___________ ,请用离子方程式解释原因:___________ 。
(2)25℃时,等浓度的①NaClO溶液,② 溶液,③
溶液,③ 溶液,三种溶液的pH值由大到小的顺序为
溶液,三种溶液的pH值由大到小的顺序为___________ (用序号表示)。
(3)下列微粒可以大量共存的是___________。
(4)体积均为10mL、pH=2的醋酸溶液与某一元酸a分别加水稀释至1000mL,稀释过程pH变化如图:
(5)
(6)
在体积、pH均相同的 与某一元酸a中加入足量的锌,生成的氢气在标准状况下的体积大小关系:
与某一元酸a中加入足量的锌,生成的氢气在标准状况下的体积大小关系:
___________ 某酸a(填“>”、“<”或“=”)。
(7)高氯酸、硫酸的酸性不同,但在水溶液中难于区分他们的酸性强弱,因为二者在水溶液中均完全电离,但是在冰醋酸中能够区分,已知硫酸在冰醋酸中部分电离,请写出硫酸在冰醋酸中的电离方程式:___________ 。
| 化学式 | 电离平衡常数(25℃) |
| HClO | 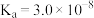 |
 |  |
 | 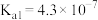 、 、 |
 | 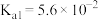 、 、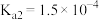 |
 |  |
(1)向一定浓度的
 溶液滴入酚酞的现象为
溶液滴入酚酞的现象为(2)25℃时,等浓度的①NaClO溶液,②
 溶液,③
溶液,③ 溶液,三种溶液的pH值由大到小的顺序为
溶液,三种溶液的pH值由大到小的顺序为(3)下列微粒可以大量共存的是___________。
A. 、 、 | B. 、HClO 、HClO |
C. 、 、 | D. 、 、 |
(4)体积均为10mL、pH=2的醋酸溶液与某一元酸a分别加水稀释至1000mL,稀释过程pH变化如图:
(5)
(6)

在体积、pH均相同的
 与某一元酸a中加入足量的锌,生成的氢气在标准状况下的体积大小关系:
与某一元酸a中加入足量的锌,生成的氢气在标准状况下的体积大小关系:
(7)高氯酸、硫酸的酸性不同,但在水溶液中难于区分他们的酸性强弱,因为二者在水溶液中均完全电离,但是在冰醋酸中能够区分,已知硫酸在冰醋酸中部分电离,请写出硫酸在冰醋酸中的电离方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】电解质在水溶液中可能存在电离平衡、水解平衡、溶解平衡等。
(1)已知部分弱酸的电离常数如下表:
①室温下,一定浓度的HCOONa溶液 ,用离子方程式表示溶液呈碱性的原因
,用离子方程式表示溶液呈碱性的原因___________ 。
②0.1 mol·L-1 NaCN溶液和0.1 mol·L-1 溶液中,
溶液中,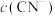
___________  (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
③将 通入NaCN溶液,反应的离子方程式是
通入NaCN溶液,反应的离子方程式是___________ 。
(2)常温时,向20 mL 0.1 mol/L 水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(δ)随pH变化的关系如图所示。
的物质的量分数(δ)随pH变化的关系如图所示。

则曲线Ⅱ表示___________ 微粒,弱酸 的
的
___________
(3)已知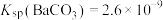 ,
,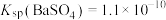 。
。
①将浓度为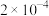 mol⋅L-1
mol⋅L-1  溶液与
溶液与 溶液
溶液等体积混合 ,则生成 沉淀所需
沉淀所需 溶液的最小浓度为
溶液的最小浓度为___________ mol⋅L-1。
②向含有 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中,写出沉淀转化的离子方程式
沉淀生成时,溶液中,写出沉淀转化的离子方程式___________ ,求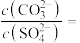
___________ (保留三位有效数字)。
(1)已知部分弱酸的电离常数如下表:
| 弱酸 | HCOOH | HCN |  |
| 电离常数(25℃) | 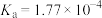 | 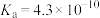 | 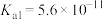 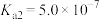 |
 ,用离子方程式表示溶液呈碱性的原因
,用离子方程式表示溶液呈碱性的原因②0.1 mol·L-1 NaCN溶液和0.1 mol·L-1
 溶液中,
溶液中,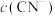
 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。③将
 通入NaCN溶液,反应的离子方程式是
通入NaCN溶液,反应的离子方程式是(2)常温时,向20 mL 0.1 mol/L
 水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中
水溶液中逐滴滴加0.1 mol/L NaOH溶液,混合溶液中 、
、 和
和 的物质的量分数(δ)随pH变化的关系如图所示。
的物质的量分数(δ)随pH变化的关系如图所示。
则曲线Ⅱ表示
 的
的
(3)已知
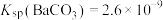 ,
,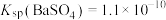 。
。①将浓度为
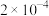 mol⋅L-1
mol⋅L-1  溶液与
溶液与 溶液
溶液 沉淀所需
沉淀所需 溶液的最小浓度为
溶液的最小浓度为②向含有
 固体的溶液中滴加
固体的溶液中滴加 溶液,当有
溶液,当有 沉淀生成时,溶液中,写出沉淀转化的离子方程式
沉淀生成时,溶液中,写出沉淀转化的离子方程式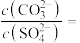
您最近一年使用:0次



