习总书记在十九大报告中明确指出:“宁要绿水青山,不要金山银山,而且绿水青山就是金山银山。”保护环境是我们的迫切需要。请回答下列问题:
(1) 会带来温室效应。目前,工业上采用氢气还原
会带来温室效应。目前,工业上采用氢气还原 制备乙醇的方法已经实现:
制备乙醇的方法已经实现: 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入
 和
和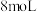
 ,在一定温度下反应,测得混合气体中
,在一定温度下反应,测得混合气体中 与时间的关系如图所示。
与时间的关系如图所示。

① 内,
内,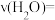
______  ;
;
②反应达到平衡时,
______ mol;
③在该温度下,该反应的化学平衡常数K______ (保留两位小数)。
(2)在恒容密闭容器中发生反应: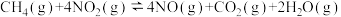
①下列说法能作为判断该反应达到化学平衡状态标志的是______ ;
A.容器内混合气体的密度保持不变
B.v正(NO2)=4v逆(CO2)
C.容器内压强保持不变
D.单位时间内,消耗nmol NO2的同时生成nmol NO
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为______ 反应(填“放热”或“吸热”)。
(3)在恒容密闭容器中,由CO可合成甲醇: ,回答问题:
,回答问题:
①该反应的化学平衡常数的表达式为______ ;
②若升高温度,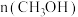 减少,则该反应为
减少,则该反应为______ 反应(填“放热”或“吸热”),若将体系温度升高,达到平衡时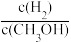
______ (填“增大”、“减小”或“不变”) 。
(1)
 会带来温室效应。目前,工业上采用氢气还原
会带来温室效应。目前,工业上采用氢气还原 制备乙醇的方法已经实现:
制备乙醇的方法已经实现: 。在2L恒容密闭容器中充入
。在2L恒容密闭容器中充入
 和
和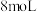
 ,在一定温度下反应,测得混合气体中
,在一定温度下反应,测得混合气体中 与时间的关系如图所示。
与时间的关系如图所示。
①
 内,
内,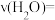
 ;
;②反应达到平衡时,

③在该温度下,该反应的化学平衡常数K
(2)在恒容密闭容器中发生反应:
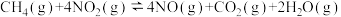
①下列说法能作为判断该反应达到化学平衡状态标志的是
A.容器内混合气体的密度保持不变
B.v正(NO2)=4v逆(CO2)
C.容器内压强保持不变
D.单位时间内,消耗nmol NO2的同时生成nmol NO
②若此时将容器的体积缩小为原来的0.5倍,达到平衡时,容器内温度将降低(容器不与外界进行热交换),则该反应的正反应为
(3)在恒容密闭容器中,由CO可合成甲醇:
 ,回答问题:
,回答问题:①该反应的化学平衡常数的表达式为
②若升高温度,
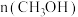 减少,则该反应为
减少,则该反应为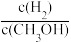
更新时间:2020-12-18 20:27:13
|
相似题推荐
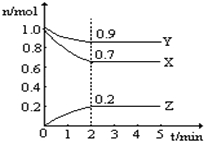
【推荐1】恒温下在2L密闭容器中,X、Y、Z三种气态物质的量随时间变化曲线如图。

(1)该反应的化学方程式为________ 。
(2)从开始至5min,Y的平均反应速率为________ ;平衡时,Z的物质的量浓度为________ ,X的转化率为________ 。
(3)反应达平衡时体系的压强是开始时的________ 倍。
(4)下列描述中能表明反应已达到平衡状态的是________ (填序号)。
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤Z 的物质的量浓度不变
的物质的量浓度不变
⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻 且不等于零 ⑧单位时间内生成2nmolZ,同时生成3nmolX
且不等于零 ⑧单位时间内生成2nmolZ,同时生成3nmolX
(5)在某一时刻采取下列措施能加快反应速率的是________。

(1)该反应的化学方程式为
(2)从开始至5min,Y的平均反应速率为
(3)反应达平衡时体系的压强是开始时的
(4)下列描述中能表明反应已达到平衡状态的是
①容器内温度不变 ②混合气体的密度不变 ③混合气体的压强不变
④混合气体的平均相对分子质量不变 ⑤Z
 的物质的量浓度不变
的物质的量浓度不变⑥容器内X、Y、Z三种气体的浓度之比为3:1:2
⑦某时刻
 且不等于零 ⑧单位时间内生成2nmolZ,同时生成3nmolX
且不等于零 ⑧单位时间内生成2nmolZ,同时生成3nmolX(5)在某一时刻采取下列措施能加快反应速率的是________。
| A.加催化剂 | B.降低温度 |
| C.体积不变,充入X | D.体积不变,从容器中分离出Y |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】在2L密闭容器中,800℃时反应2NO(g)+O2(g) 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:
(1)如图表示各物质浓度的变化曲线,A点处,v(正)___________ v(逆),A点正反应速率___________ B点正反应速率。(用“大于”“小于”或“等于”填空)。

(2)图中表示O2变化的曲线是___________ 。用NO2表示从0~2s内该反应的平均速率v=___________ 。
(3)能说明该反应已经达到平衡状态的是___________。
(4)能使该反应的反应速率增大的是___________。
 2NO2(g)体系中,n(NO)随时间的变化如表:
2NO2(g)体系中,n(NO)随时间的变化如表:| 时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |

(2)图中表示O2变化的曲线是
(3)能说明该反应已经达到平衡状态的是___________。
| A.容器内颜色保持不变 | B.v(NO)=2v(O2) |
| C.容器内的密度保持不变 | D.NO的质量百分数不变 |
| A.适当升高温度 | B.选择高效的催化剂 |
| C.减小O2的浓度 | D.及时分离出NO2气体 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐3】某温度时,在一个10L的恒容容器中,X、Y、Z均为气体,三种物质的物质的量随时间的变化曲线如图所示.根据图中数据填空:
(1)该反应的化学方程式为____________________ ;
(2)反应开始至2min,以气体Z表示的平均反应速率为______________________ ;
(3)平衡时容器内混合气体密度比起始时__________ (填“变大”,“变小”或“相等”下同),混合气体的平均相对分子质量比起始时___________ ;
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
n(X)=n(Y)=2n(Z),则原混合气体中a:b=___________ 。
(5)在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(Ⅰ)一定能证明2SO2(g)+O2(g) 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是_______ (填序号,下同)。
(Ⅱ)一定能证明I2(g)+H2(g) 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是 _________ 。
(Ⅲ)一定能证明A(s)+2B(g) C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是________ 。
(1)该反应的化学方程式为
(2)反应开始至2min,以气体Z表示的平均反应速率为
(3)平衡时容器内混合气体密度比起始时
(4)将a mol X与b mol Y的混合气体发生上述反应,反应到某时刻各物质的量恰好满足:
n(X)=n(Y)=2n(Z),则原混合气体中a:b=
(5)在恒温恒容的密闭容器中,当下列物理量不再发生变化时:①混合气体的压强,②混合气体的密度,③混合气体的总物质的量,④混合气体的平均相对分子质量,⑤混合气体的颜色,⑥各反应物或生成物的反应速率之比等于化学计量数之比
(Ⅰ)一定能证明2SO2(g)+O2(g)
 2SO3(g)达到平衡状态的是
2SO3(g)达到平衡状态的是(Ⅱ)一定能证明I2(g)+H2(g)
 2HI(g)达到平衡状态的是
2HI(g)达到平衡状态的是 (Ⅲ)一定能证明A(s)+2B(g)
 C(g)+D(g)达到平衡状态的是
C(g)+D(g)达到平衡状态的是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】随着氮氧化物对环境及人类活动影响的日趋严重,如何消除大气污染物中的氮氧化物成为人们关注的主要问题之一。利用 NH3的还原性可以消除氮氧化物的污染, 其中除去 NO 的主要反应如下:4NH3(g)+6NO(g)  5N2(g)+6H2O(l)△H<0
5N2(g)+6H2O(l)△H<0
(1)一定温度下,在恒容密闭容器中按照 n(NH3)︰n(NO) =2︰3 充入反应物,发生上述反应。下列不能判断该反应达到平衡状态的是________________________ 。
A.c(NH3)︰c(NO) =2︰3
B.n(NH3)︰n(N2) 不变
C.容器内压强不变
D.容器内混合气体的密度不变
E.1molN—H 键断裂的同时,生成 1molO—H 键
(2)已知该反应速率 正=k 正·c4(NH3)·c6 (NO),
正=k 正·c4(NH3)·c6 (NO), 逆=k 逆·cx(N2)·cy(H2O) (k 正、k 逆分别是正、逆反应速率常数),该反应的平衡常数 K=k 正/k 逆,则 x=
逆=k 逆·cx(N2)·cy(H2O) (k 正、k 逆分别是正、逆反应速率常数),该反应的平衡常数 K=k 正/k 逆,则 x=___________________ ,y=____________________ 。
(3)某研究小组将 2molNH3、3molNO 和一定量的O2充入 2L 密闭容器中,在 Ag2O 催化剂表面发生上述反应,NO 的转化率随温度变化的情况如图所示。
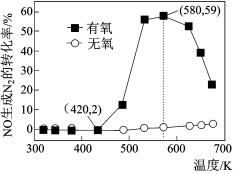
①在 5min 内,温度从 420K 升高到 580K,此时段内NO 的平均反应速率 (NO)=
(NO)=__________________ ;
②在有氧条件下,温度 580K 之后 NO 生成 N2的转化率降低的原因可能是_____________________ 。
 5N2(g)+6H2O(l)△H<0
5N2(g)+6H2O(l)△H<0(1)一定温度下,在恒容密闭容器中按照 n(NH3)︰n(NO) =2︰3 充入反应物,发生上述反应。下列不能判断该反应达到平衡状态的是
A.c(NH3)︰c(NO) =2︰3
B.n(NH3)︰n(N2) 不变
C.容器内压强不变
D.容器内混合气体的密度不变
E.1molN—H 键断裂的同时,生成 1molO—H 键
(2)已知该反应速率
 正=k 正·c4(NH3)·c6 (NO),
正=k 正·c4(NH3)·c6 (NO), 逆=k 逆·cx(N2)·cy(H2O) (k 正、k 逆分别是正、逆反应速率常数),该反应的平衡常数 K=k 正/k 逆,则 x=
逆=k 逆·cx(N2)·cy(H2O) (k 正、k 逆分别是正、逆反应速率常数),该反应的平衡常数 K=k 正/k 逆,则 x=(3)某研究小组将 2molNH3、3molNO 和一定量的O2充入 2L 密闭容器中,在 Ag2O 催化剂表面发生上述反应,NO 的转化率随温度变化的情况如图所示。

①在 5min 内,温度从 420K 升高到 580K,此时段内NO 的平均反应速率
 (NO)=
(NO)=②在有氧条件下,温度 580K 之后 NO 生成 N2的转化率降低的原因可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】空气质量的好坏与空气中氮、硫氧化物的含量有着重要的关联,控制氮、硫氧化物的排放有利于改善空气质量。
(1)目前我国已对许多大型燃煤发电厂进行“脱硝(使NOx转化为N2)”工艺改造,这有利于氮元素在自然界中实现良性循环,“脱硝”涉及到的部分反应如下:
①4NH3(g)+6NO(g) 5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;
5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;
②8NH3(g)+6NO2(g) 7N2(g)+12H2O(g) △H2;
7N2(g)+12H2O(g) △H2;
又知:③N2(g)+O2(g) 2NO(g) △H3=+180kJ·mol-1;
2NO(g) △H3=+180kJ·mol-1;
④2NO(g)+O2(g) 2NO2(g) △H4=-114kJ·mol-1
2NO2(g) △H4=-114kJ·mol-1
则△H2=__________ 。
(2)氨的催化氧化是硝酸工业中最重要的一个反应:4NH3(g)+5O2(g) 4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。
4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。

①物质a是___________ ,前3 min内用H2O表示的平均反应速率v(H2O)=____________ 。
②若最初通入的O2物质的量为3.3mol,则该温度下反应的平衡常数的值为________ 。
③下列各项数据中能表明该反应已达到化学平衡状态的是_________ (填选项字母)。
a. NH3与NO的生成速率相等 b.混合气体的密度保持不变
c. △H 保持不变 d.容器的总压强保持不变
(3)将NO2、NO混合气体用碱吸收可得到重要的化工产品NaNO2,已知常温下K(HNO2)=5×10-4,则5mol/L的NaNO2溶液的pH=________ 。
(4)消除SO2污染的方法之一是利用电化学法可直接将其转化为硫酸,转化原理如图2所示,则负极上的电极反应式为____________________________ ,质子的移动方向为____________________ (填“自左向右”或“自右向左”)。
(1)目前我国已对许多大型燃煤发电厂进行“脱硝(使NOx转化为N2)”工艺改造,这有利于氮元素在自然界中实现良性循环,“脱硝”涉及到的部分反应如下:
①4NH3(g)+6NO(g)
 5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;
5N2(g)+6H2O(g) △H1=-1776kJ·mol-1;②8NH3(g)+6NO2(g)
 7N2(g)+12H2O(g) △H2;
7N2(g)+12H2O(g) △H2;又知:③N2(g)+O2(g)
 2NO(g) △H3=+180kJ·mol-1;
2NO(g) △H3=+180kJ·mol-1;④2NO(g)+O2(g)
 2NO2(g) △H4=-114kJ·mol-1
2NO2(g) △H4=-114kJ·mol-1则△H2=
(2)氨的催化氧化是硝酸工业中最重要的一个反应:4NH3(g)+5O2(g)
 4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。
4NO(g)+6H2O(g) △H=-905kJ·mol-1;一定温度下,向2L某恒容密闭容器充入一定量的NH3、O2,测得NO与某种物质a的浓度与时间的关系如图1所示。
①物质a是
②若最初通入的O2物质的量为3.3mol,则该温度下反应的平衡常数的值为
③下列各项数据中能表明该反应已达到化学平衡状态的是
a. NH3与NO的生成速率相等 b.混合气体的密度保持不变
c. △H 保持不变 d.容器的总压强保持不变
(3)将NO2、NO混合气体用碱吸收可得到重要的化工产品NaNO2,已知常温下K(HNO2)=5×10-4,则5mol/L的NaNO2溶液的pH=
(4)消除SO2污染的方法之一是利用电化学法可直接将其转化为硫酸,转化原理如图2所示,则负极上的电极反应式为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在500℃时,将足量的A固体投入2.0L真空密闭容器中,发生A(s) 2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:

(1)已知该反应只有高温下能自发进行,则该反应的△H___________ 0(填“>”、“<”或“=”)。
(2)在上述反应条件下,从反应开始到平衡,用V(B)=___________ mol·L-1·min-1,500℃时的平衡常数K=___________ ;
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是_________ ;
A.混合气体的压强保持不变 B.气体C的体积分数保持不变
C.混合气体的密度保持不变 D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。_______
 2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
2B(g)+C(g)反应,测得气体C随时间的浓度变化如图所示:
(1)已知该反应只有高温下能自发进行,则该反应的△H
(2)在上述反应条件下,从反应开始到平衡,用V(B)=
(3)在反应温度和容器体积不变的条件下,下列能说明上述反应达到平衡状态的是
A.混合气体的压强保持不变 B.气体C的体积分数保持不变
C.混合气体的密度保持不变 D.B的正反应速率等于C的逆反应速率
(4)在500℃时,上述反应达到平衡后,在8min时将容器体积迅速压缩为1.0L,反应在12min建立新的平衡,画出8~15min内C气体物质的量浓度随时间变化的示意图。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】高炉炼铁中发生的基本反应之一如下:
FeO(s)+CO(g) Fe(s)+CO2(g) ΔH<0,K=0.263。
Fe(s)+CO2(g) ΔH<0,K=0.263。
(1)该反应平衡常数可表示为K=________ 。
(2)当压强增大后,该反应的平衡常数将________ (填“增大”“减小”或“不变”)。
(3)1 100 ℃时测得高炉中c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,在这种情况下,该反应是否处于化学平衡状态?________ (填“是”或“否”),此时,化学反应速率是v正________ v逆(填“大于”“小于”或“等于”)。
FeO(s)+CO(g)
 Fe(s)+CO2(g) ΔH<0,K=0.263。
Fe(s)+CO2(g) ΔH<0,K=0.263。(1)该反应平衡常数可表示为K=
(2)当压强增大后,该反应的平衡常数将
(3)1 100 ℃时测得高炉中c(CO2)=0.025 mol·L-1,c(CO)=0.1 mol·L-1,在这种情况下,该反应是否处于化学平衡状态?
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】CO在工业生产中具有重要作用。
(1)CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
已知△G=△H-T△S,反应CO(g)+2H2(g) CH3OH(g)的△G随温度的变化是图1中的
CH3OH(g)的△G随温度的变化是图1中的____ (填“L1”或“L2”)。

(2)已知在催化剂M作用下,NO2(g)+CO(g) CO2(g)+NO(g) △H<0。
CO2(g)+NO(g) △H<0。
①一定温度下,假设正逆反应速率与浓度关系为v正=k1c(NO2)•c(CO),v逆=k2c(CO2)•c(NO),k1、k2只与温度相关,则反应的平衡常数K=____ (用含k1、k2的式子表示)。
②催化剂M活性随温度变化情况如图2所示,相同时间测得NO2的转化率随反应温度变化情况如图3所示,写出T0后NO2的转化率出现如图变化的可能原因_____ 。

③在图3中画出并标注,其他条件不变,增大压强(催化剂不失活)情况下,NO2的转化率随温度变化图_____ 。
(1)CO(g)+2H2(g)
 CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-12CH3OH(g)
 CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1已知△G=△H-T△S,反应CO(g)+2H2(g)
 CH3OH(g)的△G随温度的变化是图1中的
CH3OH(g)的△G随温度的变化是图1中的
(2)已知在催化剂M作用下,NO2(g)+CO(g)
 CO2(g)+NO(g) △H<0。
CO2(g)+NO(g) △H<0。①一定温度下,假设正逆反应速率与浓度关系为v正=k1c(NO2)•c(CO),v逆=k2c(CO2)•c(NO),k1、k2只与温度相关,则反应的平衡常数K=
②催化剂M活性随温度变化情况如图2所示,相同时间测得NO2的转化率随反应温度变化情况如图3所示,写出T0后NO2的转化率出现如图变化的可能原因

③在图3中画出并标注,其他条件不变,增大压强(催化剂不失活)情况下,NO2的转化率随温度变化图
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】化学反应原理在科研和生产中有广泛应用。CO可用于合成甲醇,一定温度下,向体积为2 L的密闭容器中加入CO和H2,发生反应CO(g)+2H2(g)  CH3OH(g),达到平衡后测得各组分的浓度如下:
CH3OH(g),达到平衡后测得各组分的浓度如下:
(1)反应达到平衡时,CO的转化率为________ 。
(2)该反应的平衡常数K=________ 。
(3)恒温恒容条件下,可以说明反应已达到平衡状态的是________ (填字母)。
A.v正(CO)=2v逆(H2)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(4)若将容器体积压缩到1 L,则达到新平衡时c(H2)的取值范围是___________ 。
(5)若保持容器体积不变,再充入0.6 mol CO和0.4 mol CH3OH,此时v正________ v逆(填“>”“<”或“=”)。
 CH3OH(g),达到平衡后测得各组分的浓度如下:
CH3OH(g),达到平衡后测得各组分的浓度如下:| 物质 | CO | H2 | CH3OH |
| 浓度/(mol·L-1) | 0.9 | 1.0 | 0.6 |
(1)反应达到平衡时,CO的转化率为
(2)该反应的平衡常数K=
(3)恒温恒容条件下,可以说明反应已达到平衡状态的是
A.v正(CO)=2v逆(H2)
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.CH3OH、CO、H2的浓度都不再发生变化
(4)若将容器体积压缩到1 L,则达到新平衡时c(H2)的取值范围是
(5)若保持容器体积不变,再充入0.6 mol CO和0.4 mol CH3OH,此时v正
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知A(g)+B(g)⇌C(g)+D(g)反应的平衡常数和温度的关系如表:
回答下列问题:
(1)该反应的平衡常数表达式K=_______ ,∆H_______ 0(填“<”“>”“=”);
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1.,则6s时c(A)=_______ mol•L-1,C的物质的量为_______ mol;若反应经一段时间后,达到平衡时A的转化率为_______ ,如果这时向该密闭容器中再充入1mol氩气,平衡时A的转化率为_______ ;
(3)1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为_______ 。
| |温度/℃ | 700 | 900 | 830 | 1000 | 1200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
(1)该反应的平衡常数表达式K=
(2)830℃时,向一个5L的密闭容器中充入0.20mol的A和0.80mol的B,如反应初始6s内A的平均反应速率v(A)=0.003mol•L-1•s-1.,则6s时c(A)=
(3)1200℃时反应C(g)+D(g)⇌A(g)+B(g)的平衡常数的值为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】工业废水中常含有一定量的 ,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。已知元素铬(Cr)在溶液中主要以
沉淀。已知元素铬(Cr)在溶液中主要以 (蓝紫色)、
(蓝紫色)、 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。
为难溶于水的灰蓝色固体。
(1) 在强碱中可被双氧水氧化为
在强碱中可被双氧水氧化为 ,发生反应的离子方程式为
,发生反应的离子方程式为_______________ 。
(2) 和
和 在溶液中可相互转化。室温下,初始浓度为
在溶液中可相互转化。室温下,初始浓度为 的
的 溶液中
溶液中 随
随 的变化如图所示。
的变化如图所示。

①由图可知,溶液酸性增大, 的平衡转化率
的平衡转化率________ (填“增大“减小”或“不变”)。
②据A点数据,计算出该转化反应的平衡常数________ 。
③初始浓度为 的
的 溶液中加入一定量的硝酸至溶液的
溶液中加入一定量的硝酸至溶液的 ,则溶液由
,则溶液由_____ 转变到____ (填溶液颜色)。
 ,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将
,易被人体吸收累积而导致肝癌。处理工业含铬废水的方法通常是将 转化为
转化为 ,再将
,再将 转化为
转化为 沉淀。已知元素铬(Cr)在溶液中主要以
沉淀。已知元素铬(Cr)在溶液中主要以 (蓝紫色)、
(蓝紫色)、 (绿色)、
(绿色)、 (橙红色)、
(橙红色)、 (黄色)等形式存在,
(黄色)等形式存在, 为难溶于水的灰蓝色固体。
为难溶于水的灰蓝色固体。(1)
 在强碱中可被双氧水氧化为
在强碱中可被双氧水氧化为 ,发生反应的离子方程式为
,发生反应的离子方程式为(2)
 和
和 在溶液中可相互转化。室温下,初始浓度为
在溶液中可相互转化。室温下,初始浓度为 的
的 溶液中
溶液中 随
随 的变化如图所示。
的变化如图所示。
①由图可知,溶液酸性增大,
 的平衡转化率
的平衡转化率②据A点数据,计算出该转化反应的平衡常数
③初始浓度为
 的
的 溶液中加入一定量的硝酸至溶液的
溶液中加入一定量的硝酸至溶液的 ,则溶液由
,则溶液由
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】在某温度下,将H2和I2各1mol的气态混合物充入10L的密闭容器中发生反应H2(g)+I2(g) 2HI(g)ΔH<0,充分反应达到平衡后,测得c(H2)=0.08mol/L,容器内压强为p(Pa)。
2HI(g)ΔH<0,充分反应达到平衡后,测得c(H2)=0.08mol/L,容器内压强为p(Pa)。
(1)保持容器容积不变,向其中再加入1molH2,反应速率_______ (填“加快”、“变慢”或“不变”),平衡________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(2)保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率_______ (填“加快”、“变慢”或“不变”),平衡________ 移动(填“向正反应方向”、“向逆反应方向”或“不”)。
(3)该反应的化学平衡常数K=__________ 。
(4)在上述温度下,将容器体积压缩至原来的一半,混合气体颜色将_______ (填序号)
A.加深 B.变浅 C.先变深后变浅 D.先变浅后变深 E.不变
(5)在上述温度下,将H2和I2各2mol的气态混合物充入10L的恒容密闭容器中,达到化学平衡状态时,c(H2)=______ ,容器内压强为_________ 。
 2HI(g)ΔH<0,充分反应达到平衡后,测得c(H2)=0.08mol/L,容器内压强为p(Pa)。
2HI(g)ΔH<0,充分反应达到平衡后,测得c(H2)=0.08mol/L,容器内压强为p(Pa)。(1)保持容器容积不变,向其中再加入1molH2,反应速率
(2)保持容器内气体压强不变,向其中加入1molN2(N2不参加反应),反应速率
(3)该反应的化学平衡常数K=
(4)在上述温度下,将容器体积压缩至原来的一半,混合气体颜色将
A.加深 B.变浅 C.先变深后变浅 D.先变浅后变深 E.不变
(5)在上述温度下,将H2和I2各2mol的气态混合物充入10L的恒容密闭容器中,达到化学平衡状态时,c(H2)=
您最近一年使用:0次



