下列物质A~F是我们熟悉的单质或化合物,其中A、B均是常见的金属,且B的合金用量最大;E在常温下是黄绿色气体;在适当的条件下,它们之间可以发生如下图所示的转化。
试回答下列问题:
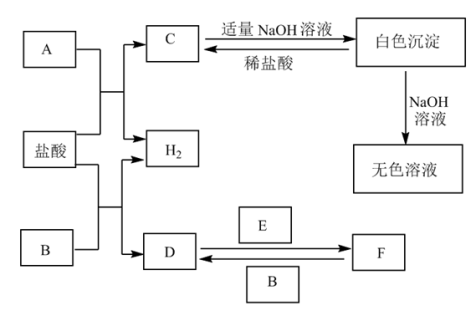
(1)A在周期表中的位置是_________________ ;
(2)检验F中金属阳离子的常用方法是_____________________________________ 。
(3)白色沉淀与NaOH溶液反应的离子方程式是________________________________ 。
(4)反应F→D的化学方程式是_____________________________________ 。
试回答下列问题:

(1)A在周期表中的位置是
(2)检验F中金属阳离子的常用方法是
(3)白色沉淀与NaOH溶液反应的离子方程式是
(4)反应F→D的化学方程式是
更新时间:2016-12-09 07:21:21
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
【推荐1】A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成.B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为_______
(2)下表为B与F实验的部分内容
写出B与稀H2SO4反应的离子方程式________
写出②中反应的化学方程式________
(3)现由6种粒子Mn2+、 、H+、H2O、
、H+、H2O、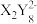 (C中含有的阴离子)、
(C中含有的阴离子)、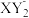 完成一个离子方程式,已知Mn2+为还原剂,得到1 mol
完成一个离子方程式,已知Mn2+为还原剂,得到1 mol  需氧化剂的物质的量为
需氧化剂的物质的量为________ mol
(4)化合物D和E相互转化D E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为
E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为________ g,E•xH2O的化学式为________ .
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为_______
A.离子键  | B.极性共价键 | C.非极性共价键 | D.氢键 |
| ①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
| ②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色,且用激光笔照射有丁达尔效应。 |
写出②中反应的化学方程式
(3)现由6种粒子Mn2+、
 、H+、H2O、
、H+、H2O、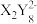 (C中含有的阴离子)、
(C中含有的阴离子)、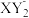 完成一个离子方程式,已知Mn2+为还原剂,得到1 mol
完成一个离子方程式,已知Mn2+为还原剂,得到1 mol  需氧化剂的物质的量为
需氧化剂的物质的量为(4)化合物D和E相互转化D
 E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为
E,若有D和E•xH2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐2】在下图所示的物质转化关系中,A是常见的气态氢化物,B是能使带火星的木条复燃的无色无味气体,C是造成酸雨的主要原因,G是一种红色金属单质(反应条件和部分生成物未列出)。
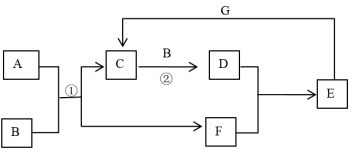
(1)A的电子式为_______ ,C的化学式为_______ 。
(2)写出化学方程式:①_______ ;②_______ 。
(3)在E→C的反应中,表现了E的_______ 性。
(4)C是常见的大气污染物,可在燃煤中加入生石灰,该反应的方程式为_______ 。

(1)A的电子式为
(2)写出化学方程式:①
(3)在E→C的反应中,表现了E的
(4)C是常见的大气污染物,可在燃煤中加入生石灰,该反应的方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】 、
、 、
、 、
、 四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8,
四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8, 元素原子的
元素原子的 层电子数与
层电子数与 、
、 层电子数之和相等,
层电子数之和相等, 元素原子的
元素原子的 、
、 层电子数之和等于电子总数的一半。试回答下列问题。
层电子数之和等于电子总数的一半。试回答下列问题。
(1)四种元素的符号依次是
______ ,
______ ,
______ ,
______ ;它们的原子半径由大到小的顺序是______ (用元素符号表示)。
(2)试写出四种元素的离子结构示意图:
______ ,
______ ,
______ ,
______ 。它们的离子半径由大到小的顺序是______ (用离子符号表示)。
(3)分别写出四种元素的最高价氧化物对应水化物的化学式:______ 。
(4)分别写出 、
、 两元素的气态氢化物的化学式:
两元素的气态氢化物的化学式:______ 。
 、
、 、
、 、
、 四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8,
四种元素原子的核电荷数依次增大,它们的简单离子的电子层数相同且最外层电子数均为8, 元素原子的
元素原子的 层电子数与
层电子数与 、
、 层电子数之和相等,
层电子数之和相等, 元素原子的
元素原子的 、
、 层电子数之和等于电子总数的一半。试回答下列问题。
层电子数之和等于电子总数的一半。试回答下列问题。(1)四种元素的符号依次是




(2)试写出四种元素的离子结构示意图:




(3)分别写出四种元素的最高价氧化物对应水化物的化学式:
(4)分别写出
 、
、 两元素的气态氢化物的化学式:
两元素的气态氢化物的化学式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】氯气是重要的化工原料,在生产和生活中应用广泛。兴趣小组以“氯气的制备、收集及性质”为主题开展探究性学习。
(1)氯气的制备与收集。实验装置如下图所示。

①装置A中反应的化学方程式是__________ 。
②装置B的作用是__________ 。
③装置C中盛放的物质X是__________ 。
④装置E用于吸收尾气,E中反应的离子方程式是__________ 。
(2)影响氯气溶解性的因素。为了探究影响氯气在 溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
实验测得 在不同浓度的
在不同浓度的 、
、 溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
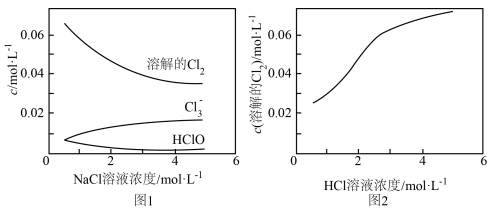
图1 图2
①从图1可以看出,氯气溶于 溶液时主要发生了两个反应,一是
溶液时主要发生了两个反应,一是 与水的反应,二是
与水的反应,二是__________ (填反应的离子方程式)。随着 溶液浓度的增大,
溶液浓度的增大, 与水的反应受到了抑制,证据是
与水的反应受到了抑制,证据是___________ 。
②结合图1、2可知,导致 在
在 溶液中溶解性随
溶液中溶解性随 溶液浓度增大而变小的微粒应是
溶液浓度增大而变小的微粒应是___________ (填微粒符号)。
(1)氯气的制备与收集。实验装置如下图所示。

①装置A中反应的化学方程式是
②装置B的作用是
③装置C中盛放的物质X是
④装置E用于吸收尾气,E中反应的离子方程式是
(2)影响氯气溶解性的因素。为了探究影响氯气在
 溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:
溶液中溶解性的因素,兴趣小组通过查阅资料,获得如下信息:实验测得
 在不同浓度的
在不同浓度的 、
、 溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
溶液中溶解达到饱和时的浓度及部分含氯微粒的浓度如图1、图2所示。
图1 图2
①从图1可以看出,氯气溶于
 溶液时主要发生了两个反应,一是
溶液时主要发生了两个反应,一是 与水的反应,二是
与水的反应,二是 溶液浓度的增大,
溶液浓度的增大, 与水的反应受到了抑制,证据是
与水的反应受到了抑制,证据是②结合图1、2可知,导致
 在
在 溶液中溶解性随
溶液中溶解性随 溶液浓度增大而变小的微粒应是
溶液浓度增大而变小的微粒应是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】为了证明在实验室制备Cl2的过程中会有水蒸气和HCl挥发出来,小明设计了如图所示的实验装置,按要求填空。
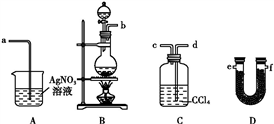
①请根据小明的意图,连接相应的装置,接口顺序: 接 , 接 , 接 。(填字母)____________
②U形管中所盛试剂的化学式为_____________ ;
③装置C中CCl4的作用是__________________ ;
④小红认为小明的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,小红同学提出在某两个装置之间再加装置F。你认为装置F应加在____ 之间(填装置序号)。瓶中可以放入_______ ;
⑤小强看到小明设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成________ ,如果观察到________ 的现象,则证明制Cl2时有HCl挥发出来。

①请根据小明的意图,连接相应的装置,接口顺序: 接 , 接 , 接 。(填字母)
②U形管中所盛试剂的化学式为
③装置C中CCl4的作用是
④小红认为小明的实验有缺陷,不能证明最终通入AgNO3溶液中的气体只有一种。为了确保实验结论的可靠性,证明最终通入AgNO3溶液的气体只有一种,小红同学提出在某两个装置之间再加装置F。你认为装置F应加在
⑤小强看到小明设计的装置后提出无需多加装置,只需将原来烧杯中的AgNO3溶液换成其他溶液。你认为可将溶液换成
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
【推荐3】针对下列9种元素,完成以下各小题
(1)常见单质为有色气体的元素是_______ (填名称)。
(2)用电子式表示元素④和⑨形成化合物的过程_________ 。
(3)最高价氧化物对应的水化物中酸性最强的是_________ (填化学式)。
(4)④和⑥两者的最高价氧化物对应的水化物反应的离子方程式为_______ 。
(5)⑦的单质的用途正确的是_____ 。
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(6)元素①和⑦非金属性较强的是____ (填写元素符号),写出一个能表示二者非金属性强弱关系的化学方程式为:_______ 。
| 周期 | IA | ⅡA | ⅢA | ⅣA | ⅥA | ⅦA | O | |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)用电子式表示元素④和⑨形成化合物的过程
(3)最高价氧化物对应的水化物中酸性最强的是
(4)④和⑥两者的最高价氧化物对应的水化物反应的离子方程式为
(5)⑦的单质的用途正确的是
A.光导纤维 B.太阳能电池 C.普通玻璃 D.计算机芯片
(6)元素①和⑦非金属性较强的是
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
名校
解题方法
【推荐1】某混合物A含有KAl(SO4)2、Al2O3和Fe2O3,在一定条件下可实现下图所示的物质之间的变化:

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是____________ 。
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B_________________ ;沉淀D __________________ ;
溶液E_________________________________________ 。
(3)写出①、④两个反应的化学方程式
①__________________________________ ;④_____________________________ 。
(4)写出②、③两个反应的离子方程式
②_________________________________ ;③______________________________ 。
(5)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3__________________________ Fe2O3____________________________ 。

据此回答下列问题:
(1)I、II、III、IV四步中对于溶液和沉淀的分离采取的方法是
(2)根据上述框图反应关系,写出下列B、D、E所含物质的化学式
固体B
溶液E
(3)写出①、④两个反应的化学方程式
①
(4)写出②、③两个反应的离子方程式
②
(5)分别写出Al2O3和Fe2O3在工业上的一种主要用途:
Al2O3
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】工业上的许多反应工艺来源于实验室里的简单操作,比如用铝土矿(成分为氧化铝、氧化铁)制取铝的过程如图:

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式___ 。
(2)沉淀C的化学式___ ,颜色为___ ,写出它的一种用途___ 。
(3)操作I、操作II、操作III的名称为___ ,这个过程用到的玻璃仪器有烧杯、___ 。
(4)整个生产过程中,除可以循环使用的物质有___ (写出3种,填化学式),用此法制取铝的副产品是___ (写出2种,填化学式)。
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?___ 。

请回答下列问题:
(1)写出铝土矿中加入NaOH溶液的反应方程式
(2)沉淀C的化学式
(3)操作I、操作II、操作III的名称为
(4)整个生产过程中,除可以循环使用的物质有
(5)氧化铝熔点高,氯化铝熔点低,工业上为什么不用熔点较低的氯化铝而用熔点更高的氧化铝为原料电解制铝?
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】A、B、C、D均为中学化学中常见的物质,它们之间转化关系如图所示(部分产物和条件已略去),回答下列问题:

(1)若A为能形成温室效应的气体,D为NaOH溶液,则C的化学式为_____________ 。
(2)若常温时A为气态氢化物,B为淡黄色固体单质,则A与C反应生成B的化学方程式为_____________ ,氧化剂与还原剂物质的量之比_____________ 。
(3)若A为黄绿色气体,D为常见金属,则A与C生成B的离子方程式为_____________ 。向C溶液滴加NaOH溶液的现象_____________ 。

(1)若A为能形成温室效应的气体,D为NaOH溶液,则C的化学式为
(2)若常温时A为气态氢化物,B为淡黄色固体单质,则A与C反应生成B的化学方程式为
(3)若A为黄绿色气体,D为常见金属,则A与C生成B的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】已知A为某种金属单质,有以下物质之间的相互转化:

试回答:
(1)写出各物质的化学式A__ ,C__ 。
(2)向G溶液中滴加KSCN的实验现象是__ 。
(3)向G溶液中加入A的有关反应的离子方程式为__ 。
(4)写出E→F的化学方程式:__ 。

试回答:
(1)写出各物质的化学式A
(2)向G溶液中滴加KSCN的实验现象是
(3)向G溶液中加入A的有关反应的离子方程式为
(4)写出E→F的化学方程式:
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐3】A、B、C为中学常见单质,其中一种为金属;通常情况下,A为固体,B为液体,C为气体。D、E、F、G、H、X均为化合物,其中X是一种无氧强酸、E为黑色固体,H在常温下为液体。它们之间的转化关系如图所示(其中某些反应条件和部分反应物已略去)。
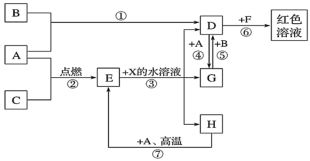
(1)写出化学式:A___________ X___________
(2)在反应①~⑦中,不属于氧化还原反应的是___________ (填编号)。
(3)反应⑥的离子方程式为___________ ;
(4)反应⑦的化学方程式为___________ ;该反应中每消耗3 mol的A,可转移电子___________ mol。

(1)写出化学式:A
(2)在反应①~⑦中,不属于氧化还原反应的是
(3)反应⑥的离子方程式为
(4)反应⑦的化学方程式为
您最近一年使用:0次




