短周期元素X、Y、Z、W、U原子序数依次递增。X与W位于同一主族,Z元素的单质既能与盐酸反应也能与NaOH溶液反应,W原子的最外层电子数是次外层电子数的一半,Z、W、U原子的最外层电子数之和为13。Y元素的单质在X的某种氧化物中可燃。下列说法正确的是
| A.X、W、U的最高价氧化物对应的水化物酸性由强到弱的顺序为:U>W>X |
| B.Y、Z元素的单质作电极,在NaOH溶液中构成原电池,Z电极上产生大量气泡 |
| C.室温下,0.05 mol·L-1U的气态氢化物的水溶液的pH>1 |
| D.Y、Z、U元素的简单离子半径由大到小的顺序:Y>Z>U |
更新时间:2016-12-09 07:42:14
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】根据元素周期律,由下列事实进行归纳推测,推测不合理 的是
| 事实 | 推测 | |
| A | 12Mg与水反应缓慢,20Ca与水反应较快 | 56Ba(ⅡA族)与水反应会更快 |
| B | Si与H2高温时反应,S与H2加热能反应 | P与H2在高温时能反应 |
| C | HCl在1500℃时分解,HI在230℃时分解 | HBr的分解温度介于二者之间 |
| D | Si是半导体材料,同族的Ge也是半导体材料 | ⅣA族的元素单质都是半导体材料 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】已知 As元素的部分信息如图所示,下列说法不正确的是


| A.H3AsO4和H3PO4都能与NaOH溶液反应生成相应的盐 |
| B.热稳定性:AsH3、H2S、HCl逐渐增强 |
C.As的一种核素表示为 ,中子数为40 ,中子数为40 |
| D.原子半径由大到小的顺序:As、Cl、Si |
您最近一年使用:0次
【推荐1】一种工业洗涤剂中间体的结构如图,其中 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是
 、
、 、
、 、
、 、
、 原子序数依次增大且分属三个短周期。
原子序数依次增大且分属三个短周期。 、
、 元素的基态原子中均有两个未成对电子,下列说法正确的是
元素的基态原子中均有两个未成对电子,下列说法正确的是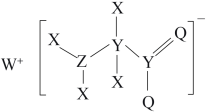
A.电负性大小: |
B.简单离子半径: |
C.简单氢化物的沸点: |
D.阴离子中各原子都满足 电子稳定结构 电子稳定结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】几种短周期元素的原子半径及主要化合价如下表:
则X可能的数值为
| 元素符号 | A | B | C | D | E |
| 原子半径(nm) | 0.160 | 0.080 | X | 0.143 | 0.074 |
| 主要化合价 | +2 | +2 | -2,+4,+6 | +3 | -2 |
| A.0.069 | B.0.102 | C.0.145 | D.0.184 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】主族元素W、X、Y、Z的原子序数均不超过20,X、Y、Z位于同周期,它们形成的一种化合物的结构如下图所示,其中X、Y、Z的电子数之和与W的电子数相等。下列说法正确的是


| A.原子半径:W>X>Y>Z |
| B.简单气态氢化物的热稳定性Y比X的强 |
| C.Z的最高价氧化物对应的水化物是强酸 |
| D.该阴离子中各原子最外层均满足8电子结构 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】短周期元素R、T、Q、W在元素周期表中的相对位置如图所示,其中T所处的周期序数与族序数相等。下列判断不正确的是( )
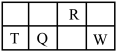

| A.最简单气态氢化物的热稳定性:R>Q |
| B.最高价氧化物对应水化物的酸性:Q<W |
| C.原子半径:T>Q>R |
| D.T的最高价氧化物对应的水化物不能和强碱反应 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】短周期主族元素A、B、C、D的原子序数依次增大,A和B形成的气态化合物的水溶液呈碱性,B位于第ⅤA族,A和C同主族,D原子最外层电子数与电子层数相等。下列叙述正确的是:
| A.原子半径:D>C>B | B.元素A、B、C的氧化物均为共价化合物 |
| C.单质的还原性:D>C | D.元素B、C、D的最高价氧化物对应水化物能相互反应 |
您最近一年使用:0次



