某兴趣小组利用以下实验装置模拟工业炼铁的主要过程:
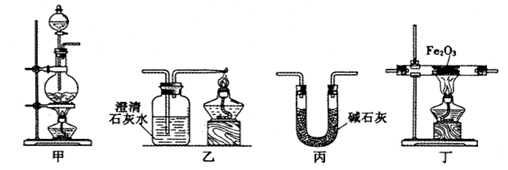
(1)装置甲中发生的反应为:HCOOH(甲酸)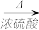 CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该
CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该______________ (填字母)。
a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→( ) →( ) →( )
(3)丙装置中碱石灰的作用是__________________________ 。
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为__________ 。
(5)为了探究影响反应产物的外界因素,在Fe2O3,与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
①甲同学猜想黑色产物中可能含有碳单质。乙同学排除了该可能,他提出的两种理由是:____ 、____ 。
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.________ ;iii.___________ 。
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
样品I的成分及质量分数为______________________ 。
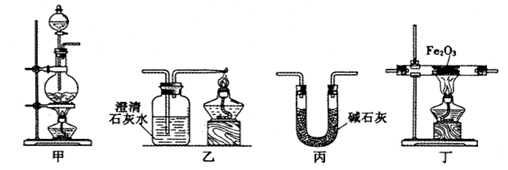
(1)装置甲中发生的反应为:HCOOH(甲酸)
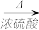 CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该
CO↑+H2O。已知甲酸是一种无色有刺激性气味的液体。制取一氧化碳时应该a.将甲酸滴入浓硫酸 b.将浓硫酸滴入甲酸 c.将甲酸与浓硫酸混合后加入
(2)请按合适的顺序连接好以下装置:甲→
(3)丙装置中碱石灰的作用是
(4)实验将近完成时,熄灭装置甲、乙、丁中酒精灯的先后顺序为
(5)为了探究影响反应产物的外界因素,在Fe2O3,与CO反应部位,该小组同学分别用酒精灯和酒精喷灯进行了两次实验,结果如下:
| 加热方式 | 通CO加热时间/min | 澄清石灰水变浑浊时间/min | 产物颜色 | 产物能否全部被磁铁吸引 |
| 酒精灯 | 30 | 5 | 黑色 | 能 |
| 酒精喷灯 | 30 | 1 | 黑色 | 能 |
①甲同学猜想黑色产物中可能含有碳单质。乙同学排除了该可能,他提出的两种理由是:
②丙同学查找资料发现,Fe3O4也能被磁铁吸引,对黑色产物成分提出以下三种假设:i.全部为铁;ii.
③通过进一步定量实验,黑色产物所含元素组成和质量分数如下:
| 样品序号 | 加热方式 | 元素组成和质量分数 |
| 产物样品I | 酒精灯 | w(Fe)=74.4%、w(O)=25.6% |
| 产物样品II | 酒精喷灯 | w(Fe)=100% |
样品I的成分及质量分数为
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-工业流程题
|
困难
(0.15)
解题方法
【推荐1】分高铁酸钾(K2FeO4)是一种集氧化、吸附、絮凝于一体的新型多功能水处理剂。其生产工艺如下:
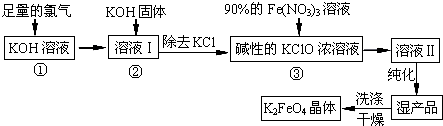
(1)反应①应在温度较低的情况下进行。因在温度较高时KOH 与Cl2反应生成的是KClO3。写出在温度较高时KOH 与Cl2反应的化学方程式___________ ,该反应的氧化产物是___________ 。
(2)在溶液I中加入KOH固体的目的是___________ (填编号)
(3)从溶液II中分离出K2FeO4后,还会有副产品KNO3、KCl,则反应③中发生的离子反应方程式为___________ 。
(4)如何判断K2FeO4晶体已经洗涤干净___________ 。
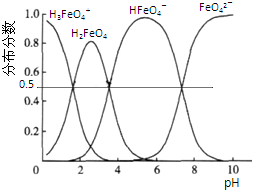
(5)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO42-的存在形态如下图所示.下列说法正确的是___________ 。

(1)反应①应在温度较低的情况下进行。因在温度较高时KOH 与Cl2反应生成的是KClO3。写出在温度较高时KOH 与Cl2反应的化学方程式
(2)在溶液I中加入KOH固体的目的是
| A.与溶液I中过量的Cl2继续反应,生成更多的KClO |
| B.KOH固体溶解时会放出较多的热量,有利于提高反应速率 |
| C.为下一步反应提供碱性的环境 |
| D.使KClO3转化为 KClO |
(4)如何判断K2FeO4晶体已经洗涤干净
(5)高铁酸钾(K2FeO4)具有极强的氧化性,是一种优良的水处理剂.其水溶液中FeO42-的存在形态如下图所示.下列说法正确的是

| A.不论溶液酸碱性如何变化,铁元素都有4种存在形态 |
| B.向pH=2的这种溶液中加KOH溶液至pH=10,HFeO4-的分布分数先增大后减小 |
| C.向pH=8的这种溶液中加KOH溶液,发生反应的离子方程式为:H2FeO4+OH-=HFeO4-+H2O |
您最近一年使用:0次
【推荐2】绿色化学在推动社会可持续发展中发挥着重要作用。某科研团队设计了一种熔盐液相氧化法制备高价铬盐的新工艺,该工艺不消耗除铬铁矿、氢氧化钠和空气以外的其他原料,不产生废弃物,实现了 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
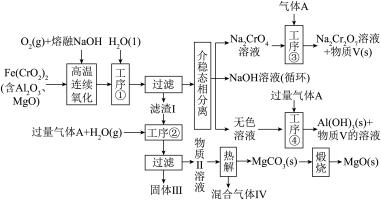
回答下列问题:
(1) 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:_________ 。
(2)滤渣Ⅰ的主要成分是_________ (填化学式)。工序③中发生反应的离子方程式为_________ 。
(3)热解工序产生的混合气体Ⅳ最适宜返回工序_________ (填“①”或“②”或“③”或“④”)参与内循环。
(4) 难溶于水,常温时
难溶于水,常温时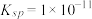 ;
; 难溶于水,能溶于强酸、强碱。
难溶于水,能溶于强酸、强碱。
①欲使 的
的 溶液中的
溶液中的 沉淀完全(离子浓度小于
沉淀完全(离子浓度小于 ),需加入等体积浓度至少为
),需加入等体积浓度至少为_________  的
的 溶液。
溶液。
②20℃时,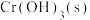 在不同浓度的NaOH溶液中的最大溶解量(
在不同浓度的NaOH溶液中的最大溶解量( )如图1所示。下列叙述正确
)如图1所示。下列叙述正确_________ 的是(填字母)。
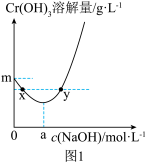
A.NaOH浓度越小,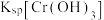 越小
越小
B.x、y两点对应的溶液中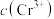 不相等
不相等
C.当NaOH浓度小于 时,随着NaOH浓度的增大,
时,随着NaOH浓度的增大, 溶解量减小是因为
溶解量减小是因为 浓度增大使
浓度增大使 溶解平衡逆向移动
溶解平衡逆向移动
D.当NaOH浓度为 时,溶液中
时,溶液中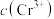 一定最小
一定最小
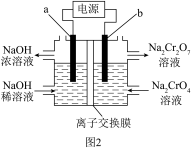
(5)工序③也可以利用电解法制 ,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为
,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为_________ (填离子符号)交换膜。制备 时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少_________ g。
 的深度利用和
的深度利用和 内循环。工艺流程如图:
内循环。工艺流程如图:
回答下列问题:
(1)
 中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:
中Cr元素的化合价为+3价,写出高温连续氧化工序中该物质发生反应的化学方程式:(2)滤渣Ⅰ的主要成分是
(3)热解工序产生的混合气体Ⅳ最适宜返回工序
(4)
 难溶于水,常温时
难溶于水,常温时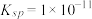 ;
; 难溶于水,能溶于强酸、强碱。
难溶于水,能溶于强酸、强碱。①欲使
 的
的 溶液中的
溶液中的 沉淀完全(离子浓度小于
沉淀完全(离子浓度小于 ),需加入等体积浓度至少为
),需加入等体积浓度至少为 的
的 溶液。
溶液。②20℃时,
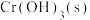 在不同浓度的NaOH溶液中的最大溶解量(
在不同浓度的NaOH溶液中的最大溶解量( )如图1所示。下列叙述正确
)如图1所示。下列叙述正确
A.NaOH浓度越小,
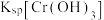 越小
越小B.x、y两点对应的溶液中
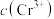 不相等
不相等C.当NaOH浓度小于
 时,随着NaOH浓度的增大,
时,随着NaOH浓度的增大, 溶解量减小是因为
溶解量减小是因为 浓度增大使
浓度增大使 溶解平衡逆向移动
溶解平衡逆向移动D.当NaOH浓度为
 时,溶液中
时,溶液中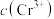 一定最小
一定最小(5)工序③也可以利用电解法制
 ,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为
,工作原理如下图2所示(a、b电极均为石墨)。该装置中的离子交换膜为 时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
时,若电路中有4mol电子转移时,理论上右侧溶液总质量减少
您最近一年使用:0次
解答题-工业流程题
|
困难
(0.15)
名校
【推荐3】辉铜矿主要成分Cu2S,此外还含有少量SiO2、Fe2O3等杂质,软锰矿主要含有MnO2,以及少量SiO2、Fe2O3等杂质.研究人员开发综合利用这两种资源,用同槽酸浸湿法冶炼工艺,制备硫酸锰晶体和碱式碳酸铜。主要工艺流程如下:

已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4
④MnSO4·H2O溶于1份冷水、0.6份沸水,不溶于乙醇。
(1)实验室配制250mL 4.8mol•L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要________________________ 。
(2)酸浸时,为了提高浸取率可采取的措施有_____________________ (任写一点)。
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式:__________ 。
(4)调节浸出液pH=4的作用是______________ 。
(5)本工艺中可循环使用的物质是____________ (写化学式)。
(6)获得的MnSO4•H2O晶体需要进一步洗涤、干燥,洗涤时应用_____________ 洗涤。
(7)测定MnSO4•H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为________________ 。

已知:
①MnO2有较强的氧化性,能将金属硫化物中的硫氧化为单质硫;
②[Cu(NH3)4]SO4常温稳定,在热水溶液中会分解生成NH3;
③部分金属阳离子生成氢氧化物沉淀的pH范围(开始沉淀和完全沉淀的pH):
Fe3+:1.5~3.2 Mn2+:8.3~9.8 Cu2+:4.4~6.4
④MnSO4·H2O溶于1份冷水、0.6份沸水,不溶于乙醇。
(1)实验室配制250mL 4.8mol•L-1的稀硫酸,所需的玻璃仪器除玻璃棒、量筒、烧杯以外还需要
(2)酸浸时,为了提高浸取率可采取的措施有
(3)酸浸时,得到浸出液中主要含有CuSO4、MnSO4等。写出该反应的化学方程式:
(4)调节浸出液pH=4的作用是
(5)本工艺中可循环使用的物质是
(6)获得的MnSO4•H2O晶体需要进一步洗涤、干燥,洗涤时应用
(7)测定MnSO4•H2O样品的纯度:准确称取样品14.00g,加蒸馏水配成100mL溶液,取出25.00mL用标准的BaCl2溶液测定,完全反应后得到了4.66g沉淀,则此样品的纯度为
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐1】实验室用废铁屑制取无水氯化铁并测其纯度。实验方案如下:
Ⅰ. 制备
制备
①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是_______ 。
(2)控制温度在40~50℃的原因是_______ 。
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为_______ 。
Ⅱ.无水 制备
制备
已知 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。
(4)按图装置进行实验。锥形瓶中生成无水 的总化学方程式为
的总化学方程式为_______ ;仪器A的作用是_______ 。
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用 溶液滴定(
溶液滴定(
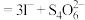 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。
①所制产品的纯度为_______ (以无水 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);
②所制产品中可能含有 杂质,检验
杂质,检验 的试剂为
的试剂为_______ (填化学式)溶液;产生 的原因可能是
的原因可能是_______ 。
Ⅰ.
 制备
制备①将废铁屑加入30%NaOH溶液中,煮沸30分钟,过滤,洗涤2~3次。
②将洗涤后废铁屑加入20%盐酸,控制温度在40~50℃之间,至反应完毕,过滤。
③向滤液中逐滴加入10%双氧水,同时加入25%盐酸,充分搅拌至溶液呈棕黄色。
④将溶液转移至蒸发皿中,加热浓缩,缓慢冷却至大量晶体析出,抽滤,洗涤。
回答下列问题:
(1)用NaOH溶液洗涤废铁屑的目的是
(2)控制温度在40~50℃的原因是
(3)滴加10%双氧水时,滴加速率过快会产生气泡。该气体为
Ⅱ.无水
 制备
制备已知
 熔点―156℃,沸点77℃,易水解生成
熔点―156℃,沸点77℃,易水解生成 和HCl。
和HCl。(4)按图装置进行实验。锥形瓶中生成无水
 的总化学方程式为
的总化学方程式为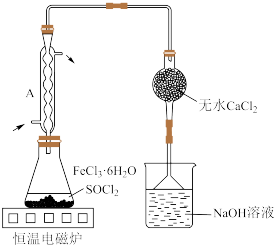
(5)称取3.250g产品试样,配制成100.00mL溶液,取20.00mL于锥形瓶中,加入足量KI溶液,经充分反应后,滴入淀粉溶液3~5滴,然后用
 溶液滴定(
溶液滴定(
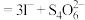 ),经三次平行实验,平均消耗
),经三次平行实验,平均消耗 溶液19.00ml。
溶液19.00ml。①所制产品的纯度为
 质量分数表示,保留三位有效数字);
质量分数表示,保留三位有效数字);②所制产品中可能含有
 杂质,检验
杂质,检验 的试剂为
的试剂为 的原因可能是
的原因可能是
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
【推荐2】硫酸亚铁容易被氧化,而硫酸亚铁铵晶体[(NH4)2SO4·FeSO4·6H2O]较稳定,常用于代替硫酸亚铁作还原剂。现以铁屑为主要原料制备硫酸亚铁铵晶体,其反应如下:Fe+H2SO4(稀)=FeSO4+H2↑、FeSO4+(NH4)2SO4+6H2O=(NH4)2SO4·FeSO4·6H2O
步骤l:在盛有适量铁屑的锥形瓶里加入某种试剂除去油污,加热,充分反应后过滤、洗涤、干燥、称量,铁屑质量为 1。
1。
步骤2:将处理过的铁屑加入到一定量的稀H2SO4中,加热至50℃—80℃充分反应,趁热过滤并用少量热水洗涤,滤液及洗涤液都转移至蒸发皿中。滤渣干燥后称重,剩余铁屑质量为 。
。
步骤3:准确称取所需质量的硫酸铵晶体加入“步骤2”的蒸发皿中,搅拌使之溶解,缓缓加热一段时间,将其冷却结晶、过滤。用无水乙醇洗涤晶体并自然干燥,称量所得晶体质量为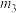 。
。
回答下列问题:
(1)能够用于除去铁屑表面油污的试剂是___________ (填字母)。
(2)步骤2中趁热过滤的目的是________________ 。
(3)硫酸亚铁在潮湿的空气中易被氧化生成一种物质(碱式硫酸铁),该反应的化学方程式为__________________________ 。
(4)铁屑表面常有少量的铁锈(Fe2O3· H2O),对FeSO4的制备
H2O),对FeSO4的制备_____ (填“有”、“无”)影响,理由是(用离子方程式回答)____________________________ 。
(5)若忽略铁锈的影响,上述实验中硫酸亚铁铵晶体的产率为_______ 。
(6)请设计一个简单的实验,检验硫酸亚铁铵晶体中含有结晶水(简述实验操作、现象和结论)________________________________________________________ 。
步骤l:在盛有适量铁屑的锥形瓶里加入某种试剂除去油污,加热,充分反应后过滤、洗涤、干燥、称量,铁屑质量为
 1。
1。步骤2:将处理过的铁屑加入到一定量的稀H2SO4中,加热至50℃—80℃充分反应,趁热过滤并用少量热水洗涤,滤液及洗涤液都转移至蒸发皿中。滤渣干燥后称重,剩余铁屑质量为
 。
。步骤3:准确称取所需质量的硫酸铵晶体加入“步骤2”的蒸发皿中,搅拌使之溶解,缓缓加热一段时间,将其冷却结晶、过滤。用无水乙醇洗涤晶体并自然干燥,称量所得晶体质量为
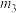 。
。回答下列问题:
(1)能够用于除去铁屑表面油污的试剂是
| A.纯碱溶液 | B.烧碱溶液 | C.明矾溶液 | D.稀硫酸 |
(3)硫酸亚铁在潮湿的空气中易被氧化生成一种物质(碱式硫酸铁),该反应的化学方程式为
(4)铁屑表面常有少量的铁锈(Fe2O3·
 H2O),对FeSO4的制备
H2O),对FeSO4的制备(5)若忽略铁锈的影响,上述实验中硫酸亚铁铵晶体的产率为
(6)请设计一个简单的实验,检验硫酸亚铁铵晶体中含有结晶水(简述实验操作、现象和结论)
您最近一年使用:0次
解答题-实验探究题
|
困难
(0.15)
解题方法
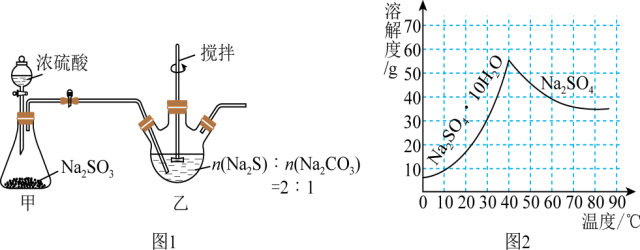
【推荐3】Na2S2O3又名“大苏打”“海波”,易溶于水,难溶于乙醇,水溶液呈微弱的碱性,在中性和碱性环境中稳定。某化学实验小组用如图1装置(略去对乙的加热装置)制备Na2S2O3·5H2O(M=248g·mol-1),已知:Na2SO4溶解度如图2所示。_______ 。
(2)在装置乙中溶解两种固体时,需先将Na2CO3溶于水配成溶液,再将Na2S固体溶于Na2CO3的溶液中,其目的_______ ;装置乙中生成Na2S2O3的总反应方程式为_______ 。
(3)实验过程中,当装置乙中pH接近7.0时,应立即停止通SO2的原因是________ (用离子方程式表示)。
(4)装置乙中需向反应后的混合液加入一定量的无水乙醇,其目的是_______ 。
(5)设计实验测定Na2S2O3·5H2O的纯度:
步骤1:准确称取16.00g样品,溶于水,加入10mL甲醛,配成200mL溶液。
步骤2:准确称取0.294gK2Cr2O7于碘量瓶中,加入 蒸馏水溶解,再加入5mL2mol·L-1硫酸溶液和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
蒸馏水溶解,再加入5mL2mol·L-1硫酸溶液和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
步骤3:向碘量瓶中加入1mL1%淀粉溶液,用待测Na2S2O3溶液滴定碘量瓶中溶液至终点,消耗Na2S2O3溶液 。(已知:I2+2S2O
。(已知:I2+2S2O =2I-+S4O
=2I-+S4O ),试计算Na2S2O3·5H2O的纯度为
),试计算Na2S2O3·5H2O的纯度为_______ (保留三位有效数字)。
(6)利用甲装置中的残渣(Na2SO4和Na2SO3的混合物)制备Na2SO4·10H2O晶体,将下列实验方案补充完整:将固体混合物溶于水配成溶液,_______ ,洗涤、干燥得Na2SO4·10H2O晶体。(实验中须使用氧气、pH计)
(2)在装置乙中溶解两种固体时,需先将Na2CO3溶于水配成溶液,再将Na2S固体溶于Na2CO3的溶液中,其目的
(3)实验过程中,当装置乙中pH接近7.0时,应立即停止通SO2的原因是
(4)装置乙中需向反应后的混合液加入一定量的无水乙醇,其目的是
(5)设计实验测定Na2S2O3·5H2O的纯度:
步骤1:准确称取16.00g样品,溶于水,加入10mL甲醛,配成200mL溶液。
步骤2:准确称取0.294gK2Cr2O7于碘量瓶中,加入
 蒸馏水溶解,再加入5mL2mol·L-1硫酸溶液和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。
蒸馏水溶解,再加入5mL2mol·L-1硫酸溶液和20mL10%KI溶液使铬元素完全转化为Cr3+,加水稀释至100mL。步骤3:向碘量瓶中加入1mL1%淀粉溶液,用待测Na2S2O3溶液滴定碘量瓶中溶液至终点,消耗Na2S2O3溶液
 。(已知:I2+2S2O
。(已知:I2+2S2O =2I-+S4O
=2I-+S4O ),试计算Na2S2O3·5H2O的纯度为
),试计算Na2S2O3·5H2O的纯度为(6)利用甲装置中的残渣(Na2SO4和Na2SO3的混合物)制备Na2SO4·10H2O晶体,将下列实验方案补充完整:将固体混合物溶于水配成溶液,
您最近一年使用:0次



