为了探究AgNO3的氧化性和热稳定性,某化学兴趣小组设计了如下实验。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用试剂:①KSCN溶液 ②NaOH溶液 ③酸性KMnO4溶液 ④K3[Fe(CN)6]溶液。
(1)请完成下表:
【实验结论】Fe的氧化产物为Fe2+和Fe3+
Ⅱ.AgNO3的热稳定性
用下图所示的实验装置A加热固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。
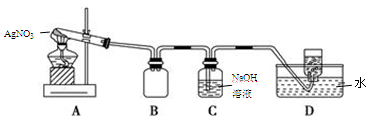
(2)装置B的作用是 。
(3)经小组讨论并验证该无色气体为O2,其操作方法是 。
(4)【查阅资料】①Ag2O和粉末的Ag均为黑色;②Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:①Ag;②Ag2O;③Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验:
【实验评价】根据上述实验,不能确定固体产物成分的实验是 (填实验编号)。
【实验结论】根据上述实验结果,得出AgNO3固体受热分解的化学方程式为 。
【实验拓展】另取2.0g AgNO3样品充分受热分解,共收集到标准状况下气体的体积为336mL,则样品中AgNO3的百分含量为 。
Ⅰ.AgNO3的氧化性
将光亮的铁丝伸入AgNO3溶液中,一段时间后将铁丝取出。为检验溶液中Fe的氧化产物,将溶液中的Ag+除尽后,进行了如下实验。可选用试剂:①KSCN溶液 ②NaOH溶液 ③酸性KMnO4溶液 ④K3[Fe(CN)6]溶液。
(1)请完成下表:
| 操作 | 现象 | 结论 |
| 取少量除尽Ag+后的溶液于试管中,加入KSCN溶液,振荡 | | 存在Fe3+ |
| 取少量除尽Ag+后的溶液于试管中,加入1~2滴 (填序号)溶液,振荡 | | 存在Fe2+ |
Ⅱ.AgNO3的热稳定性
用下图所示的实验装置A加热固体,产生红棕色气体,在装置D中收集到无色气体。当反应结束以后,试管中残留固体为黑色。

(2)装置B的作用是 。
(3)经小组讨论并验证该无色气体为O2,其操作方法是 。
(4)【查阅资料】①Ag2O和粉末的Ag均为黑色;②Ag2O可溶于氨水。
【提出假设】试管中残留的黑色固体可能是:①Ag;②Ag2O;③Ag和Ag2O。
【实验验证】该小组为验证上述设想,分别取少量黑色固体,进行了如下实验:
| 实验编号 | 操 作 | 现 象 |
| a | 加入足量氨水,振荡 | 黑色固体不溶解 |
| b | 加入足量稀硝酸,振荡 | 黑色固体溶解,并有气体产生 |
【实验结论】根据上述实验结果,得出AgNO3固体受热分解的化学方程式为 。
【实验拓展】另取2.0g AgNO3样品充分受热分解,共收集到标准状况下气体的体积为336mL,则样品中AgNO3的百分含量为 。
更新时间:2016-12-09 07:49:45
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
真题
【推荐1】某种催化剂为铁的氧化物。化学兴趣小组在实验室对该催化剂中铁元素的价态进行探究:将适量稀硝酸加入少许样品中,加热溶解;取少许溶液,滴加KSCN溶液后出现红色。一位同学由此得出该催化剂中铁元素价态为+3的结论。
(1)请指出该结论是否合理并说明理由________ 。
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KMnO4、NaOH稀溶液、0.1 mol·L-1KI、20% KSCN、蒸馏水。
①提出合理假设:
假设1:_______ ;
假设2:_______ ;
假设3:_______ 。
②设计实验方案证明你的假设(不要在答题卡上作答)。
③实验过程:
根据②的实验方案,进行实验。请写出实验操作步骤、预期现象与结论_______ 。
(1)请指出该结论是否合理并说明理由
(2)请完成对铁元素价态的探究:
限选实验仪器与试剂:烧杯、试管、玻璃棒、药匙、滴管、酒精灯、试管夹:3 mol·L-1H2SO4/3% H2O2、6 mol·L-1HNO3/0.01 mol·L-1KMnO4、NaOH稀溶液、0.1 mol·L-1KI、20% KSCN、蒸馏水。
①提出合理假设:
假设1:
假设2:
假设3:
②设计实验方案证明你的假设(不要在答题卡上作答)。
③实验过程:
根据②的实验方案,进行实验。请写出实验操作步骤、预期现象与结论
| 实验操作 | 预期现象与结论 |
| 步骤1: | |
| 步骤2: | |
| 步骤3: | |
| … |
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐2】为严厉打击食品生产经营中违法添加非食用物质、滥用食品添加剂,卫生部、农业部等部门联合公布了包含硫酸亚铁在内的22种“易滥用食品添加剂”名单。某同学为探究富含硫酸亚铁且保存时间较长的食品情况,设计了如下实验方案:

(1)试剂1的主要成分的化学式是________ 。
(2)加入新制氯水后溶液红色加深的原因是_____________ (用离子方程式表示)。
(3)该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1:溶液中的+3价铁被氧化为更高价态的铁;
假设2:___________ 。
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案:_______ 。

(1)试剂1的主要成分的化学式是
(2)加入新制氯水后溶液红色加深的原因是
(3)该同学在实验中加入了过量氯水,放置一段时间后,发现深红色褪去,现对褪色原因进行探究。
①提出假设
假设1:溶液中的+3价铁被氧化为更高价态的铁;
假设2:
②设计方案
为了对你所提出的假设2进行验证,请写出一种实验方案:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐3】某无色透明溶液中可能大量存在Ag+、Mg2+、Cu2+、Fe3+、Na+中的几种,请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子有_______ 。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是_______ ,有关的离子方程式为_______ 。
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有_______ , 有关的离子方程式为_______ 。
(4)原溶液可能大量存在的阴离子是下列的_______ 。
A.Cl- B. C.
C.
(1)不做任何实验就可以肯定原溶液中不存在的离子有
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是
(3)取(2)中的滤液,加入过量的NaOH溶液,出现白色沉淀,说明液中肯定有
(4)原溶液可能大量存在的阴离子是下列的
A.Cl- B.
 C.
C.
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】工业上利用锌焙砂(主要成分为ZnO,含有少量CuO、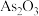 ,NiO等)生产高纯ZnO的流程示意图如下。
,NiO等)生产高纯ZnO的流程示意图如下。

(1)用足量 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。
①“浸出”前,锌焙砂预先粉碎的目的是___________ 。
②通过“浸出”步骤,锌焙砂中的ZnO转化为 ,该反应的离子方程式为
,该反应的离子方程式为___________ 。
(2)“除重金属”时,加入BaS溶液。滤渣Ⅱ中含有的主要物质是___________ 和 。
。
(3)“蒸氨”时会出现白色固体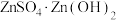 ,运用平衡移动原理解释原因
,运用平衡移动原理解释原因___________ 。
(4)“沉锌”步骤①中加入足量 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为___________ 。
(5)“煅烧”步骤中,不同温度下, 分解的失重曲线和产品ZnO的比表面积变化情况如图1、图2所示。
分解的失重曲线和产品ZnO的比表面积变化情况如图1、图2所示。
已知:i.固体失重质量分数
ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品ZnO的活性越高。

①280℃时煅烧 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为___________ (保留到小数点后一位)。
②根据图1和图2,获得高产率( 分解率>95%)、高活性(ZnO比表面积
分解率>95%)、高活性(ZnO比表面积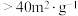 )产品ZnO的最佳条件是
)产品ZnO的最佳条件是___________ (填字母序号)。
a.恒温280℃,60~120min b.恒温300℃,240~300min
c.恒温350℃,240~300min d.恒温550℃,60~120min
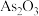 ,NiO等)生产高纯ZnO的流程示意图如下。
,NiO等)生产高纯ZnO的流程示意图如下。
(1)用足量
 溶液和氨水“浸出”锌焙砂。
溶液和氨水“浸出”锌焙砂。①“浸出”前,锌焙砂预先粉碎的目的是
②通过“浸出”步骤,锌焙砂中的ZnO转化为
 ,该反应的离子方程式为
,该反应的离子方程式为(2)“除重金属”时,加入BaS溶液。滤渣Ⅱ中含有的主要物质是
 。
。(3)“蒸氨”时会出现白色固体
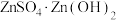 ,运用平衡移动原理解释原因
,运用平衡移动原理解释原因(4)“沉锌”步骤①中加入足量
 溶液将白色固体转化为
溶液将白色固体转化为 的离子方程式为
的离子方程式为(5)“煅烧”步骤中,不同温度下,
 分解的失重曲线和产品ZnO的比表面积变化情况如图1、图2所示。
分解的失重曲线和产品ZnO的比表面积变化情况如图1、图2所示。已知:i.固体失重质量分数

ii.比表面积指单位质量固体所具有的总面积;比表面积越大,产品ZnO的活性越高。

①280℃时煅烧
 ,300min后固体失重质量分数为33.3%,则
,300min后固体失重质量分数为33.3%,则 的分解率为
的分解率为②根据图1和图2,获得高产率(
 分解率>95%)、高活性(ZnO比表面积
分解率>95%)、高活性(ZnO比表面积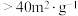 )产品ZnO的最佳条件是
)产品ZnO的最佳条件是a.恒温280℃,60~120min b.恒温300℃,240~300min
c.恒温350℃,240~300min d.恒温550℃,60~120min
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上以硫铁矿为原料制硫酸所产生的尾气除了含有N2、O2外,还含有SO2、微量的SO3和酸雾。为了保护环境,同时提高硫酸工业的综合经济效益,按照如图的工艺流程,将尾气中的SO2转化为有用的副产品。请回答下列问题。
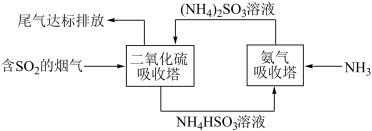
(1)写出氨吸收塔中主要发生的化学方程式_____ 。
(2)写出二氧化硫吸收塔中主要发生的离子方程式_____ 。
(3)当含SO2烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗_____ ?如可能,请写出至少一个氧化还原反应的化学方程式_____ 。
(4)上述流程可循环利用的物质是什么_____ ?
(5)在氨吸收塔中,反应所得到的高浓度溶液中,按一定比例再加入氨水,此时溶液的温度会自行降低,并析出晶体。
①导致溶液温度降低的原因可能是什么_____ ?
②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为134,计算其化学式_____ 。
③生产中得到的结晶水合物测定其相对分子质量往往会偏大,分析可能的原因_____ 。

(1)写出氨吸收塔中主要发生的化学方程式
(2)写出二氧化硫吸收塔中主要发生的离子方程式
(3)当含SO2烟气通入二氧化硫吸收塔中,可能发生氧化还原反应吗
(4)上述流程可循环利用的物质是什么
(5)在氨吸收塔中,反应所得到的高浓度溶液中,按一定比例再加入氨水,此时溶液的温度会自行降低,并析出晶体。
①导致溶液温度降低的原因可能是什么
②析出的晶体可用于造纸工业,也可用于照相用显影液的生产。已知该结晶水合物的相对分子质量为134,计算其化学式
③生产中得到的结晶水合物测定其相对分子质量往往会偏大,分析可能的原因
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】POCl3是重要的基础化工原料,广泛用于制药、染料、表面活性剂等行业。一种制备POCl3的原理为: PCl3+Cl2+SO2=POCl3+SOCl2。某化学学习小组拟利用如图装置在实验室模拟制备POCl3。

有关物质性质如下:
(1)装置C的作用是________ 。
(2)该装置有一处缺陷,解决的方法是在现有装置中再添加一个装置,该装置中应装入的试剂为____ (写名称)。若无该装置,则可能会有什么后果?请用化学方程式进行说明_______ 。
(3)D中反应温度控制在60~65℃,其原因是_______ 。
(4)测定POCl3含量。
①准确称取30.70g POCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00 mL 3.200 mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+为指示剂,用0.2000 mol/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mLKSCN溶液。
ⅰ滴定终点的现象为___________ 。
ⅱ 反应中POCl3的百分含量为__________ 。

有关物质性质如下:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g·mL-1 | 其它 |
| PCl3 | -93.6 | 76.1 | 1.574 | 遇水强烈水解,易与氧气反应 |
| POCl3 | 1.25 | 105.8 | 1.645 | 遇水强烈水解,能溶于PCl3 |
| SOCl2 | -105 | 78.8 | 1.638 | 遇水强烈水解,加热易分解 |
(2)该装置有一处缺陷,解决的方法是在现有装置中再添加一个装置,该装置中应装入的试剂为
(3)D中反应温度控制在60~65℃,其原因是
(4)测定POCl3含量。
①准确称取30.70g POCl3产品,置于盛有60.00mL蒸馏水的水解瓶中摇动至完全水解;
②将水解液配成100.00mL溶液,取10.00mL溶液于锥形瓶中;
③加入10.00 mL 3.200 mol/LAgNO3标准溶液,并加入少许硝基苯用力摇动,使沉淀表面被有机物覆盖;
④以Fe3+为指示剂,用0.2000 mol/L KSCN溶液滴定过量的AgNO3溶液,达到滴定终点时共用去10.00 mLKSCN溶液。
ⅰ滴定终点的现象为
ⅱ 反应中POCl3的百分含量为
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】Ⅰ.某小组同学对 与
与 的反应进行的探究如下图:
的反应进行的探究如下图:
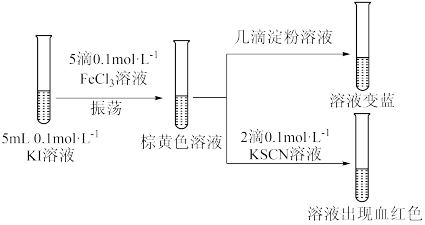
(1)写出KI溶液中滴入 溶液发生的离子反应方程式
溶液发生的离子反应方程式_______ 。
(2)实验证明 与
与 的反应为可逆反应,原因是
的反应为可逆反应,原因是_______ 。
Ⅱ.【深入探究】取1mL 溶液于试管中,向其中滴入5滴
溶液于试管中,向其中滴入5滴 碘水,充分振荡,完成下列实验:
碘水,充分振荡,完成下列实验:
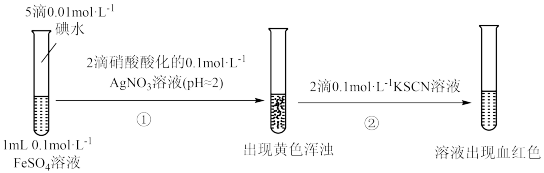
(3)实验①证明原混合液产生了_______ 。
(4)实验②证明溶液中有 ,对
,对 产生的原因做出如下假设:
产生的原因做出如下假设:
假设a:空气中存在 ,由于
,由于_______ (用离子方程式表示),可产生 ;
;
假设b:步骤①加入的 具有氧化性,可产生
具有氧化性,可产生 ;
;
假设c:原混合液中碘水可将 氧化为
氧化为 ;
;
假设d:_______ 。
(5)某同学在完成上述实验①时,不小心加了2mL 溶液,结果在溶液出现黄色浑浊几秒钟后,迅速出现大量灰黑色浑浊。为探究出现灰黑色浑浊的原因,设计并完成了实验③。
溶液,结果在溶液出现黄色浑浊几秒钟后,迅速出现大量灰黑色浑浊。为探究出现灰黑色浑浊的原因,设计并完成了实验③。
实验③:该同学向1mL 溶液中加入1mL
溶液中加入1mL 溶液,开始时,溶液无明显变化。几分钟后,出现大量灰黑色浑浊。测定溶液中
溶液,开始时,溶液无明显变化。几分钟后,出现大量灰黑色浑浊。测定溶液中 浓度随反应时间的变化如下图。
浓度随反应时间的变化如下图。
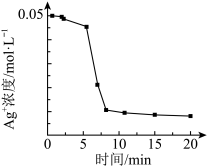
根据实验现象和 变化图像推测灰黑色浑浊可能是
变化图像推测灰黑色浑浊可能是_______ ,实验③产生灰黑色浑浊的原因是(用离子方程式表示)_______ 。
 与
与 的反应进行的探究如下图:
的反应进行的探究如下图:
(1)写出KI溶液中滴入
 溶液发生的离子反应方程式
溶液发生的离子反应方程式(2)实验证明
 与
与 的反应为可逆反应,原因是
的反应为可逆反应,原因是Ⅱ.【深入探究】取1mL
 溶液于试管中,向其中滴入5滴
溶液于试管中,向其中滴入5滴 碘水,充分振荡,完成下列实验:
碘水,充分振荡,完成下列实验:
(3)实验①证明原混合液产生了
(4)实验②证明溶液中有
 ,对
,对 产生的原因做出如下假设:
产生的原因做出如下假设:假设a:空气中存在
 ,由于
,由于 ;
;假设b:步骤①加入的
 具有氧化性,可产生
具有氧化性,可产生 ;
;假设c:原混合液中碘水可将
 氧化为
氧化为 ;
;假设d:
(5)某同学在完成上述实验①时,不小心加了2mL
 溶液,结果在溶液出现黄色浑浊几秒钟后,迅速出现大量灰黑色浑浊。为探究出现灰黑色浑浊的原因,设计并完成了实验③。
溶液,结果在溶液出现黄色浑浊几秒钟后,迅速出现大量灰黑色浑浊。为探究出现灰黑色浑浊的原因,设计并完成了实验③。实验③:该同学向1mL
 溶液中加入1mL
溶液中加入1mL 溶液,开始时,溶液无明显变化。几分钟后,出现大量灰黑色浑浊。测定溶液中
溶液,开始时,溶液无明显变化。几分钟后,出现大量灰黑色浑浊。测定溶液中 浓度随反应时间的变化如下图。
浓度随反应时间的变化如下图。
根据实验现象和
 变化图像推测灰黑色浑浊可能是
变化图像推测灰黑色浑浊可能是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐2】某校化学小组学生利用下图所示装置进行“乙二酸(俗名草酸)晶体受热分解”的实验,并验证分解产物中有CO2和CO(图中夹持装置已略去)。(已知草酸钙难溶于水,草酸沸点150℃)

(1)装置C的作用是_______ ,装置E的作用是 _______
(2)乙二酸受热分解的反应方程式是_______
(3)①证明分解产物中有CO2的现象是_______
②证明分解产物中有CO的现象是_______
(4)该装置有不足之处,请写出弥补不足之处的理由和具体方法:_______

(1)装置C的作用是
(2)乙二酸受热分解的反应方程式是
(3)①证明分解产物中有CO2的现象是
②证明分解产物中有CO的现象是
(4)该装置有不足之处,请写出弥补不足之处的理由和具体方法:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐3】某研究性学习小组设计了如图装置制取和验证SO2的性质。
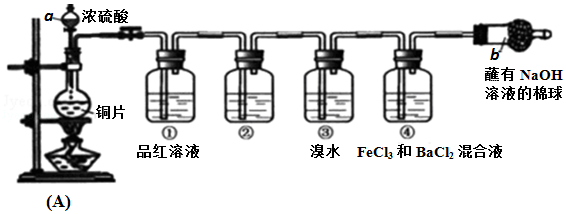
请回答:
(1)写出A反应装置中的化学方程式:____________
(2)棉球中NaOH溶液的作用是________________
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是_________ 。
A.澄清石灰水 B.无色酚酞试液 C.碘水 D.紫色石蕊试液
(4)下列说法正确的是____________ 。
A.先向装置中加入试剂(药品),再进行气密性检查
B.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)写出洗气瓶③中反应的化学方程式:_____________

请回答:
(1)写出A反应装置中的化学方程式:
(2)棉球中NaOH溶液的作用是
(3)为了验证SO2是酸性氧化物,洗气瓶②中可选择的试剂是
A.澄清石灰水 B.无色酚酞试液 C.碘水 D.紫色石蕊试液
(4)下列说法正确的是
A.先向装置中加入试剂(药品),再进行气密性检查
B.实验开始时,只需打开分液漏斗的旋塞,即可使液体顺利滴下
C.实验开始后,洗气瓶①和③中溶液均褪色,两者均可证明SO2具有漂白性
D.实验开始后,洗气瓶④中可观察到白色沉淀产生,该现象可说明SO2具有还原性
(5)写出洗气瓶③中反应的化学方程式:
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐1】“套管实验”是将一支较小的试管装入另一试管中,经组装来完成原来需要两只或更多试管进行的实验。因其有许多优点,近年来被广泛开发并应用于化学实验中。下面这个实验为“套管实验”,实验装置如下图,小试管中部有沾上无水硫酸铜粉末的脱脂棉。请观察实验装置,分析实验原理,并回答下列问题:

(1)整个实验过程中,能观察到的现象为
①烧杯A中________ ;②小试管中________ ;
③烧杯B中____________________________ ;
(2)实验结束时,在操作上要特别注意的问题是
____________________________________________________________________
(3)写出实验过程中发生反应的化学方程式____________________________

(1)整个实验过程中,能观察到的现象为
①烧杯A中
③烧杯B中
(2)实验结束时,在操作上要特别注意的问题是
(3)写出实验过程中发生反应的化学方程式
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐2】为了探究铁与水的反应,某同学设计并进行了下列实验,虚线框处用来检验生成的气体。

(1)A装置的作用是________________ ,B中反应的化学方程式为_________________ 。
(2)虚线框C处应该选择装置___________ (填甲或乙),实验现象是________________ 。
(3)球形干燥管的作用是_____________________________________________ 。
(4)A ,B两个装置中应先加热________ 装置。

(1)A装置的作用是
(2)虚线框C处应该选择装置
(3)球形干燥管的作用是
(4)A ,B两个装置中应先加热
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】下图为中学化学实验中的常见实验装置
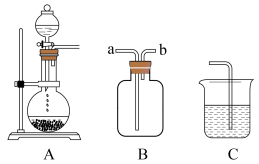
(1)装置A可用于制备多种气体,请写出用A装置制备下列气体时,圆底烧瓶和分液漏斗中应装的化学试剂
(2)装置B可用于收集多种气体,若要用于收集Cl2,则进气管为________ ;若要收集CO,简述用装置B收集CO的方法________________________________
(3)现要用上述装置制取Cl2,并设计实验比较Cl2和I2的氧化性强弱,请在表格内依次填上所需的装置和试剂(可不填满)

(1)装置A可用于制备多种气体,请写出用A装置制备下列气体时,圆底烧瓶和分液漏斗中应装的化学试剂
| 气体 | O2 | CO2 | HCl |
| 试剂 |
(3)现要用上述装置制取Cl2,并设计实验比较Cl2和I2的氧化性强弱,请在表格内依次填上所需的装置和试剂(可不填满)
| 装置 | 该装置中反应的离子方程式 |
您最近一年使用:0次



