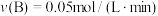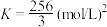在2 L密闭容器中将4 mol气体A和2 mol气体B混合,在一定温度下发生反应:3A(g)+2B(g) xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
 xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )
xC(g)+2D(g)。2 min后达到平衡时生成1.6 mol C,又测得反应速率v(D)=0.2 mol·L-1·min-1,下列说法正确的是( )| A.x=4 | B.B的转化率为60% |
| C.A的平衡浓度是2.8 mol·L-1 | D.平衡时气体的压强是原来的0.94倍 |
更新时间:2016-12-09 08:02:57
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】在恒温恒容的密闭容器中充入 和
和 ,发生反应
,发生反应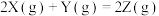 ,当反应进行到
,当反应进行到 时,测得
时,测得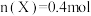 。则反应进行到
。则反应进行到 时,容器中Y的物质的量是
时,容器中Y的物质的量是
 和
和 ,发生反应
,发生反应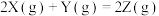 ,当反应进行到
,当反应进行到 时,测得
时,测得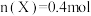 。则反应进行到
。则反应进行到 时,容器中Y的物质的量是
时,容器中Y的物质的量是A.小于 | B.大于 | C.等于 | D.无法确定 |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】下列说法中正确的是
| A.凡是放热反应都是自发的,吸热反应都是非自发的 |
B.在反应A(g)+3B(g)=2C(g)+2D(g)的速率测定实验中,分别 测得反应速率如下: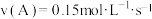 , , ,则用C来表示反应进行的速率更快。 ,则用C来表示反应进行的速率更快。 |
C.如图所示,在一U形管中装入含有紫色石蕊试液的Na2SO4溶液,通直流电,一段时间后U形管内会形成一个倒立的三色“彩虹”,从左到右颜色的次序是.红、紫、蓝 |
| D.反应HCl (aq)+ NaOH (aq) =" NaCl" (aq) + H2O (l) △H < 0,在理论上能用于设计原电池 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】硫酸的产量是衡量一个国家化工水平的标志。2SO2(g) + O2(g) 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
下列判断中,正确的是
 2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。
2SO3(g)是工业制硫酸的主要反应之一。一定温度下,在甲、乙、丙三个容积均为2 L的恒容密闭容器中投入SO2(g)和O2(g),其起始物质的量及SO2的平衡转化率如下表所示。| 甲 | 乙 | 丙 | ||
| 起始物质的量 | n(SO2) / mol | 0.4 | 0.4 | 0.8 |
| n(O2) / mol | 0.24 | 0.48 | 0.48 | |
| SO2的平衡转化率 | 80% | α1 | α2 | |
下列判断中,正确的是
| A.甲中反应的平衡常数大于乙 |
| B.平衡时,SO2的转化率:α1<80%<α2 |
| C.该温度下,乙中平衡常数值为400 |
| D.平衡时,丙中c(SO3)是甲中的2倍 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在密闭容器中发生 2CO(g)+SO2(g)  2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
 2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是| A.若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ |
| B.达到化学平衡后加入C18O,达新平衡前SO2中不含有18O |
| C.增大压强或升高温度都可以加快化学反应速率并能提高SO2的转化率 |
| D.达到化学平衡后,其它条件不变,容器体积缩小为原来的一半,CO的浓度增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】80℃时,NO2(g)+SO2(g) SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
SO3(g)+NO(g)。该温度下,在甲、乙、丙三个恒容密闭容器中,投入NO2和SO2,起始浓度如下表所示,其中甲经2min达平衡时,NO2的转化率为50%,下列判断不正确的是( )
| 起始浓度 | 甲 | 乙 | 丙 |
| c(NO2)/mol ·L-1 | 0.10 | 0.20 | 0.20 |
| c(SO2)/mol ·L-1 | 0.10 | 0.10 | 0.20 |
| A.平衡时,乙中SO2的转化率大于50% |
| B.当反应平衡时,丙中c(SO2)是甲中的2倍 |
| C.温度升至90℃,上述反应平衡常数为25/16,则正反应为吸热反应 |
| D.其他条件不变,若起始时向容器乙中充入0.10mol ·L-1 NO2和0.20 mol ·L-1 SO2,达到平衡时c(NO)与原平衡不同 |
您最近一年使用:0次

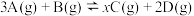 ,恒温条件下,向一个体积为2L的恒容密闭容器中通入等物质的量的A、B,经5min后反应达到平衡,测得D的物质的量为1mol,
,恒温条件下,向一个体积为2L的恒容密闭容器中通入等物质的量的A、B,经5min后反应达到平衡,测得D的物质的量为1mol,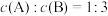 ,以C表示的平均反应速率
,以C表示的平均反应速率 ,下列说法
,下列说法