在密闭容器中发生 2CO(g)+SO2(g)  2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
 2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是| A.若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ |
| B.达到化学平衡后加入C18O,达新平衡前SO2中不含有18O |
| C.增大压强或升高温度都可以加快化学反应速率并能提高SO2的转化率 |
| D.达到化学平衡后,其它条件不变,容器体积缩小为原来的一半,CO的浓度增大 |
2017·湖南永州·一模 查看更多[3]
湖南省永州市2018届高三上学期第一次模拟考试化学试题河北省定州中学2018届高三上学期第二次月考化学试题2(已下线)第10单元 化学反应速率与化学平衡(B卷 滚动提升检测)-2021年高考化学一轮复习单元滚动双测卷
更新时间:2017-09-25 10:48:30
|
相似题推荐
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】下列实验操作正确且能达到实验目的的是
选项 | 实验操作 | 实验目的 |
A | 将 溶液置于蒸发皿中加热蒸干 溶液置于蒸发皿中加热蒸干 | 由 溶液制得 溶液制得 固体 固体 |
B | 取1mL KI溶液,加入5mL KI溶液,加入5mL 溶液,萃取分液后,向水层中滴入KSCN溶液 溶液,萃取分液后,向水层中滴入KSCN溶液 | 溶液变红色,说明 和 和 所发生的反应为可逆反应 所发生的反应为可逆反应 |
C | 用pH试纸测 溶液 溶液 , , 溶液 溶液 | 判断 和 和 酸性强弱 酸性强弱 |
D | 常温下测得 溶液的pH约为5 溶液的pH约为5 | 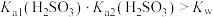 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列实验能达到预期目的是
| 实验内容 | 实验目的 | |
| A | 将0.2mol·L-1的KI溶液和0.05mol·L-1的FeCl3溶液等体积混合,充分反应后,取少许混合液滴加AgNO3溶液 | 验证Fe3+与I−的反应有一定限度 |
| B | 白铁皮(镀锌铁)出现刮痕后浸泡在饱和食盐水中,一段时间后滴入几滴K3[Fe(CN)6]溶液 | 验证该过程是否发生原电池反应 |
| C | 相同条件下,向一支试管中加入2mL5%H2O2和1mLH2O,向另一支试管中加入2mL5%H2O2和1mLFeCl3溶液,观察并比较实验现象 | 探究FeCl3对H2O2分解速率的影响 |
| D | 向2支盛有5mL不同浓度NaHSO3溶液的试管中,同时加入2mL5%H2O2溶液,观察并比较实验现象 | 探究浓度对反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列实验操作能达到实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将海带灰溶于水,过滤,向滤液中滴加淀粉溶液 | 检测海带中含有碘元素 |
| B | 将SO2通入滴有酚酞的NaOH溶液中,溶液红色褪去 | 证明SO2的漂白性 |
| C | 取5mL0.1mol•L-1KI溶液,滴加0.1mol•L-1FeCl3溶液3mL,充分反应,根据溶液中既含I2,又含I-的实验事实,判断该反应是可逆反应 | 探究化学反应的限度 |
| D | 向硅酸钠溶液中通入CO2气体,有白色沉淀产生 | 验证H2CO3的酸性强于H2SiO3 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某可逆反应平衡常数表达式为K=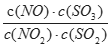 达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
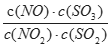 达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是
达到平衡状态时,如果升高温度(其它条件不变),则c(NO)减小.下列说法正确的是A.反应的热化学方程式为NO2(g)+SO2(g)  NO(g)(g)+SO3(g) △H>0 NO(g)(g)+SO3(g) △H>0 |
| B.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深 |
| C.混合气体的平均摩尔质量保持不变,说明反应已达平衡 |
| D.使用合适的催化剂可使该反应的反应速率和平衡常数增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】以下情况中,可以证明可逆反应达到平衡状态的有个
Ⅰ.
①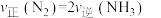 ②1个
②1个 键断裂的同时,有6个
键断裂的同时,有6个 键断裂
键断裂
Ⅱ.
③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.
⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.
⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时, 的体积分数不再改变
的体积分数不再改变
Ⅴ.
⑨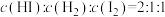
⑩恒容绝热时,压强不再改变
⑪恒容绝热时,平衡常数不再改变
Ⅰ.

①
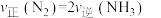 ②1个
②1个 键断裂的同时,有6个
键断裂的同时,有6个 键断裂
键断裂Ⅱ.

③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.

⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.

⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时,
 的体积分数不再改变
的体积分数不再改变Ⅴ.

⑨
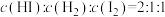
⑩恒容绝热时,压强不再改变
⑪恒容绝热时,平衡常数不再改变
| A.6 | B.7 | C.8 | D.9 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐1】体积相同的甲、乙两个容器中分别充入等物质的量的SO2和O2,在相同温度下发生反应:2SO2(g)+O2(g) 2SO3(g),并达到化学平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3(g),并达到化学平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
 2SO3(g),并达到化学平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率
2SO3(g),并达到化学平衡。在这个过程中,甲容器保持体积不变,乙容器保持压强不变,若甲容器中SO2的转化率为p%,则乙容器中SO2的转化率| A.等于p% | B.大于p% | C.小于p% | D.无法判断 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列事实不能用平衡移动原理解释的是
| A.由H2、I2(g)、HI组成的恒压平衡体系,加入氦气后颜色变浅 |
| B.农村盐碱地(主要含Na2CO3等)加入石膏可降低土壤碱性 |
| C.蒸馏水和0.1 mol·L-1 NaOH溶液中的c(OH-),前者大于后者 |
| D.向含有少量Fe3+的MgCl2酸性溶液中加MgCO3,可将Fe3+转化成Fe(OH)3除去 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】下列方案设计、现象和结论都正确的是
目的 | 方案设计 | 现象和结论 | |
A | 比较金属活泼性 | Mg、Al、NaOH溶液构成原电池装置 | 若Mg片上冒气泡,证明活泼性:Al>Mg |
B | 探究压强对平衡移动的影响 | 用针筒吸入NO2与N2O4的混合气体,将细管端用橡胶塞封闭,然后将活塞向内推,观察颜色变化 | 若颜色先变深后又逐渐变浅,证明压强增大,平衡朝气体分子数减小的方向移动 |
C | 探究反应的可逆性 | 往Fe2(SO4)3溶液中滴加KSCN溶液,再加入少量K2SO4固体 | 若溶液先变成血红色,后无明显变化,说明Fe3+与SCN-的反应不可逆 |
D | 用牺牲阳极法保护铁钉并检验其效果 | 以铁钉和锌棒作电极,酸化的3% NaCl溶液作电解质溶液,接通电源,过一段时间,取铁电极区域溶液于试管中,滴入K3[Fe(CN)6]溶液,观察现象 | 若未出现特征蓝色沉淀,证明铁钉未被腐蚀 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】在两个固定体积均为 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率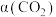 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是
 密闭容器中以不同的氢碳比
密闭容器中以不同的氢碳比 充入
充入 和
和 ,在一定条件下发生反应:
,在一定条件下发生反应: ,
, 的平衡转化率
的平衡转化率 与温度的关系如图所示。下列说法正确的是
与温度的关系如图所示。下列说法正确的是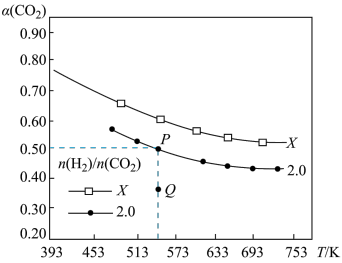
| A.该反应在常温下不可能自发进行 |
B.X的氢碳比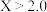 ,在氢碳比为2.0时Q点 ,在氢碳比为2.0时Q点 点 点 |
C.向处于P点状态的容器中,按2∶4∶1∶4的比例再充入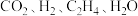 ,再次平衡后 ,再次平衡后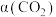 减小 减小 |
D.若起始时 、 、 浓度分别为 浓度分别为 、 、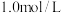 ,则可得P点对应温度的平衡常数的值为512 ,则可得P点对应温度的平衡常数的值为512 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】一定量的混合气体在密闭容器中发生反应 mA(g)+nB(g) pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
 pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是
pC(g)达到平衡后,温度不变,将气体体积缩小到原来的1/3,达到平衡时,C的浓度为原来的2.5倍,则下列说法正确的是| A.C的体积分数增加 | B.A的转化率降低 |
| C.平衡向正反应方向移动 | D.m+n>p |
您最近一年使用:0次
【推荐3】一定温度下,在三个容积均为1.0L的恒容密闭容器中发生反应:CH3OH(g)+CO(g) CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是
 CH3COOH(g) △H< 0。下列说法不正确的是
CH3COOH(g) △H< 0。下列说法不正确的是| 容器编号 | 温度(K) | 起始物质的量(mol) | 平衡时CH3COOH的物质的量(mol) | 平衡常数 | ||
| n(CH3OH) | n (CO) | n (CH3COOH) | ||||
| Ⅰ | 530 | 0.05 | 0.05 | 0 | 0.025 | K1 |
| Ⅱ | 530 | 0.03 | 0.03 | 0.006 | K2 | |
| Ⅲ | 510 | 0 | 0 | 0.05 | K3 | |
| A.达平衡时,容器Ⅰ中平衡常数K1 =40 |
| B.达平衡时,容器Ⅲ中的正反应速率比容器Ⅰ中的小 |
| C.达平街时,容器Ⅰ中CH3OH转化率与容器Ⅲ中CH3COOH转化率之和小于1 |
| D.K1>K2>K3 |
您最近一年使用:0次

 C(g)+D(g),已达到平衡状态的是(
C(g)+D(g),已达到平衡状态的是(

