以下情况中,可以证明可逆反应达到平衡状态的有个
Ⅰ.
①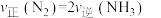 ②1个
②1个 键断裂的同时,有6个
键断裂的同时,有6个 键断裂
键断裂
Ⅱ.
③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.
⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.
⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时, 的体积分数不再改变
的体积分数不再改变
Ⅴ.
⑨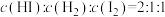
⑩恒容绝热时,压强不再改变
⑪恒容绝热时,平衡常数不再改变
Ⅰ.

①
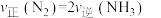 ②1个
②1个 键断裂的同时,有6个
键断裂的同时,有6个 键断裂
键断裂Ⅱ.

③恒温恒容时,气体的压强不再改变
④恒温恒压时,气体的密度不再改变
Ⅲ.

⑤恒温恒容时,气体的密度不再改变
⑥恒温恒容时,气体的平均相对分子质量不再改变
Ⅳ.

⑦恒温恒容时,气体的平均相对分子质量不再改变
⑧恒温恒压时,
 的体积分数不再改变
的体积分数不再改变Ⅴ.

⑨
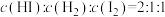
⑩恒容绝热时,压强不再改变
⑪恒容绝热时,平衡常数不再改变
| A.6 | B.7 | C.8 | D.9 |
更新时间:2022-11-17 11:31:14
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】在密闭容器中发生 2CO(g)+SO2(g)  2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
 2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是
2CO2(g)+S(s) △H=-akJ·mol-1(a>0)的反应,下列叙述正确的是| A.若反应开始时投入2 mol CO,则达平衡时,放出热量为a kJ |
| B.达到化学平衡后加入C18O,达新平衡前SO2中不含有18O |
| C.增大压强或升高温度都可以加快化学反应速率并能提高SO2的转化率 |
| D.达到化学平衡后,其它条件不变,容器体积缩小为原来的一半,CO的浓度增大 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】下列说法正确的是
| A.常温下,物质的量浓度均为0.1 mol·L-1 Na2CO3和 NaHCO3的等体积混合溶液中: 2c(OH-)-2c(H+)=3c(H2CO3)+c(HCO3-)-c(CO32-) |
| B.△H<0,△S>0的反应都是自发反应,△H>0,△S>0的反应任何条件都是非自发反应 |
C.已知:P4(g)+6Cl2(g)=4PCl3(g)△H= akJ·mol-1 P4(g)+10Cl2(g)=4PCl5(g) △H=bkJ·mol-1 P4具有正四面体结构,PCl5中P-Cl键的键能为 ckJ·mol-1,PCl3中P-Cl键的键能为1.2c kJ·mol-1,由此计算Cl-Cl键的键能 kJ·mol-1 kJ·mol-1 |
| D.在一定温度下,固定体积为2L密闭容器中,发生反应:2SO2(g)+O2(g)=2SO3(g) △H<0,当v(SO2)=v(SO3)时,说明该反应已达到平衡状态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据见表。下列说法错误的是
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据见表。下列说法错误的是
 2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据见表。下列说法错误的是
2NH3(g)+CO2(g)。实验测得不同温度下的平衡数据见表。下列说法错误的是| 温度/℃ | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强/kPa | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度/10-3mol/L | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
| A.该分解反应为吸热反应 |
| B.当混合气体平均相对分子质量为26时,该反应已达平衡状态 |
| C.根据表中数据,计算25.0℃时反应的平衡常数约为1.6×10-8mol3/L3 |
| D.若保持温度和体积不变,平衡后再充入n(NH3):n(CO2)=2:1,再次达到平衡时c(NH3)不变 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】在恒容密闭容器中进行可逆反应:2NO2(g) 2NO(g)+O2(g),下列不能说明该反应已达到平衡状态的是
2NO(g)+O2(g),下列不能说明该反应已达到平衡状态的是
 2NO(g)+O2(g),下列不能说明该反应已达到平衡状态的是
2NO(g)+O2(g),下列不能说明该反应已达到平衡状态的是| A.混合气体的颜色不再改变 | B.混合气体的密度不再改变 |
| C.混合气体的压强不再改变 | D.混合气体的平均摩尔质量不再改变 |
您最近一年使用:0次




