现有稀硫酸和稀硝酸的混合溶液,已知其中稀硫酸的浓度为4mol/L,稀硝酸的浓度为2 mol/L。取10mL混合酸,向其中加入过量铁粉,反应结束后,在标准状况下可收集到的气体成分为_______ 、_______ ;体积分别是_______ L、_______ L。(假设HNO3只被还原为NO)
更新时间:2016-12-09 08:08:08
|
相似题推荐
计算题
|
适中
(0.65)
名校
解题方法
【推荐1】将32.64g铜粉与140 mL 一定量浓硝酸恰好完全反应,铜完全溶解,反应后收集到的气体在标准状况下的体积为11.2 L。(反应中只产生NO或NO2 )请回答:
(1)NO的物质的量为___________ mol
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为_____________ 。
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是___ g
(1)NO的物质的量为
(2)待产生的气体全部释放后,向溶液中加入v mL a mol/L的 NaOH 溶液,恰好使溶液中的 Cu2+ 全部沉淀,则原硝酸的浓度为
(3)欲使铜与硝酸反应生成的气体在溶液中完全转化为NaNO3,至少需要加入30%的双氧水的质量是
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】4.35 g二氧化锰能与浓盐酸(密度为1.19 g·cm-3、质量分数为36.5%)完全反应。求:
(1)盐酸中HCl的物质的量浓度。_______
(2)被氧化的HCl的物质的量。_______
(3)将所得气体全部用石灰乳吸收,可得到漂白粉的质量。___________
(1)盐酸中HCl的物质的量浓度。
(2)被氧化的HCl的物质的量。
(3)将所得气体全部用石灰乳吸收,可得到漂白粉的质量。
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】10gFe-Mg合金溶解在一定量的某浓度的稀硝酸中,当金属完全反应后,收集到标况下4.48LNO气体(设还原产物只有NO,铁只生成Fe2+)。
(1)反应中被还原的硝酸物质的量是多少
(2)在反应后的溶液中加入足量的NaOH溶液,可得多少克沉淀?
(1)反应中被还原的硝酸物质的量是多少
(2)在反应后的溶液中加入足量的NaOH溶液,可得多少克沉淀?
您最近一年使用:0次
计算题
|
适中
(0.65)
解题方法
【推荐2】将32g铜与100mL一定浓度的硝酸反应,铜完全溶解,产生的NO和NO2混合气体在标准状况下的体积为11.2L。
请回答:
(1)NO气体与NO2气体体积比为___ 。
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为__ mol/L(用V和a表示)。
请回答:
(1)NO气体与NO2气体体积比为
(2)将产生的气体全部逸出后向溶液中加入VmLamol/LNaOH溶液,恰好使溶液中的铜离子全部转化为沉淀,则原硝酸溶液的浓度为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐3】取m克铁粉与1 L 1.2 mol/L的稀HNO3恰好完全反应,反应后的溶液中只含Fe2+且硝酸的还原产物只有NO。则:
(1)m=______________ g。
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是_________ 。
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为______ L。
(1)m=
(2)若将反应后的溶液低温蒸干,析出晶体135 g,则析出晶体的组成可能是
a.Fe(NO3)2∙7H2O和Fe(NO3)2∙4H2O
b.Fe(NO3)2∙7H2O和Fe(NO3)2∙H2O
c.Fe(NO3)2∙4H2O和Fe(NO3)2∙H2O
(3)若向反应后的溶液中加入100 mL 1.5 mol/L的稀H2SO4,则标准状态下还能产生NO的体积为
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐1】硝酸发生氧化还原反应的时候,一般硝酸浓度越稀,对应还原产物中氮的化合价越低。若硝酸现有一定量的铝粉和铁粉的混合物与一定量很稀的HNO3充分反应,反应过程中无任何气体放出。在反应结束后的溶液中,逐滴加入4mol /LNaOH溶液,所加NaOH溶液的体积(mL)与产生沉淀的物质的量(mol)关系如图所示。求:
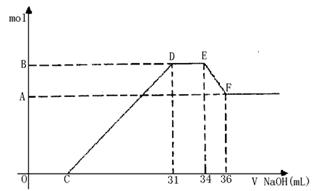
(1)B与A的差值: mol;
(2)B的数值: mol;
(3)C的数值: mL。(要求有计算过程)

(1)B与A的差值: mol;
(2)B的数值: mol;
(3)C的数值: mL。(要求有计算过程)
您最近一年使用:0次
计算题
|
适中
(0.65)
【推荐2】印刷电路板是由高分子材料和铜箔复合而成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,生成CuCl2和FeCl2。现有一包铁粉和铜粉的混合粉末17.6 g,使其完全溶解恰好需要200 mL 3.0 mol/L的FeCl3溶液。假设溶液反应前后体积不变,试计算:
(注意:无计算过程不给分)
(1)混合粉末中铜的质量;
(2)反应后溶液中FeCl2的物质的量浓度;
(3)常温下,该混合粉末与足量浓硝酸反应,最多可生成气体的体积。(25℃、101 kPa时,该气体的摩尔体积为24.5 L/mol)
(注意:无计算过程不给分)
(1)混合粉末中铜的质量;
(2)反应后溶液中FeCl2的物质的量浓度;
(3)常温下,该混合粉末与足量浓硝酸反应,最多可生成气体的体积。(25℃、101 kPa时,该气体的摩尔体积为24.5 L/mol)
您最近一年使用:0次
【推荐3】硝酸铜是重要的化工原料,以下三种方法均可得到硝酸铜。
已知:2NO2+2NaOH=NaNO3+ NaNO2+H2O ,NO+NO2+2NaOH=2NaNO2+H2O(以下涉及到的气体体积均为标准状况下数据):
(1)甲组用a克Cu粉,在加热的条件下,与空气充分反应,然后将生成的CuO全部溶于VmL稀硝酸中,制得硝酸铜溶液,则所需稀硝酸的浓度至少为_______ mol/L,需要质量分数为ω%,密度为ρg/cm3的浓硝酸_______ mL(均用最简分式表示)。
(2)乙组用b克Cu粉,全部溶于过量的稀硝酸中,溶液质量增重_____ 克,将生成的气体通入足量NaOH溶液中并同时通入氧气的体积至少_______ L才能使生成的气体吸收完全(均用最简分式表示)。
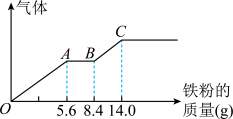
(3)丙组取某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。列式计算原混合酸中硝酸的物质的量是多少?____________ 硫酸的物质的量浓度多少?_________
已知:2NO2+2NaOH=NaNO3+ NaNO2+H2O ,NO+NO2+2NaOH=2NaNO2+H2O(以下涉及到的气体体积均为标准状况下数据):
(1)甲组用a克Cu粉,在加热的条件下,与空气充分反应,然后将生成的CuO全部溶于VmL稀硝酸中,制得硝酸铜溶液,则所需稀硝酸的浓度至少为
(2)乙组用b克Cu粉,全部溶于过量的稀硝酸中,溶液质量增重
(3)丙组取某稀硫酸和稀硝酸的混合溶液200 mL,平均分成两份。向其中一份中逐渐加入铜粉,最多能溶解9.6 g。向另一份中逐渐加入铁粉,产生气体的量随铁粉质量增加的变化如图所示(已知硝酸只被还原为NO气体)。列式计算原混合酸中硝酸的物质的量是多少?

您最近一年使用:0次



