50 mL 0.50 mol·L-1盐酸与50 mL 0.55 mol·L-1NaOH溶液在图示的装置中进行中和反应。通过测定反应过程中所放出的热量可计算中和热。回答下列问题:
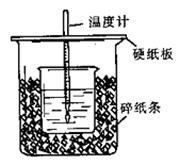
(1)从实验装置上看,图中尚缺少的一种玻璃用品是_____________ 。
(2)烧杯间填满碎纸条的作用是___________________ 。
(3)大烧杯上如不盖硬纸板,求得的中和热数值_________ (填“偏大”“偏小”“无影响”)。
(4)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量_____ (填“相等”“不相等”),所求中和热 _____ (填“相等”“不相等”)
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会_____ ;用50 mL 0.50 mol·L-1NaOH溶液进行上述实验,测得的中和热的数值会 __________ (均填“偏大”“偏小”“无影响”) 。
(6)写出NaOH溶液和盐酸反应表示中和热的热化学方程式__________ 。

(1)从实验装置上看,图中尚缺少的一种玻璃用品是
(2)烧杯间填满碎纸条的作用是
(3)大烧杯上如不盖硬纸板,求得的中和热数值
(4)实验中改用60 mL 0.50 mol·L-1盐酸跟50 mL 0.55 mol·L-1NaOH溶液进行反应,与上述实验相比,所放出的热量
(5)用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得的中和热的数值会
(6)写出NaOH溶液和盐酸反应表示中和热的热化学方程式
更新时间:2019-01-30 18:14:09
|
相似题推荐
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐1】经检测某工厂的酸性废水中所含离子及其浓度如下表所示:
(1)c(H+)=________ mol/L。
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O).
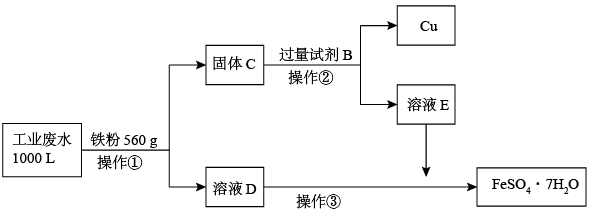
① 工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+ =Fe2++Cu、________________ 、_________________ 。
②试剂B是__________ 。
③ 操作③是_____________ 、_____________ 、过滤,最后用少量冷水洗涤晶体,在低温下干燥。
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是__________________ 。
⑤ 获得的FeSO4·7H2O需密闭保存,原因是___________________________ 。若将所得FeSO4·7H2O配成溶液,向溶液中滴加NaOH溶液的现象是_________________________________________________________________ 。
⑥上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是_________ mol。
| 离子 | Fe3+ | Cu2+ | SO42- | Na+ | H+ |
| 浓度/(mol/L) | 2×10-3 | 1×10-3 | 1×10-2 | 2×10-3 |
(1)c(H+)=
(2)为了减少污染并变废为宝,工程师们设计了如下流程,回收铜和绿矾(FeSO4·7H2O).

① 工业废水中加入铁粉后,反应的离子方程式为:Fe+Cu2+ =Fe2++Cu、
②试剂B是
③ 操作③是
④通过检验溶液D中Fe3+来判断废水中Fe3+是否除尽,实验方法是
⑤ 获得的FeSO4·7H2O需密闭保存,原因是
⑥上述1000 L废水经处理,可获得 FeSO4·7H2O的物质的量是
您最近一年使用:0次
解答题-工业流程题
|
较难
(0.4)
解题方法
【推荐2】锌是一种应用广泛的金属,目前工业上主要采用“湿法”工艺冶炼锌,以某硫化锌精矿(主要成分是ZnS,还含有少量FeS等其他成分)为原料冶炼锌的工艺流程如图所示:
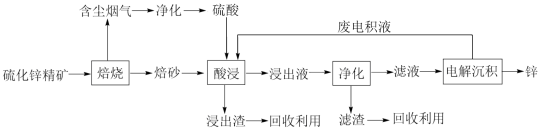
回答下列问题:
(1)“焙烧”过程在氧气气氛的沸腾炉中进行,“焙砂”中铁元素主要以Fe3O4形式存在,写出“焙烧”过程中FeS主要发生反应的化学方程式:_______ ;“含尘烟气”中的SO2可用氨水吸收,经循环利用后制取硫酸,用氨水吸收SO2至溶液的pH=5时,所得溶液中的 =
=_______ 。[已知:Ka1(H2SO3)=l。4×10-2;Ka2(H2SO3)=6.0×10-8]
(2)浸出液“净化”过程中加入的主要物质为锌粉,所得“滤渣”的成分为_______ (填化学式),分离“滤液”'“滤渣”的操作名称为_______ 。
(3)在该流程中可循环使用的物质是Zn和_______ (填化学式)。
(4)改进的锌冶炼工艺,采用了“氧压酸(稀硫酸)浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。
①下列设想的加快浸取反应速率的措施中不合理的是_______ (填标号)。
A.将稀硫酸更换为98%的浓硫酸
B.将硫化锌精矿粉碎
C.适当升高温度
②硫化锌精矿的主要成分ZnS遇到硫酸铜溶液可慢慢地转化为铜蓝(CuS):ZnS(s)+Cu2+(aq) CuS(s)+Zn2+(aq),该反应的平衡常数K=
CuS(s)+Zn2+(aq),该反应的平衡常数K=_______ 。[已知:Ksp(ZnS)=1.6×10-24,Ksp(CuS)=6.4×10-36]
(5)金属锌化学性质活泼,可用于多种化学电源的电极材料。一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收了ZnSO4溶液的有机高聚物为固态电解质,电池总反应为MnO2+ Zn+(1+
Zn+(1+ )H2O+
)H2O+ ZnSO4
ZnSO4 MnOOH+
MnOOH+ [ZnSO4·3Zn(OH)2·xH2O]。放电时正极的电极反应式为
[ZnSO4·3Zn(OH)2·xH2O]。放电时正极的电极反应式为_______ 。

回答下列问题:
(1)“焙烧”过程在氧气气氛的沸腾炉中进行,“焙砂”中铁元素主要以Fe3O4形式存在,写出“焙烧”过程中FeS主要发生反应的化学方程式:
 =
=(2)浸出液“净化”过程中加入的主要物质为锌粉,所得“滤渣”的成分为
(3)在该流程中可循环使用的物质是Zn和
(4)改进的锌冶炼工艺,采用了“氧压酸(稀硫酸)浸”的全湿法流程,既省略了易导致空气污染的焙烧过程,又可获得一种有工业价值的非金属单质。
①下列设想的加快浸取反应速率的措施中不合理的是
A.将稀硫酸更换为98%的浓硫酸
B.将硫化锌精矿粉碎
C.适当升高温度
②硫化锌精矿的主要成分ZnS遇到硫酸铜溶液可慢慢地转化为铜蓝(CuS):ZnS(s)+Cu2+(aq)
 CuS(s)+Zn2+(aq),该反应的平衡常数K=
CuS(s)+Zn2+(aq),该反应的平衡常数K=(5)金属锌化学性质活泼,可用于多种化学电源的电极材料。一种3D打印机的柔性电池以碳纳米管作电极材料,以吸收了ZnSO4溶液的有机高聚物为固态电解质,电池总反应为MnO2+
 Zn+(1+
Zn+(1+ )H2O+
)H2O+ ZnSO4
ZnSO4 MnOOH+
MnOOH+ [ZnSO4·3Zn(OH)2·xH2O]。放电时正极的电极反应式为
[ZnSO4·3Zn(OH)2·xH2O]。放电时正极的电极反应式为
您最近一年使用:0次
解答题-实验探究题
|
较难
(0.4)
【推荐3】三氯化氧磷( )是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料,一研究小组在实验室模拟反应
)是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料,一研究小组在实验室模拟反应 制备
制备 并测定产品含量。
并测定产品含量。

资料卡片:
(1)若选用 固体与70%浓
固体与70%浓 制取
制取 ,反应的化学方程式是
,反应的化学方程式是________________ 。
(2)反应装置图的虚框中未画出的仪器最好选择___________ (填“己”或“庚”);溶液A饱和食盐水乙装置中应该盛装的试剂为___________ (填“ ”或“碱石灰”或“浓
”或“碱石灰”或“浓 ”或“无水硫酸铜”)。
”或“无水硫酸铜”)。
(3)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是__________________________ 。
(4)甲、丁装置的作用除了用于气体的净化除杂外,还有________________ 。
(5)通过佛尔哈德法可测定经过提纯后的产品中 的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000
的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000 的
的 溶液20.00mL(
溶液20.00mL(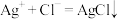 ),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖加入
),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖加入 作指示剂,用0.1000
作指示剂,用0.1000 KSCN标准溶液滴定过量的
KSCN标准溶液滴定过量的 至终点(
至终点( ),做平行实验,平均消耗KSCN标准溶液10.00mL。
),做平行实验,平均消耗KSCN标准溶液10.00mL。
①达到滴定终点的现象是__________________ 。
② 的质量分数为
的质量分数为___________ (保留一位小数)。
 )是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料,一研究小组在实验室模拟反应
)是一种重要的化工原料,常用作半导体掺杂剂及光导纤维原料,一研究小组在实验室模拟反应 制备
制备 并测定产品含量。
并测定产品含量。
资料卡片:
物质 | 熔点/℃ | 沸点/℃ | 相对分子质量 | 其他 |
| -93.6 | 76.1 | 137.5 | 遇水剧烈水解,易与 |
| 1.25 | 105.8 | 153.5 | 遇水剧烈水解,能溶于 |
| -105 | 78.8 | 119 | 遇水剧烈水解,受热易分解 |
(1)若选用
 固体与70%浓
固体与70%浓 制取
制取 ,反应的化学方程式是
,反应的化学方程式是(2)反应装置图的虚框中未画出的仪器最好选择
 ”或“碱石灰”或“浓
”或“碱石灰”或“浓 ”或“无水硫酸铜”)。
”或“无水硫酸铜”)。(3)水浴加热三颈烧瓶,控制反应温度在60~65℃,其原因是
(4)甲、丁装置的作用除了用于气体的净化除杂外,还有
(5)通过佛尔哈德法可测定经过提纯后的产品中
 的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000
的含量:准确称取1.600g样品在水解瓶中摇动至完全水解,将水解液配成100mL溶液,取10.00mL于锥形瓶中,加入0.2000 的
的 溶液20.00mL(
溶液20.00mL(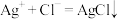 ),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖加入
),再加少许硝基苯,用力振荡,使沉淀被有机物覆盖加入 作指示剂,用0.1000
作指示剂,用0.1000 KSCN标准溶液滴定过量的
KSCN标准溶液滴定过量的 至终点(
至终点( ),做平行实验,平均消耗KSCN标准溶液10.00mL。
),做平行实验,平均消耗KSCN标准溶液10.00mL。①达到滴定终点的现象是
②
 的质量分数为
的质量分数为
您最近一年使用:0次
【推荐1】有效去除大气中的SO2、H2S以及废水中的硫化物是环境保护的重要课题。
(1)在一定条件下,CO可以去除烟气中的SO2,其反应过程分三步完成(Cat表示催化剂,[]表示空穴):
i.Cat[ ]+SO2=Cat[O]+SO
ii.Cat[ ]+SO=Cat[O]+S
iii.……
①写出第iii步反应方程式:______ 。
②在500℃条件下(硫的沸点445℃),将0.05mol混合气体(CO体积分数0.1%,SO2体积分数为0.05%,其余为N2)通入1L刚性容器中,在催化剂作用下发生反应,100min时测得CO体积分数0.01%。
i.100min时SO2去除率为______ 。
ii.0~100min内CO平均反应速率v(CO)=______ 。
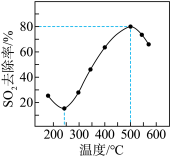
③已知脱硫总反应的△H>0,其他条件相同时,以γ-Al2O3作为催化剂,反应相同的时间,SO2的去除率随反应温度的变化如图所示,当温度高于500℃,SO2去除率降低的原因是_____ 。
(2)工业上可用克劳斯法处理H2S废气,其脱硫原理的反应分两步进行,其过程与能量变化如图所示。

①克劳斯法脱硫的总反应的热化学方程式为_____ 。
②在一定温度、285kPa反应条件下,将n(H2S):n(O2)=2:1混合气进行下列反应:
I.2H2S(g)+3O2(g) 2SO2(g)+2H2O(g)
2SO2(g)+2H2O(g)
II.2SO2(g)+4H2S(g) 3S2(g)+4H2O(g)
3S2(g)+4H2O(g)
测得平衡时混合气体中S2与SO2的分压相等,且H2S平衡转化率为45%,此时p(S2)=_____ ;反应I的平衡常数Kp=______ (列出数字运算表达式即可)。
(1)在一定条件下,CO可以去除烟气中的SO2,其反应过程分三步完成(Cat表示催化剂,[]表示空穴):
i.Cat[ ]+SO2=Cat[O]+SO
ii.Cat[ ]+SO=Cat[O]+S
iii.……
①写出第iii步反应方程式:
②在500℃条件下(硫的沸点445℃),将0.05mol混合气体(CO体积分数0.1%,SO2体积分数为0.05%,其余为N2)通入1L刚性容器中,在催化剂作用下发生反应,100min时测得CO体积分数0.01%。
i.100min时SO2去除率为
ii.0~100min内CO平均反应速率v(CO)=
③已知脱硫总反应的△H>0,其他条件相同时,以γ-Al2O3作为催化剂,反应相同的时间,SO2的去除率随反应温度的变化如图所示,当温度高于500℃,SO2去除率降低的原因是

(2)工业上可用克劳斯法处理H2S废气,其脱硫原理的反应分两步进行,其过程与能量变化如图所示。

①克劳斯法脱硫的总反应的热化学方程式为
②在一定温度、285kPa反应条件下,将n(H2S):n(O2)=2:1混合气进行下列反应:
I.2H2S(g)+3O2(g)
 2SO2(g)+2H2O(g)
2SO2(g)+2H2O(g)II.2SO2(g)+4H2S(g)
 3S2(g)+4H2O(g)
3S2(g)+4H2O(g) 测得平衡时混合气体中S2与SO2的分压相等,且H2S平衡转化率为45%,此时p(S2)=
您最近一年使用:0次
【推荐2】近年来,改善环境是科学研究的重要课题,对实现碳循环及废气资源的再利用技术的发展都具有重要意义。
(1)以 、
、 为原料合成
为原料合成 涉及的主要反应如下
涉及的主要反应如下
I.
II.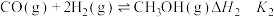
III.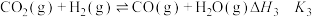
则
___________ (用含 、
、 的代数式表示),
的代数式表示),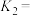
___________ (用含 、
、 的代数式表示)。
的代数式表示)。
(2)一定条件下, 和
和 发生反应:
发生反应: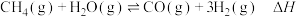 ,设起始
,设起始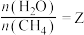 ,在恒压下,反应达到平衡时
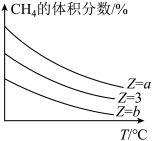
,在恒压下,反应达到平衡时 的体积分数与
的体积分数与 和
和 (温度)的关系如图所示。下列说法正确的是___________(填标号)。
(温度)的关系如图所示。下列说法正确的是___________(填标号)。
(3)在 时,往
时,往 的某恒容密闭容器中充入
的某恒容密闭容器中充入 和
和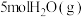 ,发生反应
,发生反应 ,5min后该反应达到平衡,此时测得混合气体的总物质的量为起始总物质的量的1.5倍,则:
,5min后该反应达到平衡,此时测得混合气体的总物质的量为起始总物质的量的1.5倍,则:
① 内,
内,
___________  ,
, 的平衡转化率为
的平衡转化率为___________ %。
②该反应的平衡常数
___________  。
。
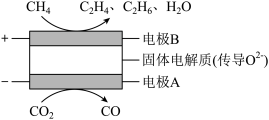
(4) 和
和 都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。请写出电极A的电极反应式:
都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。请写出电极A的电极反应式:___________ 。
(1)以
 、
、 为原料合成
为原料合成 涉及的主要反应如下
涉及的主要反应如下I.

II.
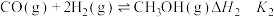
III.
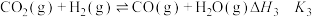
则

 、
、 的代数式表示),
的代数式表示),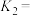
 、
、 的代数式表示)。
的代数式表示)。(2)一定条件下,
 和
和 发生反应:
发生反应: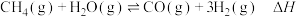 ,设起始
,设起始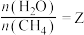 ,在恒压下,反应达到平衡时
,在恒压下,反应达到平衡时 的体积分数与
的体积分数与 和
和 (温度)的关系如图所示。下列说法正确的是___________(填标号)。
(温度)的关系如图所示。下列说法正确的是___________(填标号)。
| A.若氢气的物质的量分数不再随时间而改变,则该反应达到平衡 |
B.加入合适的催化剂,该反应的平衡转化率和 的值均增大 的值均增大 |
| C.当混合气体的平均相对分子质量不再随时间而改变时,该反应达到平衡 |
D.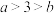 |
 时,往
时,往 的某恒容密闭容器中充入
的某恒容密闭容器中充入 和
和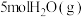 ,发生反应
,发生反应 ,5min后该反应达到平衡,此时测得混合气体的总物质的量为起始总物质的量的1.5倍,则:
,5min后该反应达到平衡,此时测得混合气体的总物质的量为起始总物质的量的1.5倍,则:①
 内,
内,
 ,
, 的平衡转化率为
的平衡转化率为②该反应的平衡常数

 。
。(4)
 和
和 都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。请写出电极A的电极反应式:
都是比较稳定的分子,科学家利用化学装置实现两种分子的耦合转化,其原理如图所示。请写出电极A的电极反应式:
您最近一年使用:0次
【推荐3】 等温室气体会让地球“发烧”,将
等温室气体会让地球“发烧”,将 进行综合利用是目前的研究热点。回答下列问题:
进行综合利用是目前的研究热点。回答下列问题:
(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚 已有广泛应用。
已有广泛应用。
反应I: ;
;
反应Ⅱ: 。
。
则
___________ 。
(2) 催化加氢制取甲醇
催化加氢制取甲醇 ,反应如下:
,反应如下:
主反应: ;
;
副反应: 。
。
在一定条件下,向某 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应。实验测得
发生反应。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图所示:
的选择性随温度变化如图所示: 的选择性
的选择性 。
。
①图中表示平衡时 的选择性的曲线为
的选择性的曲线为___________ (填“ ”或“
”或“ ”),温度高于
”),温度高于 时,曲线
时,曲线 随温度升高而升高的原因是
随温度升高而升高的原因是___________ 。
② 时,反应
时,反应 容器内达到平衡状态时,压强为
容器内达到平衡状态时,压强为 ,副反应的
,副反应的 ,初始充入
,初始充入 的物质的量a=
的物质的量a=___________ mol,主反应的平衡常数
___________ 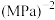 (用平衡分压代替平衡浓度,分压=总压×物质的量分数,计算结果用分数表示)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数,计算结果用分数表示)。
(3)利用 与
与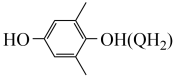 电解转化法从烟气中分离
电解转化法从烟气中分离 的原理如图(已知气体可选择性通过膜电极,溶液不能通过)。
的原理如图(已知气体可选择性通过膜电极,溶液不能通过)。___________ 极。
②纯净的 从
从___________ (填“出口1”或“出口2”)排出, 在
在 极上发生反应的离子方程式为
极上发生反应的离子方程式为___________ 。
 等温室气体会让地球“发烧”,将
等温室气体会让地球“发烧”,将 进行综合利用是目前的研究热点。回答下列问题:
进行综合利用是目前的研究热点。回答下列问题:(1)通过使用不同的新型催化剂,实现二氧化碳加氢合成转化为二甲醚
 已有广泛应用。
已有广泛应用。反应I:
 ;
;反应Ⅱ:
 。
。则

(2)
 催化加氢制取甲醇
催化加氢制取甲醇 ,反应如下:
,反应如下:主反应:
 ;
;副反应:
 。
。在一定条件下,向某
 恒容密闭容器中充入
恒容密闭容器中充入 和
和 发生反应。实验测得
发生反应。实验测得 的平衡转化率和平衡时
的平衡转化率和平衡时 的选择性随温度变化如图所示:
的选择性随温度变化如图所示: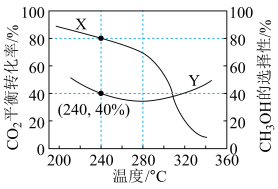
 的选择性
的选择性 。
。①图中表示平衡时
 的选择性的曲线为
的选择性的曲线为 ”或“
”或“ ”),温度高于
”),温度高于 时,曲线
时,曲线 随温度升高而升高的原因是
随温度升高而升高的原因是②
 时,反应
时,反应 容器内达到平衡状态时,压强为
容器内达到平衡状态时,压强为 ,副反应的
,副反应的 ,初始充入
,初始充入 的物质的量a=
的物质的量a=
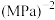 (用平衡分压代替平衡浓度,分压=总压×物质的量分数,计算结果用分数表示)。
(用平衡分压代替平衡浓度,分压=总压×物质的量分数,计算结果用分数表示)。(3)利用
 与
与 电解转化法从烟气中分离
电解转化法从烟气中分离 的原理如图(已知气体可选择性通过膜电极,溶液不能通过)。
的原理如图(已知气体可选择性通过膜电极,溶液不能通过)。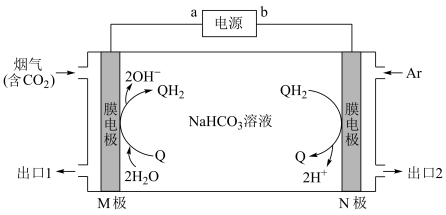
②纯净的
 从
从 在
在 极上发生反应的离子方程式为
极上发生反应的离子方程式为
您最近一年使用:0次


 反应
反应


