明胶是水溶性蛋白质混合物、溶于水会形成胶体。工业明胶制成的胶囊中往往含有超标的重金属Cr,因而对人体造成伤害。
(1)用一束光照射明胶水溶液,可观察到______ 现象。
(2)Na2CrO4是工业上常用的氧化剂,工业上可用FeCr2O4(Cr元素的化合价为+3)制Na2CrO4,其反应为FeCr2O4+8Na2CO3+Na2CrO4+7O2 Na2CrO4+Fe2O3+8CO2↑。
Na2CrO4+Fe2O3+8CO2↑。
①FeCr2O4铁元素的化合价为_______ ,用氧化物的形式表示FeCr2O4的化学式:________
②该反应的氧化产物是_______ ;每生成1molNa2CrO4时,转移电子_____ mol。
(1)用一束光照射明胶水溶液,可观察到
(2)Na2CrO4是工业上常用的氧化剂,工业上可用FeCr2O4(Cr元素的化合价为+3)制Na2CrO4,其反应为FeCr2O4+8Na2CO3+Na2CrO4+7O2
 Na2CrO4+Fe2O3+8CO2↑。
Na2CrO4+Fe2O3+8CO2↑。①FeCr2O4铁元素的化合价为
②该反应的氧化产物是
更新时间:2016-12-09 10:48:43
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】现有以下物质:①NaOH溶液;②液氨;③BaCO3固体;④熔融KHSO4;⑤Fe(OH)3胶体;⑥铜;⑦CO2;⑧CH3COOH;⑨蔗糖;⑩矿泉水请回答下列问题:
(1)以上物质中属于混合物的是_______ (填序号),以上物质中属于电解质的是_______ (填序号);以上纯净物中能导电的是_______ (填序号)。
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是_______
(3)写出④在水溶液中的电离方程式_______ 。
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式_______ 。
(1)以上物质中属于混合物的是
(2)在小烧杯中加入20 mL蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和FeCl3溶液,继续煮沸至溶液呈红褐色,即制得Fe(OH)3胶体。证明制备出Fe(OH)3胶体的操作方法是
(3)写出④在水溶液中的电离方程式
(4)在①溶液中缓缓通入过量的CO2可生成酸式盐,写出反应的离子方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】(1)除去Fe(OH)3胶体中混有的FeCl3的方法是_________________ 。
(2)在一定条件下,某固态化合物X受热分解的反应为:2X A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为
A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为_______ 。
(3)将标准状况下的a L HCl气体溶于1 L水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为________________ 。
(4)现有某温度下饱和NaCl溶液V mL,密度为ρg•cm-3,物质的量浓度为C mol•L-1则该温度下NaCl的溶解度为_________________ (用V、ρ、C表示)。
(5)有A、B、C、D 四种可溶性盐,它们的阳离子是Ba2+、Ag+、Na+、Cu2+ 中的某一种,阴离子是NO3-、SO42-、Cl-、CO32- 的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,C盐的溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
A、____________ C、______________ D、______________
(2)在一定条件下,某固态化合物X受热分解的反应为:2X
 A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为
A↑+B↑+2C↑,测得反应后生成的混合气体的密度是同温同压下H2密度的12倍,则化合物X的摩尔质量为(3)将标准状况下的a L HCl气体溶于1 L水中,得到的盐酸密度为b g/cm3,则该盐酸的物质的量浓度为
(4)现有某温度下饱和NaCl溶液V mL,密度为ρg•cm-3,物质的量浓度为C mol•L-1则该温度下NaCl的溶解度为
(5)有A、B、C、D 四种可溶性盐,它们的阳离子是Ba2+、Ag+、Na+、Cu2+ 中的某一种,阴离子是NO3-、SO42-、Cl-、CO32- 的某一种。
①若把四种盐分别溶解于盛有蒸馏水的四支试管中,C盐的溶液呈蓝色。
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味气体逸出。
根据①②实验事实可推断它们的化学式为:
A、
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量 。反应方程式为:
。反应方程式为:
(1)用双线桥标出该反应中电子转移方向和数目________ 。
(2)氧化剂与还原剂的物质的量比是________ ;在标况下,若生成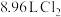 ,则转移的电子数为
,则转移的电子数为________  。
。
 。反应方程式为:
。反应方程式为:
(1)用双线桥标出该反应中电子转移方向和数目
(2)氧化剂与还原剂的物质的量比是
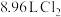 ,则转移的电子数为
,则转移的电子数为 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题:
(1)中国古代著作中有“银针验毒”的记录,其原理为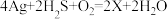 ,则X的化学式是
,则X的化学式是___________ ,其中H2S在该反应中___________ (填标号)。
A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作:
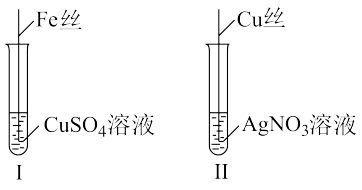
充分反应后观察到的现象是:I中铁丝上附着一层红色的铜,II中铜丝上附着一层光亮的银,结合I、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为___________ 。
(3)在Fe、Fe2+、Fe3+、S2-、I-、S中,只有氧化性的是___________ ,只有还原性的是___________ ,既有氧化性又有还原性的是___________ 。
(1)中国古代著作中有“银针验毒”的记录,其原理为
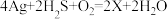 ,则X的化学式是
,则X的化学式是A.作氧化剂 B.作还原剂
C.既是氧化剂又是还原剂 D.既不是氧化剂又不是还原剂
(2)按如图所示操作:

充分反应后观察到的现象是:I中铁丝上附着一层红色的铜,II中铜丝上附着一层光亮的银,结合I、Ⅱ实验现象可知Fe2+、Cu2+、Ag+的氧化性由强到弱的顺序为
(3)在Fe、Fe2+、Fe3+、S2-、I-、S中,只有氧化性的是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】硒是动物和人体所必需的微量元素之一,在周期表中信息如图所示。完成下列填空:

(1)Se元素在周期表中的位置为___ 。表中78.96的意义为__ 。Se原子最外层电子排布的轨道表示式为___ 。
(2)从原子结构角度解释硫的非金属性大于硒___ 。
(3)硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种___ (选填“极性、或非极性”)分子,其空间结构为___ 型。
(4)工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式___ 。理论上该反应每转移1mol电子,可得到SeO2的质量为___ g,得到SO2在标准状况下的体积为___ L。

(1)Se元素在周期表中的位置为
(2)从原子结构角度解释硫的非金属性大于硒
(3)硒化氢(H2Se)是一种有恶臭味的有毒气体,是一种
(4)工业上常用浓H2SO4焙烧CuSe的方法提取硒,反应产生SO2、SeO2的混合气体,写出反应的化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】根据已经学过的化学知识,回答下列问题。
Ⅰ.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现___________ 性;___________ (填“能”或“不能”)用氢氧化钠溶液代替。
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:___________ 。
Ⅱ.物质的量是学习化学的基础。
(3)在标准状况下8.96 L CO2的分子数为___________ 。
(4)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是___________ 。
(5)质量分数为24%、密度为1.18g/m3的NaClO溶液的物质的量浓度约为___________ mol·L-1(计算结果保留一位小数)。在用NaClO固体配制100mL  溶液过程中,下列操作中能使所配溶液的浓度偏高的有
溶液过程中,下列操作中能使所配溶液的浓度偏高的有___________ (填序号)。
①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为___________ mol。
Ⅰ.金属及其化合物在生产生活中有着广泛的应用。
(1)胃舒平(主要成分为氢氧化铝)可用于治疗胃酸过多,氢氧化铝体现
(2)NaHSO4是一种酸式盐,写出NaHSO4在水中的电离方程式:
Ⅱ.物质的量是学习化学的基础。
(3)在标准状况下8.96 L CO2的分子数为
(4)19 g某二价金属的氯化物ACl2中含有0.4 mol Cl-,金属A的相对原子质量是
(5)质量分数为24%、密度为1.18g/m3的NaClO溶液的物质的量浓度约为
 溶液过程中,下列操作中能使所配溶液的浓度偏高的有
溶液过程中,下列操作中能使所配溶液的浓度偏高的有①用托盘天平称量时物品和砝码放反(托盘天平的最小砝码为1g)
②烧杯中固体溶解后未冷却直接转移定容
③转移前,容量瓶中含有少量蒸馏水
④定容时,加蒸馏水超过标线,又用胶头滴管吸出
⑤定容时,俯视刻度线
(6)根据反应14CuSO4+5FeS2+12H2O=7Cu2S+5FeSO4+12H2SO4,可知当有2.5 mol FeS2参加反应时,被氧化的硫元素的物质的量为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】过氧化氢(H2O2)可作为采矿业的废液消毒剂,如消除采矿废液中有剧毒的氰化钾(KCN,其中氮元素为-3价),化学方程式为KCN+H2O2+H2O===A+NH3↑(已配平),请回答下列问题:
(1)生成物A的化学式是________ 。
(2)该反应中发生氧化反应的物质是________ ,理由是______________________ 。
(3)若生成4分子NH3,转移电子数为________ 个。
(4)用双线桥表示电子转移的方向和数目___________________________ 。
(1)生成物A的化学式是
(2)该反应中发生氧化反应的物质是
(3)若生成4分子NH3,转移电子数为
(4)用双线桥表示电子转移的方向和数目
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】高铁酸钠是一种能氧化、杀菌、脱色、除臭的新型高效水处理剂。
(1)电解法生产高铁酸钠的原理是: ,
, 中铁元素的化合价为
中铁元素的化合价为___________ ,若生成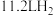 (标准状况),转移的电子数为
(标准状况),转移的电子数为___________ 。
(2)干法制备高铁酸钠的主要反应为: ,该反应中的还原剂是
,该反应中的还原剂是___________ ,生产1mol的高铁酸钠,需要消耗 的物质的量是
的物质的量是___________ mol。
(3)其净水过程中所发生的化学反应主要为:_____Na2FeO4+________H2O→_____Fe(OH)3(胶体)+_____NaOH+_____X↑,请推测X的化学式为___________ ,配平该化学方程式,将化学计量数标在上式横线处。___________
(1)电解法生产高铁酸钠的原理是:
 ,
, 中铁元素的化合价为
中铁元素的化合价为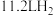 (标准状况),转移的电子数为
(标准状况),转移的电子数为(2)干法制备高铁酸钠的主要反应为:
 ,该反应中的还原剂是
,该反应中的还原剂是 的物质的量是
的物质的量是(3)其净水过程中所发生的化学反应主要为:_____Na2FeO4+________H2O→_____Fe(OH)3(胶体)+_____NaOH+_____X↑,请推测X的化学式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】铁是应用最广泛的金属,铁的卤化物,氧化物以及高价铁的含氧酸盐均为重要化合物。
(1)铁元素在周期表中的位置为_______ 。
(2)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。则x=_____ 。
(3)实验室用铁氰化钾确定某铁的氯化物中是否含有FeCl2,该反应的离子方程式为_____ 。
(4)Fe(OH)3固体与氢碘酸反应时可生成棕色物质的离子方程式为________ 。
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为_______ 。
(6)实验室准确称取1.44g草酸亚铁固体,在空气中灼烧,得到0.773g铁的氧化物,写出该铁的氧化物的化学式__________ 。
(1)铁元素在周期表中的位置为
(2)要确定铁的某氯化物FeClx的化学式,可利用离子交换和滴定的方法。实验中称取0.54 g的FeClx样品,溶解后先进行阳离子交换预处理,再通过含有饱和OH-的阴离子交换柱,使Cl-和OH-发生交换。交换完成后,流出溶液的OH-用0.40 mol·L-1的盐酸滴定,滴至终点时消耗盐酸25.0 mL。则x=
(3)实验室用铁氰化钾确定某铁的氯化物中是否含有FeCl2,该反应的离子方程式为
(4)Fe(OH)3固体与氢碘酸反应时可生成棕色物质的离子方程式为
(5)高铁酸钾(K2FeO4)是一种强氧化剂,可作为水处理剂和高容量电池材料。FeCl3和KClO在强碱性条件下反应可制取K2FeO4,其反应的离子方程式为
(6)实验室准确称取1.44g草酸亚铁固体,在空气中灼烧,得到0.773g铁的氧化物,写出该铁的氧化物的化学式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐3】(1)配平氧化还原反应方程式:
C2O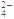 +
+____ MnO +____H+===____CO2↑+____Mn2++____H2O
+____H+===____CO2↑+____Mn2++____H2O
(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为________ mol。
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
KMnO4溶液在滴定过程中作________ (填“氧化剂”或“还原剂”),该滴定过程________ (填“需要”或“不需要”)另加指示剂。滴至16 mL时反应完全,此时溶液颜色由________ 变为__________ 。
C2O
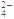 +
+ +____H+===____CO2↑+____Mn2++____H2O
+____H+===____CO2↑+____Mn2++____H2O(2)称取6.0 g含H2C2O4·2H2O、KHC2O4和K2SO4的试样,加水溶解,配成250 mL溶液。量取两份此溶液各25 mL,分别置于两个锥形瓶中。
①第一份溶液中加入酚酞试液,滴加0.25 mol·L-1NaOH溶液至20 mL时,溶液由无色变为浅红色。该溶液被中和的H+的总物质的量为
②第二份溶液中滴加0.10 mol·L-1的酸性高锰酸钾溶液。
KMnO4溶液在滴定过程中作
您最近一年使用:0次



