A、B、C、D是短周期中四种非金属元素,它们的原子序数依次增大.A元素原子核外只有一个电子.C、D元素在周期表中处于相邻的位置,B原子的最外层电子数是内层电子数的2倍,而D原子的最外层电子数是内层电子数的3倍.请回答下列问题:
(1)写出元素符号:A____________ D___________ .
(2)B元素在元素周期表中的位置是第_________ 周期、第__________ 族.
(3)A的单质和C的单质在一定条件下反应生成化合物X,X的化学式__________ ;向X 的水溶液中滴入酚酞溶液,会观察到__________ .
(1)写出元素符号:A
(2)B元素在元素周期表中的位置是第
(3)A的单质和C的单质在一定条件下反应生成化合物X,X的化学式
更新时间:2016-12-09 11:05:57
|
相似题推荐
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐1】A、B、C、D、E、F、G为原子序数依次增大的短周期主族元素。B、C、D均能与A形成10电子分子,E单质可用于野外焊接钢轨的原料,F与D同主族。
(1)D、E、F的离子半径由大到小的顺序为_______ (填离子符号)。
(2)写出能证明G比F非金属性强的一个化学方程式:_______ 。
(3)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2∶1∶6,甲的电子式为_______ ,该反应的化学方程式为_______ 。
(4)C能分别与A和D按原子个数比1∶2形成化合物乙和丙,乙的结构式为_______ 。常温下,液体乙与气体丙反应生成两种无污染的物质,该反应的氧化产物与还原产物的物质的量之比为_______ 。
(1)D、E、F的离子半径由大到小的顺序为
(2)写出能证明G比F非金属性强的一个化学方程式:
(3)F和G形成的一种化合物甲中所有原子均为8电子稳定结构,该化合物与水反应生成F单质、F的最高价含氧酸和G的氢化物,三种产物的物质的量之比为2∶1∶6,甲的电子式为
(4)C能分别与A和D按原子个数比1∶2形成化合物乙和丙,乙的结构式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
【推荐2】(1)下面是我们熟悉的物质:
①O2 ②SO2 ③CaCl2 ④HNO3 ⑤NaOH ⑥NH4Cl
这些物质中,属于共价化合物的是___________ ;属于离子化合物的是___________ ;只含离子键的是___________ 。
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。
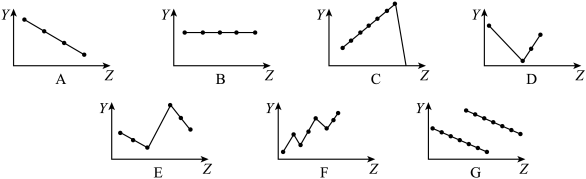
把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数________________ 。
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径________________ 。
③第二、三周期主族元素随原子序数递增原子半径的变化____________ 。
(3)已知某单核粒子的结构示意图为: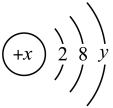
①当x-y=10时,该粒子为____________ (填“原子”、“阳离子”或“阴离子”)。
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是_____________ 。
(4)已知A、B、C、D是中学化学中常见的四种10电子微粒,
它们之间存在如图中转化关系。

请写出:A的化学式___________ (写一种);D的化学式___________ 。
①O2 ②SO2 ③CaCl2 ④HNO3 ⑤NaOH ⑥NH4Cl
这些物质中,属于共价化合物的是
(2)下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。

把与下面的元素有关性质相符的曲线的标号填入相应括号中:
①第ⅡA族元素的最外层电子数
②第三周期离子Na+、Mg2+、Al3+、P3-、S2-、Cl-的离子半径
③第二、三周期主族元素随原子序数递增原子半径的变化
(3)已知某单核粒子的结构示意图为:

①当x-y=10时,该粒子为
②当y=8时,若该微粒的氧化性很弱,得一个电子后变为原子,该微粒的符号是
(4)已知A、B、C、D是中学化学中常见的四种10电子微粒,
它们之间存在如图中转化关系。

请写出:A的化学式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】已知A、B、C、D、E、F、G是元素周期表前四周期的元素,且原子序数依次增大,其相关信息如下表所示:
回答下列问题:
(1)C元素位于第___________ 族___________ 区。
(2)A、B、C三种原子半径由大到小为___________ (用元素符号表示)。
(3)F元素基态原子的最高能级具有的原子轨道数为___________ ,该原子轨道呈___________ 形。
(4)D、E元素第一电离能大小比较为:___________ (用元素符号表示),原因是___________ 。
(5) 的电子排布式为
的电子排布式为___________ 。
(6)B、D形成的化合物能与水反应,化学方程式为___________ 。
| 元素代号 | 相关信息 |
| A | 原子核外有6种运动状态不同的电子 |
| B | 基态原子的最外层为3个未成对电子 |
| C | 电负性为4.0 |
| D | 其第一至第四电离能分别是: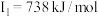 , ,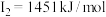 , ,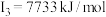 , ,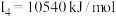 |
| E | 价层电子数等于其电子层数 |
| F | 基态原子的价层电子排布式为 |
| G | 基态原子核外有7个能级上有电子,且能量最高的能级上有6个电子 |
(1)C元素位于第
(2)A、B、C三种原子半径由大到小为
(3)F元素基态原子的最高能级具有的原子轨道数为
(4)D、E元素第一电离能大小比较为:
(5)
 的电子排布式为
的电子排布式为(6)B、D形成的化合物能与水反应,化学方程式为
您最近一年使用:0次
解答题-结构与性质
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、Q、E五种元素中,X原子的M层中只有两对成对电子,Y原子的L层上的电子数是K层的两倍,Z是地壳内含量(质量分数)最高的元素,Q的核电荷数是X与E的核电荷数之和,E在元素周期表中电负性最大。回答下列问题:
(1)Y、Z、Q三种元素可形成一种分子式为QYZ3的化合物。
①基态Q原子核外有___________ 种空间运动状态不同的电子。
②QYZ3分子中的阴离子的空间构型为_______________ 。
③X、Y两种元素的最高价氧化物对应水化物的酸性较强的是___________ (填化学式)。
(2)将足量的XZ2充入含有 的溶液中,发生反应的离子方程式为
的溶液中,发生反应的离子方程式为________ 。
(3)X的单质的常见形式为X8,其环状结构如图所示,则X的原子采用的轨道杂化方式是_______ 。
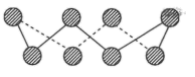
(4)YX2分子中,共价键的成键形式有_____ ,属于______ (填“极性分子”或“非极性分子”),写出与YX2具有相同空间构型和键合形式的分子:_______ (写一条即可)。
(1)Y、Z、Q三种元素可形成一种分子式为QYZ3的化合物。
①基态Q原子核外有
②QYZ3分子中的阴离子的空间构型为
③X、Y两种元素的最高价氧化物对应水化物的酸性较强的是
(2)将足量的XZ2充入含有
 的溶液中,发生反应的离子方程式为
的溶液中,发生反应的离子方程式为(3)X的单质的常见形式为X8,其环状结构如图所示,则X的原子采用的轨道杂化方式是

(4)YX2分子中,共价键的成键形式有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
解题方法
【推荐2】X、Y、Z、W、M、N是原子序数依次增大的前四周期元素,X的核外电子总数与其电子层数相同;Z和M同主族,且两者的单质室温下均为气体;W的原子序数为Y原子价电子数的3倍, 极易溶于水;基态
极易溶于水;基态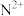 的d轨道半充满。由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。
的d轨道半充满。由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。

回答下列问题:
(1)基态W原子的价电子排布式为___________ ,其中电子占据最高能级的电子云轮廓图为___________ 形。写出N在周期表中的位置___________ 。
(2)W、M形成的一种化合物以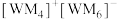 的形式存在,下列对
的形式存在,下列对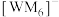 中心原子杂化方式推断合理的
中心原子杂化方式推断合理的___________ (填标号)。
a. b.
b. c.
c. d.
d.
(3)①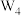 是W元素的常见单质,已知
是W元素的常见单质,已知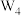 易溶于
易溶于 ,难溶于水,可能原因是
,难溶于水,可能原因是___________ 。
②W与M的第一电离能,W___________ M(填大于、小于或等于),从原子结构的角度解释原因___________ 。
(4)如果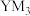 的水解产物是
的水解产物是 和HClO,则Y与M中电负性较大的是
和HClO,则Y与M中电负性较大的是___________ (填元素符号)。
 极易溶于水;基态
极易溶于水;基态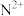 的d轨道半充满。由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。
的d轨道半充满。由上述元素中的四种组成的两种化合物常用于合成阻燃材料,其结构简式如图所示。
回答下列问题:
(1)基态W原子的价电子排布式为
(2)W、M形成的一种化合物以
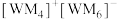 的形式存在,下列对
的形式存在,下列对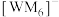 中心原子杂化方式推断合理的
中心原子杂化方式推断合理的a.
 b.
b. c.
c. d.
d.
(3)①
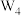 是W元素的常见单质,已知
是W元素的常见单质,已知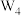 易溶于
易溶于 ,难溶于水,可能原因是
,难溶于水,可能原因是②W与M的第一电离能,W
(4)如果
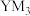 的水解产物是
的水解产物是 和HClO,则Y与M中电负性较大的是
和HClO,则Y与M中电负性较大的是
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】前四周期的A、B、C、D、E、F六种元素,原子序数依次增大。基态A原子核外电子的L层电子数是K层的2倍;B原子基态时的2p轨道上未成对的电子数最多;C元素为最活泼的非金属元素;D元素核外有3个电子层,最外层电子数是核外电子总数的 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
(1)E元素在周期表中位置为_______ ,E3+价电子轨道表示式为_______ 。
(2)B、C、F三种元素电负性由大到小的顺序为_______ (用元素符号表示),第一电离能D_______ (填“>”、“<”或“=”)Al,其原因是_______ 。
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是_______ (填化学式),理由是_______ 。
(4)F元素可能的性质_______ (填标号)。
 ;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。
;E元素正三价离子的3d轨道为半充满状态;F元素与B元素位于同一主族,其某种氧化物有剧毒。(1)E元素在周期表中位置为
(2)B、C、F三种元素电负性由大到小的顺序为
(3)相同条件下,A、B的简单氢化物在水中溶解度较大的是
(4)F元素可能的性质
| A.其单质可作半导体材料 |
| B.存在-3、+3、+5等多种化合价 |
| C.最高价氧化物对应的水化物是强酸 |
| D.单质还原性弱于磷单质 |
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐1】A、B、C、D、E、F六种元素均是短周期元素,且原子序数依次增大。B、F原子的最外层电子数均为其电子层数的两倍,D、F元素原子的最外层电子数相等。X、Y、Z、W、甲、乙六种物质均由上述元素的两种或三种元素组成,元素B形成的单质M与甲、乙均能反应(相对分子质量甲<乙)转化关系如图(反应条件略去),元素E形成的单质是 “21世纪的能源”,是目前应用最多的半导体材料。请回答下列问题:
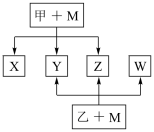
(1)写出M与甲的浓溶液加热时反应的化学方程式___________
(2)X、Y、Z、W属于同一类物质,这类化合物通常熔沸点较___________ (填“高”或“低”); X、Y、W都能与Z反应,则Z的结构式为___________
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=___________ ,写出反应的化学方程式___________
(4)化合物ED2与元素B形成的某种单质能在高温下能发生置换反应,若反应中有1mol电子发生了转移,则参加反应的化合物ED2的质量为___________ g。
(5)元素B的另一种单质能导电,具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12g该单质中含有___________ NA个正六边形。

(1)写出M与甲的浓溶液加热时反应的化学方程式
(2)X、Y、Z、W属于同一类物质,这类化合物通常熔沸点较
(3)将X、W与D2按1∶1∶n的物质的量之比通入Z中,充分反应后无气体剩余或生成,则n=
(4)化合物ED2与元素B形成的某种单质能在高温下能发生置换反应,若反应中有1mol电子发生了转移,则参加反应的化合物ED2的质量为
(5)元素B的另一种单质能导电,具有平面层状结构,同一层中的原子构成许许多多的正六边形,则12g该单质中含有
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐2】A、B、C、D、E、F为常见的原子序数依次增大的短周期元素,B、C、D、E、F的简单离子的电子层结构相同,A和E同主族,且原子的最外层电子数的关系为A+D=B+F=8。请回答:
(1)试写出B2单质的电子式为__________ 。试写出由上述元素组成的分子中含有4个原子核且为18电子结构的物质的化学式______________ 。
(2)含F元素对应的金属阳离子的溶液中滴加过量E的最高价氧化物对应水化物的溶液,其离子方程式是__________________________ 。
(3)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色单质,且产物对大气无污染,其化学反应方程式是____________________________ 。
(4)在2 L的密闭容器中,通入2 mol B2气体和3 mol A2气体,一定温度下反应生成BA3气体,当反应达到平衡时,A2的浓度为0.15 mol·L-1,同时放出约83.2 kJ的热量,该反应的热化学方程式为______________________________________________________ 。
(5)已知某化合物EB3与水可以反应生成两种气体单质和一种碱,试写出其化学方程式_____________ ;若0.1 mol该化合物完全反应,转移电子的物质的量为____________ 。
(1)试写出B2单质的电子式为
(2)含F元素对应的金属阳离子的溶液中滴加过量E的最高价氧化物对应水化物的溶液,其离子方程式是
(3)已知B2A4与BA3具有相似的性质,B2A4通过炽热的氧化铜粉末,粉末由黑色变为红色单质,且产物对大气无污染,其化学反应方程式是
(4)在2 L的密闭容器中,通入2 mol B2气体和3 mol A2气体,一定温度下反应生成BA3气体,当反应达到平衡时,A2的浓度为0.15 mol·L-1,同时放出约83.2 kJ的热量,该反应的热化学方程式为
(5)已知某化合物EB3与水可以反应生成两种气体单质和一种碱,试写出其化学方程式
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】现有A、B、C、D四种短周期主族元素,其原子序数依次增大。已知A、C位于同一主族,A在周期表中原子半径最小。B、D的最外层电子数相等,且B、D的原子序数之和为A、C原子序数之和的两倍。请回答下列问题:
(1)元素D在周期表中的位置是________________________ 。
(2)C2B2所含的化学键类型有___________ ;请写出C2B2与A2B反应的离子方程式________________ 。
(3)元素B、C形成的简单离子中半径较大的是_________ (写电子式)。
(4)仅由C、D两种元素组成的一种盐溶于水后pH>7的原因是_____________ (用离子方程式表示)。
(5)如图所示以铂作电极,以C、D两元素的最高价氧化物的水化物X、Y的溶液作为电解质溶液,A、B元素的单质分别在两电极上发生原电池反应,则通入B单质的电极反应式为_________ ,通入A单质的X溶液的pH将__________ (填“增大”、“不变”或“减小”)。

(1)元素D在周期表中的位置是
(2)C2B2所含的化学键类型有
(3)元素B、C形成的简单离子中半径较大的是
(4)仅由C、D两种元素组成的一种盐溶于水后pH>7的原因是
(5)如图所示以铂作电极,以C、D两元素的最高价氧化物的水化物X、Y的溶液作为电解质溶液,A、B元素的单质分别在两电极上发生原电池反应,则通入B单质的电极反应式为

您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐1】X、Y、Z、M是元素周期表中前20号元素,其原子序数依次增大,且X、Y、Z相邻。X的核电荷数是Y的核外电子数的一半,Y与M可形成化合物M2Y。用微粒符号完成下列问题:
(1)Y、Z两种元素的最高价氧化物的水化物酸性___________ 强于___________ 。
(2)M、Z、Y形成的简单离子的半径的大小________________ 。
(3)M2X2固体中阴、阳离子个数比____________ ,其电子式为_______________ 。该物质中含有化学键的类型有______________ 和______________ 。
(4)将Z的单质通入YX2的水溶液中发生反应的离子方程式为____________ 。
(1)Y、Z两种元素的最高价氧化物的水化物酸性
(2)M、Z、Y形成的简单离子的半径的大小
(3)M2X2固体中阴、阳离子个数比
(4)将Z的单质通入YX2的水溶液中发生反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
名校
【推荐2】A、B、C、D、E、F是六种短周期元素,它们的原子序数依次增大;A元素的原子是半径最小的原子;B元素的最高价氧化物对应水化物与其气态氢化物反应生成一种盐X;D与A同主族,且与F同周期;F元素的最外层电子数是其次外层电子数的3/4倍,A、B、D、F这四种元素,每一种与C元素都能形成元素的原子个数比不相同的若干种化合物。D、E、F三种元素对应的最高价氧化物的水化物间两两皆能反应。
请回答下列问题:
(1)写出B、C、E元素的名称B_________ 、C___________ 、E____________ ;
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为_______________ ;
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)_________________ ;
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为____________ 。
(5)A、C、D、F四种元素可以形成两种酸式盐 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为_____ 、______ ,这两种酸式盐相互反应的离子方程式为______________________ 。
请回答下列问题:
(1)写出B、C、E元素的名称B
(2)写出C、D两种元素形成的原子个数比为1:1的物质的电子式为
(3)可以验证C和F两种元素非金属性强弱的结论是(填编号)
①比较这两种元素的气态氢化物的沸点
②比较这两种元素的单质与氢气化合的难易程度
③比较这两种元素的气态氢化物的还原性
④比较这两种元素反应中得电子的多少
(4)向E的硝酸盐溶液中滴加过量D的最高价氧化物的水化物溶液,反应的离子方程式为
(5)A、C、D、F四种元素可以形成两种酸式盐
 均由四种元素组成
均由四种元素组成 ,这两种酸式盐的化学式分别为
,这两种酸式盐的化学式分别为
您最近一年使用:0次
解答题-无机推断题
|
较难
(0.4)
解题方法
【推荐3】Ⅰ.几种短周期元素的原子半径及主要化合价如下表:已知X是短周期中最活泼的金属,且与R同周期。(请用化学用语答题)
(1)R的元素符号为_______ ; M在元素周期表中的位置为___________________ 。
(2)X与Y按原子个数比1:1构成的物质的电子式为________ ;所含化学键类型________ 。
(3)X+, Y2‾,M2‾ 离子半径大小顺序为________________________________ 。
(4)将YM2通入FeCl3溶液中的离子方程式_________________________________ 。
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式_________________________ 。
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为____________________________ 。
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为______________________________ 。
元素代号 | X | Y | Z | M | R |
原子半径/nm | 0.186 | 0.102 | 0.075 | 0.074 | 0.143 |
主要化合价 | +1 | +6 -2 | +5 -3 | -2 | +3 |
(2)X与Y按原子个数比1:1构成的物质的电子式为
(3)X+, Y2‾,M2‾ 离子半径大小顺序为
(4)将YM2通入FeCl3溶液中的离子方程式
(5)用Cu单质作阳极,石墨作阴极,X的最高价氧化物对应的水化物溶液作电解液进行电解,写出阳极的反应式
Ⅱ.如下图转化关系

①若B为白色胶状不溶物,则A与C反应的离子方程式为
②若向B溶液中滴加铁氰化钾溶液会产生特征蓝色沉淀,则A与C反应的离子方程式为
您最近一年使用:0次



